
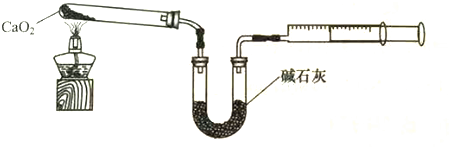
分析 (1)第①步中氯化銨和氫氧化鈣發生復分解反應生成一水合氨和氯化鈣;
第②步反應中,氯化鈣、雙氧水、一水合氨和水反應生成CaO2•8H2O和氯化銨;
(2)第①步中氯化銨參加反應、第②步中生成氯化銨;
H2O2價格較高且易分解;
(3)實驗室用硝酸酸化的硝酸銀溶液檢驗;
(4)CaO2能和水反應,氧氣能抑制CaO2分解;
(5)根據過氧化鈣和氧氣之間的關系式計算;
過氧化鈣的含量也可用重量法測定,需要測定的物理量有樣品質量和反應后固體質量.
解答 解:(1)第①步中氯化銨和氫氧化鈣發生復分解反應生成一水合氨和氯化鈣,反應方程式為2NH4Cl+Ca(OH)2=2NH3•H2O+CaCl2;
第②步反應中,氯化鈣、雙氧水、一水合氨和水反應生成CaO2•8H2O和氯化銨,反應方程式為CaCl2+H2O2+2NH3•H2O+6H2O=CaO2•8H2O↓+2NH4Cl;
故答案為:2NH4Cl+Ca(OH)2=2NH3•H2O+CaCl2;CaCl2+H2O2+2NH3•H2O+6H2O=CaO2•8H2O↓+2NH4Cl;
(2)第①步中氯化銨參加反應、第②步中生成氯化銨,所以可以循環使用的物質是NH4Cl;
H2O2價格較高且易分解,堿性條件下抑制CaO2•8H2O溶解,所以工業上常采用Ca(OH)2過量而不是H2O2過量的方式來生產;
故答案為:NH4Cl;H2O2價格較高且易分解,堿性條件下抑制CaO2•8H2O溶解;
(3)實驗室用硝酸酸化的硝酸銀溶液檢驗,如果沉淀沒有洗滌干凈,向洗滌液中加入硝酸酸化的硝酸銀溶液應該有白色沉淀,其檢驗方法是:取少量最后一次洗滌上清液,然后向洗滌液中加入少量硝酸酸化的硝酸銀溶液,如果產生白色沉淀就證明沒有洗滌干凈,否則洗滌干凈,
故答案為:取少量最后一次洗滌上清液,然后向洗滌液中加入少量硝酸酸化的硝酸銀溶液,觀察溶液是否產生白色沉淀,如果產生白色沉淀就證明沒有洗滌干凈,否則洗滌干凈;
(4)CaO2能和水反應生成氫氧化鈣和氧氣,CaO2在350℃迅速分解生成CaO和O2,所以通入氧氣能抑制超氧化鈣分解;
故答案為:防止過氧化鈣和水反應、防止過氧化鈣分解;
(5)設超氧化鈣質量為x,
2CaO2$\frac{\underline{\;350℃\;}}{\;}$2CaO+O2↑
144g 22.4L
x 10-3VL
144g:22.4L=x:10-3VL
x=$\frac{144g×1{0}^{-3}VL}{22.4L}$=$\frac{144V}{22400}$g=$\frac{9V}{1400}g$,
其質量分數=$\frac{\frac{9V}{1400}g}{mg}×100%$=$\frac{9V}{14m}$%,
過氧化鈣的含量也可用重量法測定,需要測定的物理量有樣品質量和反應后固體質量,
樣品質量和反應后固體質量,
故答案為:$\frac{9V}{14m}$%;樣品質量和反應后固體質量.
點評 本題考查制備實驗方案評價,為高頻考點,側重考查離子檢驗、化學反應方程式的書寫、物質含量測定等知識點,明確實驗原理及物質性質是解本題關鍵,難點是題給信息的挖掘和運用.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
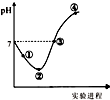 常溫下,將Cl2緩慢通入一定量的水中至飽和,然后向所得飽和氯水中逐滴加入0.1mol•L-1的氫氧化鈉溶液,整個過程中pH變化如圖所示,下列有關敘述正確的是( )
常溫下,將Cl2緩慢通入一定量的水中至飽和,然后向所得飽和氯水中逐滴加入0.1mol•L-1的氫氧化鈉溶液,整個過程中pH變化如圖所示,下列有關敘述正確的是( )| A. | 曲線起點處水的電離程度最大,可用pH試紙測定溶液pH | |
| B. | ②點之前所發生反應的離子方程式為Cl2+H2O=2H++Cl-+ClO- | |
| C. | 氯氣~氯水體系中:c(H+)=c(Cl2)+c(HClO)+c(ClO-) | |
| D. | ③點所示溶液中:c(Na+)=c(Cl-)+c(ClO-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cu和Fe相連插入某溶液中形成原電池,則Fe一定作負極 | |
| B. | MgCl2中混有少量的FeCl3,可以通過溶解,加入過量MgO、過濾、結晶等操作進行提純 | |
| C. | 用惰性電極電解CuSO4溶液一段時間后,若需加入適量的Cu(OH)2才能使溶液恢復到電解前狀態,說明陰極只有Cu2+被還原 | |
| D. | 將Fe、Cu的混合物投入FeCl2和CuCl2的混合溶液中,最后可能只有Fe剩余 |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北石家莊辛集中學高二上階段考一化學卷(解析版) 題型:填空題
“立方烷”是一種新合成的烴,其分子為正方體結構,其碳架結構如圖所示。

(1)立方烷的分子式為______________。
(2)該立方烷與氯氣發生取代反應,生成的一氯代物有_________種,生成的二氯代物有____________種。
(3)若要使1mol該烷烴的所有氫原子全部被氯原子取代,需要_________mol氯氣。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北石家莊辛集中學高二上階段考一化學卷(解析版) 題型:選擇題
下列實驗中不能獲得成功的是( )
A. 用水檢驗苯和溴苯 B. 苯、濃硫酸、濃硝酸共熱制硝基苯
C. 用溴水除去混在苯中的己烯 D. 苯、液溴、溴化鐵混合制溴苯
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北石家莊辛集中學高二上階段考一化學卷(解析版) 題型:選擇題
已知PbI2的Ksp = 7.0×l0-9,將7.5×l0-3 mol•L-1 的KI與一定濃度的Pb(NO3)2溶液按2∶1的體積比混合,則生成PbI2沉淀所需Pb(NO3)2溶液的最小濃度為( )
A. 8.4×l0-4 mol•L-1 B.5.6×l0-4 mol•L-1 C.4.2×l0-4 mol•L-1 D.2.8×l0-4 mol•L-1
查看答案和解析>>
科目:高中化學 來源:2017屆吉林省長春市高三上學期期中考試化學試卷(解析版) 題型:選擇題
短周期元素X、Y、Z、W的原子序數依次增大,W與X同主族,Y的最外層電子數是電子層數的3倍,Y與W核外電子數相差6,Z的最外層電子數等于電子層數。下列說法正確的是
A. X、Y、W元素的原子半徑依次遞增
B. Z、W分別與Y形成的化合物均可作為耐高溫材料
C. X、W分別與Y形成化合物在常溫下均為氣態
D. X、Z、W元素的最高價氧化物的水化物的酸性依次遞增
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com