
【題目】為測定Na2SO3、Na2SO4混合樣品ag中Na2SO3的質量分數,下列方案不合理的是
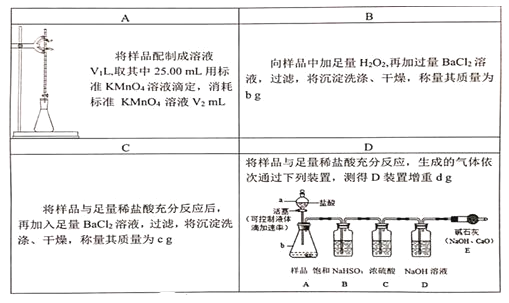
A. AB. BC. CD. D
【答案】A
【解析】
A. Na2SO3與KMnO4溶液發生氧化還原反應,可以通過KMnO4的量求出Na2SO3的量,但是只給出KMnO4的體積,未給出KMnO4溶液的濃度,無法求得Na2SO3的物質的量及其質量分數,A錯誤;
B.H2O2將Na2SO3氧化成Na2SO4,加足量BaCl2溶液將硫酸根沉淀得到BaSO4沉淀,根據沉淀的質量可以求得氧化后Na2SO4總物質的量,根據元素守恒及混合物樣品質量,可得Na2SO3、Na2SO4的物質的量,可以求得Na2SO3的質量分數,B正確;
C.鹽酸與Na2SO3反應,BaCl2與Na2SO4反應轉化成BaSO4沉淀,求出Na2SO4的質量,根據樣品總質量可求出Na2SO3的質量,最后求出Na2SO3的質量分數,C正確;
D. 鹽酸與Na2SO3反應產生SO2氣體,SO2氣體中會混有雜質HCl,用飽和NaHSO3吸收HCl,再用濃硫酸干燥SO2氣體后,通入NaOH溶液,測量增重質量dg,進一步計算出Na2SO3的質量分數,D正確;
故合理選項是A。


科目:高中化學 來源: 題型:
【題目】取碘水四份于試管中,編號為Ⅰ、Ⅱ、Ⅲ、Ⅳ,分別加入汽油、![]() 、酒精、NaCl溶液,振蕩后靜置,現象正確的是
、酒精、NaCl溶液,振蕩后靜置,現象正確的是![]()
![]()
A.Ⅰ中溶液分層,下層呈紫紅色B.Ⅱ中溶液分層,下層呈紫紅色
C.Ⅲ中溶液分層,下層呈黃褐色D.Ⅳ中溶液不分層,溶液由黃褐色變成黃綠色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為測定某銅器表面Cux(OH)yClz(Cu為+2價,x、y、z為正整數)的組成,現進行如下實驗:取少量Cux(OH)yClz,將其完全溶解于稀硝酸中,將所得溶液分成兩等份。向其中一份滴加足量AgNO3溶液,將所得沉淀過濾、洗滌、干燥,得到固體0.1435 g。向另一份中加入0.1000 mol·L1 EDTA(已知Cu2+與EDTA反應的化學計量數比為1∶1),恰好完全反應時消耗EDTA 20mL。則Cux(OH)yClz的化學式中y的值為( )
A.1B.2C.3D.4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據Mg能在CO2中燃燒,某興趣小組推測Na應該也能在CO2中燃燒,且固體產物可能為C、Na2O和Na2CO3中的兩種或三種。該小組用如下圖裝置進行了實驗探究。已知PdCl2能被CO還原得到黑色的Pd。
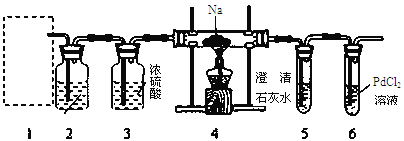
回答下列問題:
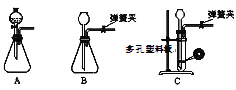
(1)為了使反應隨開隨用,隨關隨停,上圖虛線方框內應選用____裝置(填下圖字母代號),如何檢驗所選裝置的氣密性_____。
(2)裝置2中所盛試劑為_______。
A.NaOH溶液 B.飽和NaHCO3溶液
C.飽和Na2CO3溶液 D.飽和NaCl溶液
(3)檢測裝置的氣密性完好并裝好藥品后,在點燃酒精燈前應先進行裝置1中的反應操作,待觀察到_____現象時,再點燃酒精燈,這步操作的目的是________。
(4)由實驗現象和進一步的探究得出反應機理。
A.裝置6中有黑色沉淀生成;
B.取反應后直玻管中的固體物質23.0g溶于足量的水中,無氣泡產生且得到澄清的溶液;將溶液加水稀釋配成250 mL的溶液;
C.取25.00ml步驟B的溶液,滴加足量BaCl2溶液,將生成的白色沉淀過濾、洗滌、干燥,稱量得固體質量為1.97g。
①步驟C中不溶物干燥前必須經過洗滌,如何檢驗該沉淀是否洗滌干凈____。
②該探究得出鈉與二氧化碳反應的化學方程式為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在兩個密閉容器中,分別充有質量相同的甲、乙兩種氣體,若兩容器的溫度和壓強均相同,且甲的密度大于乙的密度,則下列說法正確的是( )
A.甲的分子數比乙的分子數多
B.甲的摩爾體積比乙的摩爾體積小
C.甲的相對分子質量比乙的相對分子質量小
D.甲的物質的量比乙的物質的量少
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯水中含有多種成分,因而具有多種性質,根據新制氯水分別與如圖四種物質發生的反應填空(a、b、c、d、e中重合部分代表物質間反應,且氯水足量)。
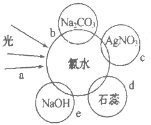
(1)能證明氯水具有漂白性的是___(填“a”“b”“c”或“d”);
(2)c過程中的現象是___;
(3)e過程中的化學方程式為___;
(4)實驗室保存飽和氯水的方法是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)6.02×1023個氫氧根離子的物質的量是________mol,其摩爾質量為________。
(2)在標準狀況下,0.01mol某氣體的質量為0.44g,則該氣體的密度為________g·L-1(保留小數點后兩位),該氣體的相對分子質量為________。
(3)將4g NaOH固體溶于水配成250mL溶液,此溶液中NaOH的物質的量濃度為______;取出10mL此溶液,將此10mL溶液加水稀釋到100mL,稀釋后溶液中NaOH的物質的量濃度為______。
(4)硫通常是一種淡黃色晶體,它的蒸氣有橙色、無色、紅棕色等多種,它們都是硫的單質,但是每個分子中硫原子的個數不同,可用Sx表示,對下列蒸氣測定的結果是:無色蒸氣的密度是同狀況下氫氣密度的64倍,則它的分子式為:______。
(5)把18.0mol/L的濃硫酸稀釋成2.00mol/L的稀硫酸100mL,下列操作對所配溶液濃度造成的后果,屬于“偏低”的是______________
①未洗滌稀釋過濃硫酸的小燒杯;
②使用經蒸餾水洗滌后未干燥的小燒杯稀釋濃硫酸;
③加水時不慎超過了刻度線,又將超出部分用吸管吸出;
④配溶液用的容量瓶用蒸餾水洗滌后未經干燥;
⑤定容時俯視刻度;
⑥倒轉容量瓶搖勻后,液面降至刻度線下,再加水至刻度。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖,A、B、C、D、E各代表碳、鐵、二氧化碳、硫酸銅溶液、氫氧化鋇溶液中的一種物質。一定條件下,相連環物質間能發生反應,不相連環物質間不能發生反應,且B的相對分子質量大于D。請填空:
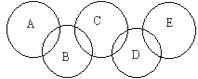
(1)寫出下列物質的化學式:A_____,B_____,D_____。
(2)寫出下列反應的離子方程式:B+C:_____________________。
(3)相連環物質間發生的反應中,氧化還原反應共有___________個。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種三室微生物燃料電池污水凈化系統原理如圖所示,圖中有機廢水中有機物可用C6H10O5表示。下列有關說法正確的是:

A. b電極上發生氧化反應
B. b電極附近溶液的pH增大
C. a電極反應式:C6H10O5+24e-+7H2O===6CO2↑+24H+
D. 中間室:Na+移向左室,Cl-移向右室
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com