
下列各組離子在相應的條件下一定能大量共存的是
A.在堿性溶液中:CO32-、K+、S2-、Na+
B.與鋁粉反應放出氫氣的無色溶液中:NO3-、Mg2+、Na+、SO42-
C.在c(H+)/c(OH-)==1×1012的溶液中:NH4+、AlO2-、C1-、K+
D.在中性溶液中:Fe3+、C1-、NO3-、A13+
科目:高中化學 來源:2014-2015學年廣東省佛山市高三上學期第一次月考化學試卷(解析版) 題型:選擇題
設NA為阿伏加德羅常數的數值,下列說法正確的是
A.1mol S在足量O2中燃燒,轉移的電子數為6 NA
B.標況下,22.4L氦氣含有的原子數為2NA
C.28 g C2H4中含有2 NA個碳原子
D.0.1 mol·L-1的碳酸氫鈉溶液中含鈉離子數為0.1NA
查看答案和解析>>
科目:高中化學 來源:2016屆貴州省貴陽市高三8月摸底考試化學試卷(解析版) 題型:選擇題
二氧化碳和鈉在一定條件下可制得金剛石,其化學方程式為3CO2+4Na=2X+C(金剛石)。設NA為阿伏加德羅常數的值,下列有關此反應的敘述不正確的是
A.金剛石是自然界最堅硬的單質
B.1 mol CO2中含有的共用電子對數目為2NA
C.46g Na完全反應需要標準狀況下CO2的體積為33.6L
D.當有0.4mo1 Na參與反應時,被還原的CO2的分子數目為0.1 NA
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省等六校教研會高三第一次聯考化學試卷(解析版) 題型:選擇題
在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1 mol的混合溶液中加入0.1 mol鐵粉,充分攪拌后鐵完全反應,同時析出0.1 mol Ag。則下列結論中不正確的是
A、向反應后的溶液中繼續加入少量鐵粉,鐵粉可以繼續溶解
B、氧化性:Ag+>Fe3+>Cu2+>Zn2+
C、反應后溶液的質量減輕
D、反應后溶液中Cu2+與Fe2+的物質的量之比為1∶1
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省等六校教研會高三第一次聯考化學試卷(解析版) 題型:選擇題
根據原子結構及元素周期律的知識,下列推斷正確的是
A、同主族元素含氧酸的酸性隨核電荷數的增加而減弱
B、核外電子排布相同的微粒化學性質也相同
C、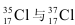 得電子能力相同
得電子能力相同
D、F-、O2-、Mg2+、Na+半徑逐漸減小
查看答案和解析>>
科目:高中化學 來源:2016屆四川省高三秋季零診考試化學試卷(解析版) 題型:選擇題
能正確表示下列反應的離子方程式是
A.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2 (s)+ 2Fe3+(aq)= 2Fe(OH)3 (s)+ 3Mg2+(aq)
B.鈉與CuSO4溶液反應:2Na + Cu2+ = Cu↓ + 2Na+
C.已知:酸的強弱H2CO3>HClO>HCO3-,則:2ClO-+ CO2(少量)+ H2O ===CO32-+ 2HClO
D.將足量的NaHCO3溶液加入少量澄清石灰水中:Ca2+ + OH- + HCO3- = CaCO3↓ + H2O
查看答案和解析>>
科目:高中化學 來源:2016屆湖北省高三普通班8月月考化學試卷(解析版) 題型:選擇題
某溶液中含有大量NH4+、Na+、HCO3ˉ、CO32ˉ、CH3COO-,加入足量的Na2O2固體后,溶液中離子濃度基本保持不變的是(假設溶液體積無變化)
A.Na+ B.CO32ˉ
C.CH3COO- D.NH4+
查看答案和解析>>
科目:高中化學 來源:2015-2016學年海南華僑中學高二上會考模擬化學試卷(解析版) 題型:選擇題
下列各組性質比較中,正確的是
①失電子能力: K>Na>Li ②堿性: NaOH >Mg(OH)2>Al(OH)3
③氧化性:F>Si>O ④穩定性:PH3 <H2S<HCl
A.①②③ B.②③④ C.①②④ D.①③④
查看答案和解析>>
科目:高中化學 來源:2016屆吉林省高三上學期第一次模擬化學試卷(解析版) 題型:填空題
(15分)原子序數依次增大的四種元素A、B、C、D分別處于第一至第四周期,自然界中存在多種A的化合物,B原子核外電子有6種不同的運動狀態,B與C可形成正四面體形分子,D的基態原子的最外能層只有一個電子,其他能層均已充滿電子。請回答下列問題:
(1)這四種元素中電負性最大的元素,其基態原子的價電子排布圖為 ,第一電離能最小的元素是 (填元素符號)。
(2)C所在主族的前四種元素分別與A形成的化合物,沸點由高到低的順序是 (填化學式),呈現如此遞變規律的原因是 。
(3)B元素可形成多種單質,一種晶體結構如圖一所示,其原子的雜化類型為 、另一種的晶胞如圖二所示,該晶胞的空間利用率為 ,若此晶胞中的棱長為356.6 pm,則此晶胞的密度為 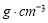 (保留兩位有
(保留兩位有 效數字)。(
效數字)。(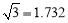 )
)
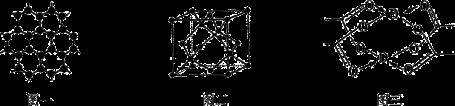
(4)D元素形成的單質,其晶體的堆積模型為 ,D的醋酸鹽晶體局部結構如圖三,該晶體中含有的化學鍵是 (填選項序號)。
①極性鍵 ②非極性鍵 ③配位鍵 ④金屬鍵
(5)向D的硫酸鹽溶液中滴加過量氨水,觀察到的現象是 。請寫出上述過程的離子方程式: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com