
短周期元素A、B、C的原子序數之和為37,A、B在同一周期,A+、C-具有相同的核外電子層結構。下列推測不正確的是( )
A. 同周期元素中C的氫化物穩定性最強
B. 同周期元素中A的金屬性最強
C. 原子半徑:A>B,離子半徑:A+>C-
D. A、B、C的簡單離子中,會破壞水的電離平衡的是C
 小天才課時作業系列答案
小天才課時作業系列答案 一課四練系列答案
一課四練系列答案 黃岡小狀元滿分沖刺微測驗系列答案
黃岡小狀元滿分沖刺微測驗系列答案 新輔教導學系列答案
新輔教導學系列答案科目:高中化學 來源:2017屆內蒙古高三上9月月考化學卷(解析版) 題型:選擇題
下列各組物質相互混合反應后,最終有白色沉淀生成的是( )
①少量Ca( OH)2投入過量NaHCO3溶液中
OH)2投入過量NaHCO3溶液中
②過量NaOH溶液和明礬溶液混合
③金屬鈉投入到FeCl2中
④向NaAlO2溶液中通入過量CO2[
⑤向飽和Na2CO3溶液中通入過量CO2
A.①②③④⑤ B.只有①④⑤ C.只有②③ D.只有③④
D.只有③④
查看答案和解析>>
科目:高中化學 來源:2017屆江西省高三上學期第二次段考化學試卷(解析版) 題型:選擇題
化學在工農業生產和日常生活中都有著重要的應用。下列說法錯誤的是( )
A.利用催化設施,可以將汽車尾氣中CO和NO轉化為無害氣體
B.半導體行業中有一句話:“從沙灘到用戶”,計算機芯片的材料是二氧化硅
C.鍋爐水垢中含有 的CaSO4,可先用Na2CO3溶液處理,后用酸除去
的CaSO4,可先用Na2CO3溶液處理,后用酸除去
D.防止酸雨發生的重要措施之一是使用清潔能源
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省無錫市三校聯合體高三上第一次月考化學試卷(解析版) 題型:選擇題
從海帶中制取單質碘需要經過灼燒、溶解、過濾、氧化、萃取、分液、蒸餾等操作。下列圖示對應的裝置合理、操作規范的是

A.灼燒 B.過濾 C.分液 D.蒸餾
查看答案和解析>>
科目:高中化學 來源:2017屆湖南省益陽市高三上學期第二次月考化學試卷(解析版) 題型:填空題
鋅是一種常用金屬,鎵(Ga)的化合物氮化鎵(GaN)是制造LED的重要材料,被譽為第三代半導體材料。
I.鎵(Ga)是火法冶煉鋅過程中的副產品,鎵與鋁同主族且相鄰,化學性質與鋁相似。
⑴Ga的原子結構示意圖為 ___________________。
⑵GaN可由Ga和NH3在高溫條件下制取,該反應的化學方程式 。
⑶下列有關鎵和鎵的化合物的說法正確的是____ 。
A.常溫下,Ga可與水劇烈反應放出氫氣
B.一定條件下,Ga可溶于鹽酸和氫氧化鈉
C.一定條件下,Ga2O3可與NaOH反應生成鹽
D.Ga2O3可由Ga(OH)3受熱分解得到
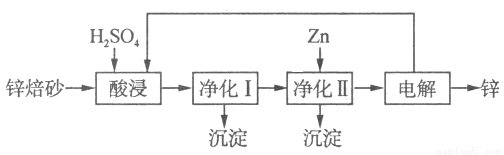
II.鋅的冶煉方法有火法和濕法。工業上利用鋅焙砂(主要含ZnO、ZnFe2O4,還含有少量CaO、FeO、CuO、NiO等氧化物)濕法制取金屬鋅的流程如圖所示:
已知:Fe的活潑性強于Ni
⑷ZnFe2O4可以寫成ZnO·Fe2O3,ZnFe2O4與H2SO4反應的化學方程式為 。
⑸凈化I操作分為兩步:第一步是將溶液中少量的Fe2+氧化;第二步是控制溶液pH,只使Fe3+轉化為Fe(OH)3沉淀。凈化I生成的沉淀中還含有溶液中的懸浮雜質,溶液中的懸浮雜質被共同沉淀的原因是____________________。
⑹凈化II中加入Zn的目的是___________________。
⑺常溫下,凈化I中,如果要使c(Fe3+) < 10-5 mol/L,則應控制溶液pH的范圍為_____________。已知:Ksp[Fe(OH)3] = 8.0 × 10-38;lg5 = 0.7
查看答案和解析>>
科目:高中化學 來源:2017屆湖南省益陽市高三上學期第二次月考化學試卷(解析版) 題型:選擇題
下列實驗能達到預期目的的是( )
編號 | 實驗內容 | 實驗目的 |
A | 室溫下,用pH試紙分別測定濃度為18mol/L和0.1 mol·L—1H2SO4溶液的pH | 比較不同濃度H2SO4的酸性強弱 |
B | 向含有酚酞的Na2CO3溶液中加入少量BaC12固體,溶液紅色變淺 | 證明Na2CO3溶液中存在水解平衡 |
C | 向10mL 0.2 mol·L—1 NaOH溶液中滴入2滴0.1 mol·L—1MgCl2溶液,產生白色沉淀后,再滴加2滴0.1 mol·L—1FeCl3溶液,又生成紅褐色沉淀 | 證明在相同溫度下的 Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
D | 配制FeCl2溶液時,先將FeCl2溶于適量濃鹽酸中,再用蒸餾水稀釋到所需濃度,最后在試劑瓶中加入少量銅粉 | 抑制Fe2+水解,并防止Fe2+被氧化 |
查看答案和解析>>
科目:高中化學 來源:2017屆四川省校高三上學期第二次月考化學試卷(解析版) 題型:填空題
【化學-選修3:物質結構與性質】
A、B、C、D、E五種元素的原子序數依次增大。A是原子半價最小的元素;B的最外層電子數是次外層電子數的2倍;D的L能層有兩對成對電子;E+的核外有三個能層,且都外于全滿狀態。試回答下列問題:
(1)基態D原子核外電子的排布式為___________________。
(2)B、C、D三種元素的電負性由大到小的順序是_______________________(填元素符號)。
(3)E(NH3)2+ 4離子的顏色是___________;含有化學鍵類型是_________________;離子中N原子雜化軌道類型是_________________。
(4)D、E能形成兩種晶體,其晶胞分別如甲、乙兩圖。晶體乙中,E的配位數為_________;在一定條件下,甲和C2A4反應生成乙,同時生成在常溫下分別為氣體和液體的另外兩種常見無污染物質。該化學反應方程式為___________________________。

(5)若甲的密度為ρ g/cm3,NA表示阿伏加德羅常數,則甲晶胞的邊長可表示為_________cm。
查看答案和解析>>
科目:高中化學 來源:2017屆湖南省實驗班高三上第一次質檢化學試卷(解析版) 題型:選擇題
瓦斯爆炸是煤礦開采中的重大危害,一種瓦斯分析儀(如圖甲)在煤礦巷道中的甲烷濃度達到一定值時,其傳感器就可以顯示。該瓦斯分析儀工作原理類似燃料電池的工作原理,其裝置如圖乙所示,其中的固體電解質是Y2O3-Na2O,O2-可以在其中自由移動。下列有關敘述正確的是

A.瓦斯分析儀工作時,電池內電路中電子由電極b流向電極a
B.電極b是正極,O2-由電極a流向電極b
C.電極a的反應式為CH4+4O2--8e- CO2+2H2O
CO2+2H2O
D.當固體電解質中有1 mol O2-通過時,電子轉移4 mol
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省高二上第一次考試化學卷(解析版) 題型:選擇題
肼(N2H4)是火箭發動機的燃料,它與N2O4反應時,N2O4為氧化劑,生成氮氣和水蒸氣。已知:
N2(g)+2O2(g)=N2O4(g) ΔH=+8.7 kJ/mol,
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534.0 kJ/mol,
下列表示肼跟N2O4反應的熱化學方程式,正確的是( )
A.2N2H4(g)+N2O4(g)=3N2(g) +4H2O(g) ΔH=-542.7 kJ/mol
B.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ΔH=-1059.3 kJ/mol
C.N2H4(g)+ N2O4(g)=
N2O4(g)= N2(g)+2H2O(g) ΔH=-1076.7 kJ/mol
N2(g)+2H2O(g) ΔH=-1076.7 kJ/mol
D.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ΔH=-1076.7 kJ/mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com