
分析 根據n=$\frac{m}{M}$計算出5.6g鐵離子的物質的量,再根據硫酸鐵化學式計算出溶液中硫酸根離子的物質的量,再根據c=$\frac{n}{V}$計算出溶液中SO42-的物質的量濃度.
解答 解:n(Fe3+ )=$\frac{5.6g}{56g/mol}$=0.1mol,根據化學式可知Fe2(SO4)3得150mL該溶液中含有硫酸根離子的物質的量為0.1mol×$\frac{3}{2}$=0.15mol,
則溶液中SO42-的物質的量濃度為:c(SO42-)=$\frac{0.15mol}{0.15L}$=1mol/L,
故答案為:1mol/L.
點評 本題考查了物質的量濃度的計算,題目難度中等,明確物質的量濃度的概念及表達式為解答關鍵,注意熟練掌握物質的量與摩爾質量、物質的量濃度之間的關系,試題培養了學生的化學計算能力.


科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4 L H2O中含有氫原子數目為2NA | |
| B. | 17 g NH3所含質子數為10NA | |
| C. | 0.1mol Cu(NO3)2中含有的離子數目為0.2NA | |
| D. | 28g N2 體積為22.4L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
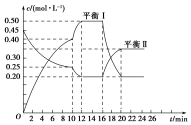 向一容積不變的密閉容器中充入一定量A和B,發生如下反應:xA(g)+2B(s)?yC(g)△H<0在一定條件下,容器中A、C的物質的量濃度隨時間變化的曲線如圖所示.請回答下列問題:
向一容積不變的密閉容器中充入一定量A和B,發生如下反應:xA(g)+2B(s)?yC(g)△H<0在一定條件下,容器中A、C的物質的量濃度隨時間變化的曲線如圖所示.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
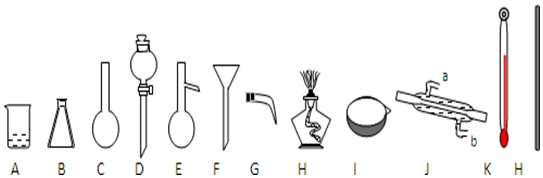
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化鈉溶液與稀鹽酸反應:H++OH-=H2O | |
| B. | 鐵和稀鹽酸反應:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 碳酸鈉溶液與稀鹽酸反應:Na2CO3+2H+=2Na++H2O+CO2↑ | |
| D. | 氫氧化鋇溶液與稀硫酸反應:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
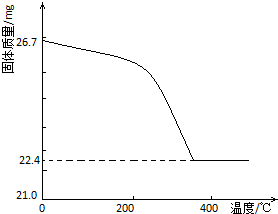 工業上從廢鉛酸電池的鉛膏回收鉛的過程中,可用碳酸鹽溶液與鉛膏(主要成分為PbSO4)發生反應:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).某課題組用PbSO4為原料模擬該過程,探究上述反應的實驗條件及固體產物的成分.
工業上從廢鉛酸電池的鉛膏回收鉛的過程中,可用碳酸鹽溶液與鉛膏(主要成分為PbSO4)發生反應:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).某課題組用PbSO4為原料模擬該過程,探究上述反應的實驗條件及固體產物的成分.| 實驗步驟(不要求寫出具體操作過程) | 預期的實驗現象和結論 |
| 取一定量樣品充分干燥,… |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
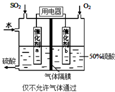 回答下列問題:
回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 75mL 2mol•L-1FeCl3溶液 | B. | 25mL 2mol•L-1KCl溶液 | ||
| C. | 150mL 1mol•L-1NaCl溶液 | D. | 20mL 1.5mol•L-1 MgCl2溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com