
【題目】(1)0.5 mol H2O的質量為____ ,含有______個原子。
(2)質量都是50 g的 HCl、CH4、N2三種氣體中,原子數目最多的是氣體是_______ ,在相同溫度和相同壓強條件下,密度最大的氣體是__________ 。
(3)標準狀況下11.2L,由CO和H2組成的混合氣體的質量為7.2g,則混合氣體的平均摩爾質量為_______。
(4)實驗室需用濃硫酸配制100 mL 1 molL-1的稀硫酸。可供選用的儀器有:
①量筒;②燒杯;③膠頭滴管,還必須需要的玻璃儀器有________________ (寫儀器名稱)。
(5)一定條件下,RO![]() 和Cl2可發生如下反應:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,從而可知在RO
和Cl2可發生如下反應:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,從而可知在RO![]() 中,元素R的化合價是_____,當有標準狀況下8.96L Cl2被消耗時,反應中共轉移電子物質的量為____mol。
中,元素R的化合價是_____,當有標準狀況下8.96L Cl2被消耗時,反應中共轉移電子物質的量為____mol。
【答案】 9g 1.5NA或9.03x1023 CH4 HCl 14.4g/moL 玻璃棒、100ml容量瓶 +4 0.8
【解析】(1)本題考查物質的量與質量、微粒個數之間關系,0.5molH2O的質量為0.5×18g=9g,0.5molH2O中含有原子物質的量為(0.5×2+0.5×1)mol=1.5mol,原子個數為1.5NA或9.03×1023;(2)本題考查微粒個數、物質的量、質量之間的關系,以及阿伏加德羅推論的運用,依據n=m/M,n=N/NA,50gHCl的物質的量為50/36.5mol≈1.4mol,含有原子物質的量為1.4×2mol=2.8mol,50gCH4的物質的量為50/16mol=3.125mol,含有原子物質的量為3.125×5mol=15.625mol,50gN2的物質的量為50/28mol≈1.8mol,含有原子物質的量為1.8×2mol=3.6mol,因此原子數目最多的氣體是CH4,根據阿伏加德羅推論,相同溫度、相同壓強下,密度之比等于其摩爾質量之比,HCl的摩爾質量為36.5g·mol-1,CH4摩爾質量為16g·mol-1,N2的摩爾質量為28g·mol-1,因此密度最大的是HCl;(3)考查n=m/M,以及V/Vm=n,混合氣體物質的量為11.2/22.4mol=0.5mol,混合氣體平均摩爾質量為7.2/0.5g·mol-1=14.4g·mol-1;(4)考查配制一定物質的量濃度溶液的需要的儀器,配制100mL1mol·L-1的稀硫酸需要的儀器是量筒、燒杯、玻璃棒、膠頭滴管、100mL容量瓶,因此缺少的儀器是玻璃棒、100mL容量瓶;(5)考查離子反應方程式,氧化還原反應得失電子數目的計算,根據離子反應方程式,反應前后所帶電荷數守恒,n=2,RO3n-中R的化合價為+4,根據離子反應方程式,氯氣中Cl的化合價降低,因此轉移電子物質的量為8.96×2×1/22.4mol=0.8mol。


科目:高中化學 來源: 題型:
【題目】硫酸銅是一種重要的化工產品。某工廠用刻蝕印刷電路板產生的堿性廢液[含較多[Cu(NH3)4]2+及少量Cu2+、NH4+、NH3和Cl-]制備硫酸銅晶體,流程如下:
(1)通過“中和、沉淀和過濾”可得堿式氯化銅[Cu(OH)Cl]固體,請將生成該固體的反應的離子方程式補充完整:[Cu(NH3)4]2+ +。
(2)制備Cu(OH)Cl沉淀時,溶液的pH對銅元素含量的影響如下圖所示:
①若要提高Cu(OH)Cl沉淀的量,應將溶液的pH控制在(填字母序號)。
A. <5.2 B. 5.2~5.8 C. >5.8
②pH< 5.2 時,隨pH減小,溶液中銅元素含量增大,其原因用反應的離子方程式可表示為。
(3)“化漿、酸化"過程可得到硫酸銅粗品,發生的反應為Cu(OH)Cl+ 4H2O+ H2SO4= CuSO4·5H2O+ HCl。則硫酸銅粗品中,含銅元素的雜質為 , 檢驗樣品中含有該雜質的方法是:取少量硫酸銅粗品,加入適量水使其充分溶解,。
(4)硫酸銅粗品還需要通過重結晶法進行提純,具體操作是:將粗晶體溶解于熱水中形成飽和溶液,然后加入適量乙醇,攪拌,冷卻,過濾并洗滌,得到高純度的硫酸銅晶體。加入乙醇能夠提高硫酸銅的產率,從溶解性角度解釋其可能的原因是。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】幾位同學分組對四種無色溶液分別進行離子檢驗,給出實驗結果如下。你認為其中明顯錯誤的是
A.K+、Ca2+、Cl-、NO3-B.Cu2+、NO3-、OH-、HCO3-
C.Na+、OH-、Cl-、CO32-D.Mg2+、K+、SO42-、Na+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質在水中的電離方程式書寫錯誤的是
A.CaCl2=Ca2++2Cl-B.Ba(OH)2=Ba2++OH2-
C.KOH=K++OH-D.H2SO4=2H++SO42-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】T℃時,在某容積恒為2L密閉容器中充入2molN2、4molH2 , 在催化劑輔助下發生反應:N2(g)+3H2(g)2NH3(g)△H=﹣92.0kJ/mol.t0時刻,建立平衡后,測得生成NH3的量為2mol;從t1時刻開始,改變反應的一個條件,體系中反應速率隨時間變化的情況,如圖所示. 
試回答下列問題:
(1)T℃時,t0時刻,建立平衡后N2的轉化率為: , 該反應的平衡常數K= .
(2)t1時刻,改變的外界條件是 .
(3)t4時刻,改變的外界條件是 ,
(4)平衡常數K(t5~t6)K(t7~t8)(填“>、<或=”,下同).分析原因是 .
(5)T℃時,建立平衡后,向容器中加入2molN2和2molNH3 , 則此時 v正v逆 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖表示在密閉容器中反應:2SO2+O22SO3+Q達到平衡時,由于條件改變而引起反應速度和化學平衡的變化情況,a b過程中改變的條件可能是;bc過程中改變的條件可能是; 若增大壓強時,反應速度變化情況畫在c~d處 . 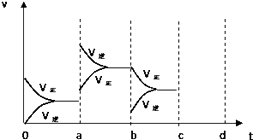
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下反應A(g)+B(g)C(g)△H<0達到平衡后,據下列圖象判斷:
達到新的平衡對應的圖象 | 平衡移動方向 | |
(i)使用催化劑 | ||
(ii)升溫 | ||
(iii)降壓 | ||
(iv)增加A的量 | ||
(v)減少C的量 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】媒化學小組設計了細下的實驗裝置制取Cl2和SO2,并研究它們的漂白性。請問答:

(1)若用裝置A 制取Cl2,可選擇二氧化錳固體和濃鹽酸,反應的離子方程式為_______。若用裝置B制取SO2,可選擇亞硫酸鈉固體和濃硫酸,反應的化學方程式為__________。
(2)反應開始一段時間后,觀察到C、D兩個試管中的品紅溶液_______(填寫序號)。
①都褪色 ②都不褪色 ③C褪色,D不褪色 ④C不褪色,D褪色
停止通氣后,取下C、D,再分別給C、D 兩個試管加熱,兩個試管中的現象分別為C:______,D:_______。
(3)燒杯E中可盛裝_______(填化學式)溶液,其作用是____________。
(4)某同學將制得的SO2和Cl2等體積混合后通入到品紅溶液中,觀察到的現象是________,用離子方程式表示產生該現象的原因_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某無色溶液中含有的金屬陽離子為Mg2+、Al3+,向該溶液中緩慢地滴入NaOH溶液直至過量,產生沉淀的物質的量與加入NaOH的物質的量的關系如圖所示。

(1)由此確定原溶液中一定還大量含有某陽離子,它可能是________。
(2)若溶質為MgCl2和Al2(SO4)3,則原溶液中鋁離子的物質的量為______________。
(3)下列圖象中,橫坐標表示加入試劑或通入氣體的物質的量,縱坐標表示產生沉淀的質量,用圖象的序號或文字回答下列問題:

Ⅰ.表示向AlCl3溶液中逐漸滴加NaOH溶液的是______;
Ⅱ.表示向NaAlO2溶液中逐漸滴加稀鹽酸的是________;
Ⅲ.表示向NaAlO2溶液中通入CO2的是________;
Ⅳ.③圖____________(填“能”或“不能”)代表向含NaOH的澄清石灰水中通入CO2。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com