
分析 (1)紅棕色固體粉末1.60g是,物質的量是1.60g÷160g/mol=0.01mol,則根據鐵元素守恒可知3.96 g化合物A中含有Fe元素的物質的量為0.02mol.將所得濾液在一定條件下蒸發可得到一種純凈的不含結晶水的鹽10.44g,該物質是硫酸鉀,物質的量是10.44g÷174g/mol=0.06mol,則鉀離子的物質的量是0.12mol,其中有0.08mol是氫氧化鉀中的鉀離子,因此3.96 g化合物A中含有鉀元素的物質的量為0.04mol.則根據質量守恒可知氧元素的物質的量是$\frac{3.96g---0.02mol×56g/mol-0.04mol×39g/mol}{16g/mol}=0.08mol$,則K、Fe、O三種元素的個數之比是2:1:4,所以化合物A的化學式為K2FeO4.
(2)A在水溶液中不穩定,一段時間后轉化為紅褐色沉淀,這說明反應中有氫氧化鐵生成;
(3)由于高鐵酸鉀溶于水能分解生成氫氧化鐵紅褐色測定,因此探究溫度對化合物A水溶液穩定性的影響實驗方案可設計為將適量K2FeO4固體溶解水并等分為兩份,然后做對比實驗.
解答 解:(1)紅棕色固體粉末1.60g是,物質的量是1.60g÷160g/mol=0.01mol,則根據鐵元素守恒可知3.96 g化合物A中含有Fe元素的物質的量為0.02mol.將所得濾液在一定條件下蒸發可得到一種純凈的不含結晶水的鹽10.44g,該物質是硫酸鉀,物質的量是10.44g÷174g/mol=0.06mol,則鉀離子的物質的量是0.12mol,其中有0.08mol是氫氧化鉀中的鉀離子,因此3.96 g化合物A中含有鉀元素的物質的量為0.04mol.則根據質量守恒可知氧元素的物質的量是$\frac{3.96g---0.02mol×56g/mol-0.04mol×39g/mol}{16g/mol}=0.08mol$,則K、Fe、O三種元素的個數之比是2:1:4,所以化合物A的化學式為K2FeO4.
根據以上分析,3.96g化合物A中含有Fe元素的物質的量為0.02mol,含有鉀元素的物質的量為0.04mol.化合物A的化學式為K2FeO4;
故答案為:0.02;0.04;K2FeO4;
(2)由上述分析可知,A的化學式為:K2FeO4,高鐵酸鉀與水反應生成氧氣和Fe(OH)3、氫氧化鉀,反應方程式為4K2FeO4+10H2O=4Fe(OH)3+8KOH+3O2↑,離子方程式為4FeO42-+10H2O=4Fe(OH)3↓+3O2↑+8OH-,
故答案為:4FeO42-+10H2O=4Fe(OH)3↓+3O2↑+8OH-;
(3)其方法為:將適量K2FeO4固體溶解水并等分為兩份,置于不同溫度的恒溫水浴中,底部各放一張畫有“+”字的白紙,觀察記錄看不到“+”字所需時間,
故答案為:將適量K2FeO4固體溶解水并等分為兩份,置于不同溫度的恒溫水浴中,底部各放一張畫有“+”字的白紙,觀察記錄看不到“+”字所需時間.
點評 本題考查無機物推斷,屬于計算型推斷,綜合考查學生閱讀題目獲取信息的能力、計算能力、設計實驗能力等,需要學生具有扎實的基礎知識與靈活運用知識解決問題的能力,題目難度中等.


 金牌教輔培優優選卷期末沖刺100分系列答案
金牌教輔培優優選卷期末沖刺100分系列答案科目:高中化學 來源: 題型:解答題
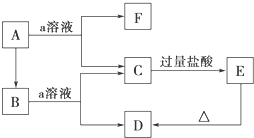
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molSO2(g)的能量總和大于lmolS(s)和lmolO2(g)的能量總和 | |
| B. | 將2molSO2(g)與lmolO2(g)在一定條件下充分反應,放出196.6kJ的熱量 | |
| C. | S(g)+O2(g)→SO2(g)+Q,Q值小于297.16kJ | |
| D. | 當lmolS(s)完全轉化為SO3(g)時(假設無熱量損失),放出395.46kJ的熱量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 34 | B. | 8.5 | C. | 17 | D. | 16 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 溫度一定,一個化學反應的平衡常數是一個常數 | |
| B. | 兩種物質反應,不管怎樣書寫化學方程式,平衡常數不變 | |
| C. | 溫度一定時,對于給定的化學反應,正、逆反應的平衡常數互為倒數 | |
| D. | 濃度商Qc<Kc,v(正)<v(逆) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
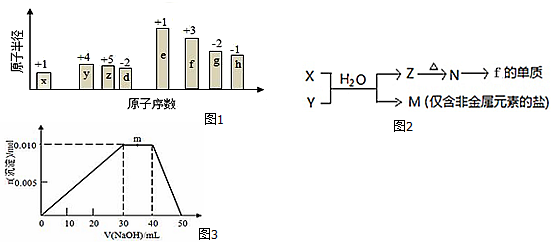
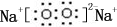 ;B是常見的液態化合物,其稀溶液易被催化分解,可使用的催化劑為AB.(填序號)
;B是常見的液態化合物,其稀溶液易被催化分解,可使用的催化劑為AB.(填序號)查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③⑥⑤④⑧⑦⑨ | B. | ①②⑤③⑥④⑧⑦⑨ | C. | ①②③④⑤⑧⑥⑦⑨ | D. | ①②③⑤⑥④⑧⑦⑨ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 若I中裝過量高錳酸鉀溶液,Ⅱ中裝澄清石灰水,則能檢驗SO2中是否混有CO2 | |
| B. | 若I中裝足量澄清石灰水,Ⅱ中裝濃硫酸,則能測定CO2和水蒸氣的混合氣體中水蒸氣的含量 | |
| C. | 若I中裝足量飽和碳酸鈉溶液,Ⅱ中裝濃硫酸,則能除去CO2中混有的HCl | |
| D. | 若I中裝BaCl2溶液,Ⅱ中裝水,則能證明SO2和NO2混合氣體中SO2不與BaCl2反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
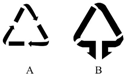 呵護生存環境,共建和諧社會是當今社會的主題.
呵護生存環境,共建和諧社會是當今社會的主題.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com