“西氣東輸”工程使北京用上了更加清潔的能源--天然氣(主要成分是CH
4)。在使用天然氣以前北京用的煤氣主要是將碳與水蒸氣在高溫下反應制得的水煤氣,水煤氣的主要成分是CO和H
2,兩者的體積比約為
1:1。 已知:CO的燃燒熱△H=-283.0 kJ/mol;H
2的燃燒熱△H=-286.0 kJ/mol;CH
4的燃燒熱△H=-890.0 kJ/mol。
(1)用H
2為原料設計成氫氧燃料電池(電解質溶液為KOH),正極的電極反應式是:_______________。
(2)已知:
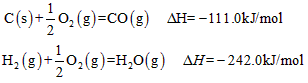
寫出由C(s)與H
2O(g)反應生成水煤氣的熱化學方程式:______________________。
(3)忽略水煤氣中其它成分,若獲得相等的熱量,所需相同狀況下水煤氣與甲烷的體積比約為_______;排放的CO
2物質的量的比約為_________。通過計算得知:使用天然氣能______(填“增多”或“減少”)溫室氣體(CO
2)的排放。(各種燃料均完全燃燒)
(4)若將由amolCH
4、CO和H
2組成的混合氣體完全燃燒,生成CO
2氣體和液態水時放出熱量(Q)的取值范圍是___________。

 小天才課時作業系列答案
小天才課時作業系列答案 一課四練系列答案
一課四練系列答案 黃岡小狀元滿分沖刺微測驗系列答案
黃岡小狀元滿分沖刺微測驗系列答案 新輔教導學系列答案
新輔教導學系列答案