
【題目】某汽車安全氣囊的產氣藥劑主要含有 NaN3、Fe2O3、KClO4、NaHCO3 等物質。當汽車發生碰撞時,產氣藥劑產生大量氣體使氣囊迅速膨脹,從而起到保護作用。
(1) NaN3 是氣體發生劑,受熱分解產生 N2 和 Na,N2 的電子式為___________________。
(2) Fe2O3是主氧化劑,與 Na 反應生成的還原產物為_____________ (已知該反應為置換反應)。
(3) KClO4是助氧化劑,反應過程中與 Na 作用生成 KCl 和 Na2O。KClO4 含有化學鍵的類型為_____________________,K 的原子結構示意圖為________________。
【答案】:NN: Fe 離子鍵和共價鍵 · ·
·
【解析】
(1)N2分子中N原子之間形成3對共用電子對,據此書寫其電子式;
(2)Fe2O3是氧化劑,與Na發生置換反應,據此分析;
(3)KClO4由鉀離子與高氯酸根離子構成,據此分析其所含的化學鍵;K原子質子數為19原子核外有4個電子層,據此分析。
(1)由8電子結構可知,N2分子中N原子之間形成3對共用電子對,其電子式為::NN:;故答案::NN:;
(2)Fe2O3是主氧化劑,與Na發生置換反應,Fe元素發生還原反應,則還原產物為Fe,故答案:Fe;
(3)KClO4由鉀離子與高氯酸根離子構成,高氯酸根離子中Cl原子與O原子之間形成共價鍵,即該物質含有離子鍵、共價鍵;K原子質子數為19,原子核外有4個電子層,各層電子數為2、8、8、1;
故答案:離子鍵和共價鍵; 。
。


科目:高中化學 來源: 題型:
【題目】(一)碳酸鑭![]() 可用于治療終末期腎病患者的高磷酸鹽血癥,制備反應原理為:2LaCl3+6NH4HCO3═La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O;某化學興趣小組利用下列裝置實驗室中模擬制備碳酸鑭。
可用于治療終末期腎病患者的高磷酸鹽血癥,制備反應原理為:2LaCl3+6NH4HCO3═La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O;某化學興趣小組利用下列裝置實驗室中模擬制備碳酸鑭。

(1)制備碳酸鑭實驗流程中導管從左向右的連接順序為:F→_____→_____→_____→_____→_____;
(2)Y中發生反應的化學反應式為_______________;
(3)X中盛放的試劑是___________,其作用為___________________;
(4)Z中應先通入![]() ,后通入過量的
,后通入過量的![]() ,原因為__________________;
,原因為__________________;
二、氫氧化鈰![]() 是一種重要的稀土氫氧化物,它可由氟碳酸鈰精礦(主要含
是一種重要的稀土氫氧化物,它可由氟碳酸鈰精礦(主要含![]() )經如下流程獲得:
)經如下流程獲得:

已知:在酸性溶液中![]() 有強氧化性,回答下列問題:
有強氧化性,回答下列問題:
(5)氧化焙燒生成的鈰化合物二氧化鈰(![]() ),其在酸浸時反應的離子方程式為_________________;
),其在酸浸時反應的離子方程式為_________________;
(6)已知有機物HT能將![]() 從水溶液中萃取出來,該過程可表示為:
從水溶液中萃取出來,該過程可表示為:![]() (水層)+
(水層)+![]() (有機層)
(有機層)![]()
![]() +
+![]() (水層)從平衡角度解釋:向
(水層)從平衡角度解釋:向![]() (有機層)加入
(有機層)加入![]() 獲得較純的含
獲得較純的含![]() 的水溶液的原因是________________;
的水溶液的原因是________________;
(7)已知298K時,Ksp[Ce(OH)3]=1×10-20,為了使溶液中![]() 沉淀完全,需調節pH至少為________;
沉淀完全,需調節pH至少為________;
(8)取某![]() 產品0.50g,加硫酸溶解后,用
產品0.50g,加硫酸溶解后,用![]() 的
的![]() 溶液滴定至終點(鈰被還原成
溶液滴定至終點(鈰被還原成![]() ).(已知:
).(已知:![]() 的相對分子質量為208)
的相對分子質量為208)
①![]() 溶液盛放在________(填“酸式”或“堿式”)滴定管中;
溶液盛放在________(填“酸式”或“堿式”)滴定管中;
②根據下表實驗數據計算![]() 產品的純度____________;
產品的純度____________;
滴定次數 |
| |
滴定前讀數 | 滴定后讀數 | |
第一次 | 0.50 | 23.60 |
第二次 | 1.00 | 26.30 |
第三次 | 1.20 | 24.10 |
③若用硫酸酸化后改用![]() 的
的![]() 溶液滴定產品從而測定
溶液滴定產品從而測定![]() 產品的純度,其它操作都正確,則測定的
產品的純度,其它操作都正確,則測定的![]() 產品的純度____________(填“偏高”、“偏低”或“無影響”)。
產品的純度____________(填“偏高”、“偏低”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溴丙胺太林片是一種用于治療胃腸痙攣性疼痛的藥物,其合成路線如下:

回答下列問題:
(1)A→B的反應類型___________反應;F→G的反應類型________反應。
(2)C含有的官能團名稱______________________________________。
(3)C→D的化學反應方程式___________________________________。
(4)E→F的化學反應方程式_____________________________________。
(5)I的結構簡式是_____________________________________________。
(6)假設有機物J苯環上的氫化學環境相同,則J核磁共振氫譜有______組峰。
(7)寫出1種與NaOH物質的量比1:3發生反應的E的同分異構體的結構簡式____________。
(8)將下列合成路線補充完整

該路線中化合物X為______________;化合物Y為:___________________;試劑與條件a為:__________________、__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用惰性電極電解足量下列溶液一段時間后,再加入一定量括號內的純凈物,能使溶液恢復到原來的成分和濃度的是
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
【答案】D
【解析】石墨電極為惰性電極,溶液中陽離子在陰極放電,陰離子在陽極放電。A、電解AgNO3溶液,Ag+在陰極放電生成Ag,OH-在陽極放電生成O2,且n(Ag)∶n(O2)=2∶1,則應加入Ag2O恢復濃度,故A錯誤;B、電解NaOH溶液,H+在陰極放電生成H2,OH-在陽極放電生成O2,且n(H2)∶n(O2)=2∶1,則應加入一定量的H2O恢復原樣,故B錯誤;C、電解KCl溶液,H+在陰極放電生成H2,Cl-在陽極放電生成Cl2,且n(H2)∶n(Cl2)=1∶1,則應加入一定量HCl恢復原樣,故C錯誤;D、電解CuSO4溶液,Cu2+在陰極放電生成Cu,OH-在陽極放電生成O2,且n(Cu)∶n(O2)=2∶1,則應加入一定量CuO恢復原樣,故D正確。故選D。
點睛:分析電解反應的原理,在兩極析出什么物質(固體或氣體),相當于什么物質脫離反應體系,根據元素守恒和原子比例,加入對應的物質,即可使溶液完全復原。
【題型】單選題
【結束】
28
【題目】工業上用電解法處理含鎳酸性廢水并得到單質Ni的原理如圖所示。下列說法不正確的是

已知:①Ni2+在弱酸性溶液中發生水解
②氧化性:Ni2+(高濃度)>H+>Ni2+(低濃度)
A. 碳棒上發生的電極反應:4OH--4e-=O2↑+2H2O
B. 電解過程中,B中NaCl溶液的物質的量濃度將不斷減少
C. 為了提高Ni的產率,電解過程中需要控制廢水pH
D. 若將圖中陽離子膜去掉,將A、B兩室合并,則電解反應總方程式發生改變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,a、b、c、d、e 為元素周期表中前 4 周期的一部分元素,下列有關敘述正確的是( )

A.元素 b 位于第ⅥA 族,有+6、-2 價兩種常見化合價
B.五種元素中,元素 e 的性質最穩定
C.元素 c 和 d 的最高價氧化物對應的水化物的酸性:c>d
D.元素 c 和 e 的氣態氫化物的穩定性:c>e
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是電解CuCl2溶液的裝置,其中c、d為石墨電極,則下列有關判斷正確的是( )
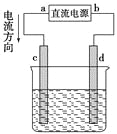
A. a為負極,b為正極
B. a為陽極,b為陰極
C. 電解過程中,d電極質量增加
D. 電解過程中,氯離子濃度不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面是某同學的化學筆記,需要改正的是
A.實驗后剩余的鈉粒,不能放回原試劑瓶中
B.在自然界中,鈉元素和氯元素只以化合態存在
C.Na2O2可作為呼吸面具里氧氣的來源
D.鹽酸的工業制法:H2+Cl2![]() 2HCl
2HCl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(NH4)2Fe(SO4)26H2O(M=392g/mol)又稱摩爾鹽,簡稱FAS,它是淺藍色綠色晶體,可溶于水,難溶于水乙醇。某小組利用工業廢鐵屑進行下列實驗。請按要求回答下列問題:
Ⅰ. FAS的制取。流程如下:

(1)步驟①加熱的目的是_________________________。
(2)步驟②必須在剩余少量鐵屑時進行過濾,其原因是(用離子方程式表示): ______________。
Ⅱ.NH4+含量的測定。裝置如圖所示:

實驗步驟:①稱取FAS樣品a g,加水溶解后,將溶液注入Y中
②量取b mL c1 mol/LH2SO4溶液于Z中
③向Y加入足量NaOH濃溶液,充分反應后通入氣體N2,加熱(假設氨完全蒸出),蒸氨結束后取下Z。
④用c2mol/LNaOH標準溶液滴定Z中過量的硫酸,滴定終點時消耗d mLNaOH標準溶液。
(3)儀器X的名稱______________;N2的電子式為______________。
(4)步驟③蒸氨結束后,為了減少實驗誤差,還需要對直形冷凝管進行處理的操作是__________________;NH4+質量百分含量為(用代數式表示)__________________。
Ⅲ. FAS純度的測定。稱取FAS m g樣品配制成500 mL待測溶液。分別取20.00mL待測溶液,進行如下方案實驗:
(5)方案一:用0.01000mol/L的酸性KMnO4溶液進行滴定。滴定過程中需用到的儀器中(填圖中序號)_________。滴定中反應的離子方程式為____________________。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
① ② ③ ④ ⑤ ⑥ ⑦ ⑧
(6)方案二: 待測液 ![]() 固體n g ;則FAS的質量百分含量為(用代數式表示)_____________________________。
固體n g ;則FAS的質量百分含量為(用代數式表示)_____________________________。
(7)方案一、二實驗操作均正確,卻發現方案一測定結果總是小于方案二的,其可能的原因是_______________;為驗證該猜測正確,設計后續實驗操作為_________________,現象為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某校化學實驗興趣小組探究實驗室中制備 Cl2 的過程,為證明過程中有水蒸氣和 HCl 揮發出來,同時證明Cl2的某些性質,甲同學設計了如下圖所示的實驗裝置,按要求回答問題。

(1)用濃鹽酸與足量的 MnO2 反應制Cl2 的化學反應方程式_____。
(2)①裝置 B 中盛放的試劑名稱為_____,作用是_____,現象是_____。
②裝置 D 和E 中出現的不同現象說明的問題是_________。
③裝置 F 的作用是_____。
④寫出裝置G 中發生反應的離子方程式_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com