
含有Na2O雜質的Na2O2試樣.請從如圖中選用適當的實驗裝置,設計一個最簡單的實驗,測定Na2O2試樣的純度(可供選用的反應物只有CaCO3固體,稀鹽酸和蒸餾水).
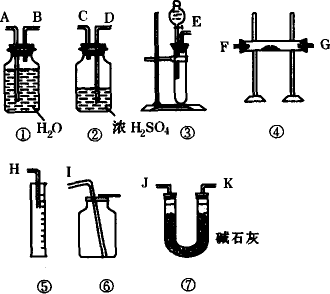
請填寫下列空白:
(1)寫出實驗中Na2O2和Na2O分別發生反應的化學方程式:________.
(2)應選用的裝置是(只要求寫出圖中裝置的標號)________.
(3)所選用裝置的連接順序應是________(填各接口的字母,連接膠管省略).
|
(1)2Na2O2+2H2O (2)③②①⑤ (3)E、D、C、B、A、H |
|
思路點撥:根據不同的反應原理,會有不同實驗設計思路,結合本題各裝置的特點,可設計出兩種實驗方案.一種是:制取CO2→干燥CO2→通入樣品反應→吸收未反應的CO2→排水法測O2的體積,選用裝置依次是③②④⑦①⑤.另一種是:用水直接滴入樣品中,考慮到該反應是一個放熱反應,將帶出較多量水蒸氣,故應先干燥,后用排水法測量O2的體積,選用裝置依次是③②①⑤.題目的要求是“設計一個最簡單的實驗”,故應選擇后一種方案. 小結點評:該題構思非常巧妙,不僅要求掌握不同的反應原理和設計出多種實驗途徑,而且要求學生能對自己設計的方案作出評價,從中優選出最佳方案.解題時還需知道各套儀器的用途,這樣才能將理論與實際聯系起來,才能活學活用所學知識. |


科目:高中化學 來源: 題型:閱讀理解
為了測定某種含有Na2O雜質的Na2O2試樣的純度,3個課外活動小組分別設計了如下三個實驗方案。首先準確稱量出要進行反應的樣品的質量m g,然后,將按照以下方案進行實驗:
方案一:將樣品與水充分反應,使產生的氣體與加熱的銅粉充分反應,測定反應后生成的氧化銅的質量為n g,通過計算求出試樣中的含量。
(1)按照此方案,則試樣中Na2O2的含量為 (用含 m、n的式子表示)
a(Na2O2)% ==
(2)此方案測定的結果誤差較大,主要原因是:
方案二:將樣品與實驗生成的二氧化碳反應,通過測定反應產生的氣體的體積,計算求出試樣中Na2O2的含量。
(1)按照此方案,以下制取二氧化碳和進行反應使用的儀器的連接次序是
(填寫儀器的編號)
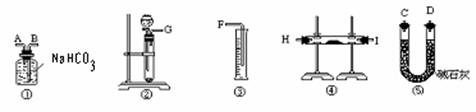
(2)通過①儀器的氣體從流向上看,次序為 進 出(填寫導管的字母)
方案三:將樣品與水充分反應,測定出反應后的溶液的準確體積VL,因為體積較大,再從反應后的溶液中,取一定的準確的體積為V1ml溶液,裝入錐形瓶中,用標準濃度的鹽酸進行滴定,測定出樣品與水反應后所得到的溶液的濃度,再計算求出試樣中Na2O2的含量。
(1) 按照此方案,進行酸堿中和滴定時,最后一步操作應該選擇的下列儀器中的
(填寫儀器的編號)


(2)選擇甲基橙做指示劑,確定終點的現象應該是溶液顏色由 變 并且半分鐘內不變你認為方案二、方案三中測定結果最準的是
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com