
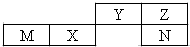
 五種短周期元素在元素周期表中的位置如圖,其中只有一種為金屬元素.下列說法正確的是( )
五種短周期元素在元素周期表中的位置如圖,其中只有一種為金屬元素.下列說法正確的是( )| A. | 簡單離子半徑大小:M>N>Z | |
| B. | 最簡單氣態氫化物的沸點高低:N>Z>Y | |
| C. | M的最高價氧化物可與N的最高價氧化物對應水化物反應 | |
| D. | N單質可與Z的最簡單氫化物反應置換出Z單質 |
分析 五種短周期元素在元素周期表中的位置如圖,其中只有一種為金屬元素,只能M為金屬,則M為Al,結合位置關系,可知X為Si,Y為N,Z為O,N為S.
A.電子層結構相同的離子,核電荷數越大離子半徑越小,電子層越多離子半徑越大;
B.水為液體,氨氣、硫化氫為氣體,故水的沸點最高,氨氣分子之間形成氫鍵,沸點高于硫化氫;
C.氧化鋁與硫酸反應生成硫酸鋁與水;
D.氧氣的氧化性比較硫的強.
解答 解:五種短周期元素在元素周期表中的位置如圖,其中只有一種為金屬元素,只能M為金屬,則M為Al,結合位置關系,可知X為Si,Y為N,Z為O,N為S.
A.電子層結構相同的離子,核電荷數越大離子半徑越小,電子層越多離子半徑越大,故離子半徑:S2->O2->Al3+,故A錯誤;
B.水為液體,氨氣、硫化氫為氣體,故水的沸點最高,氨氣分子之間形成氫鍵,沸點高于硫化氫,故B錯誤;
C.氧化鋁與硫酸反應生成硫酸鋁與水,故C正確;
D.氧氣的氧化性比較硫的強,氧氣可以與硫化氫反應得到硫單質,故D錯誤,
故選:C.
點評 本題考查結構性質位置關系應用,需要學生熟練掌握元素周期表結構,注意氫鍵對物質性質的影響,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 已知常溫下0.1 mol.L -1NaCN溶液的pH=12,則已水解的CN -約占總數的10% | |
| B. | 已知25℃時NH4CN溶液顯堿性,則25℃時的電離常數K(NH 3.H 2O)>K(HCN) | |
| C. | NH4ClO4溶液中,c(ClO4-)>c (NH4+)>c(OH -)>?c(H +)? | |
| D. | 欲使0.1 mol•L-1Na2S溶液中$\frac{c(Na)^{+}}{c({S}^{2-})}$更接近2,可加入適量KOH |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
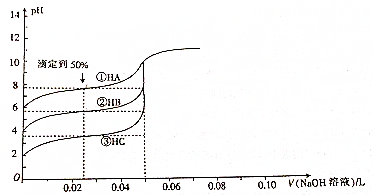
| A. | Ka(HA)>Ka(HB)>Ka(HC) | |
| B. | 滴定到50%時,溶液中:c(A-)>(B-)>(C-) | |
| C. | V(NaOH)溶液=50mL時,溶液中水的電離程度:①>②>③ | |
| D. | V(NaOH)溶液=50mL時,溶液pH的大小關系:pH(A)<pH(B)<pH(C) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
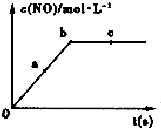 氮元素的單質及其化合物的研究和應用在工農業生產中有著非常重要的地位、工業制硝酸的主要反應之一是:
氮元素的單質及其化合物的研究和應用在工農業生產中有著非常重要的地位、工業制硝酸的主要反應之一是:| 深度/mol•L-1 時間/min | C(NH3) | c(O2) | c(NO) | c(H2O) |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | 4.5 | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
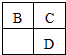
| A. | 簡單離子的半徑大小關系:B>C>E | |
| B. | D、E兩種元素形成的化合物,可能含有離子鍵和共價鍵 | |
| C. | B、D分別和C形成的化合物,都有可能使溴水或品紅溶液褪色 | |
| D. | A、B、C三種元素形成的化合物,晶體類型一定相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 元素 | Mn | Fe | |
| 電離能/mol | I1 | 717 | 758 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com