
 已知:CH3CH2OH+NaBr+H2SO4(濃) $\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.
已知:CH3CH2OH+NaBr+H2SO4(濃) $\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.分析 本題利用醇能與HX酸反應的原理制備溴乙烷,涉及溴的物理性質是紅棕色液體,易揮發,可通過水溶加熱的方法控制反應溫度,反應后的混合物因有機物與無機溶液不相溶而分層,下層為密度大于水的溴乙烷,通過分液分離后再進一步進行分離提純;
(1)濃硫酸具有強氧化性,溫度過高會把溴離子氧化成紅棕色的溴;
(2)溴乙烷沸點為38.4℃,同時考慮到濃硫酸的強氧化性,為避免更多的副反應進行,只要控制溫度略高于38.4℃即行,因此可以通過水浴進行加熱就可以了;
(3)溴乙烷密度比水的密度大,分層后處于混合液的下層;分液后,溴乙烷中混有溴,除雜時注意溴和溴乙烷的性質角度考慮;
(4)溴乙烷沸點低,可以采用蒸餾方法分離;
(5)檢驗溴乙烷中溴元素,應在堿性條件下水解,最后加入硝酸酸化,加入硝酸銀,觀察是否有黃色沉淀生成;有溴乙烷參加的主要反應是溴乙烷和堿溶液中的水解
解答 解:(1)由于濃硫酸具有強氧化性,能氧化Br-,會有溴生成,化學式為Br2,故答案為:Br2;
(2)可以利用水浴加熱來控制反應溫度,故答案為:水浴加熱;
(3)由于溴乙烷密度大于水的密度,故溴乙烷應該在下層;粗制的C2H5Br呈棕黃色,說明含有單質溴雜質,則
A.Na2SO3與溴發生氧化還原反應,Na2SO3可除去溴,故A正確;
B.溴在溴乙烷中的溶解度比在水中大,加水難以除去溴乙烷中的溴,故B錯誤;
C.氫氧化鈉溶液顯示堿性,可以除去雜質溴,但溴乙烷也會在此溶液里發生水解反應,故C錯誤;
D.溴和溴乙烷都能溶于四氯化碳,不能將二者分離,故D錯誤;
故答案為:下層;A;
(4)溴乙烷的沸點是38.4℃,故采用蒸餾操作分離,故答案為:蒸餾;
(5)檢驗溴乙烷中溴元素,應在堿性條件下水解,最后加入硝酸酸化,加入硝酸銀,觀察是否有黃色沉淀生成,所以操作順序為④①⑤③②,
故答案為:④①⑤③②.
點評 本題主要考查了溴乙烷的制備,掌握相關物質的基本化學性質,是解答本題的關鍵,平時須注意積累相關反應知識,本題難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 6:5:6 | B. | 1:3:5 | C. | 15:5:3 | D. | 1:6:10 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②④ | B. | ①③⑤ | C. | ①②⑤ | D. | ①④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯化鋁溶液和硫化鈉溶液反應制備Al2S3 | |
| B. | 用鎂粉和空氣反應制備Mg3N2 | |
| C. | 用鋁粉和MnO2制得錳 | |
| D. | 電解熔融氯化鋁的方法制得單質鋁 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 序號 | 實驗方案 | 實驗現象 | 結論 |
| ① | 將白色固體B加入水中, 加熱溶解,冷卻結晶、過濾 | 得到白色晶體和無色溶液 | 無 |
| ② | 取少量濾液于試管中, 滴入稀HNO3和AgNO3溶液 | 生成白色沉淀 | 濾液含Cl- |
| ③ | 干燥白色晶體,測定熔點 | 白色晶體在122.4℃左右完全熔化 | 白色晶體是苯甲酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 時間min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| n(SO2) | 2.00 | 1.92 | 1.84 | 1.76 | 1.76 | 1.64 | 1.52 | 1.40 | 1.40 | 1.40 |
| n(O2) | 1.00 | 0.96 | 0.92 | 0.88 | 0.88 | 0.82 | 0.76 | 0.70 | 0.70 | 0.70 |
| n(SO3) | 0 | 0.08 | 0.16 | 0.24 | 0.24 | 0.36 | 0.48 | 0.60 | 0.60 | 0.60 |
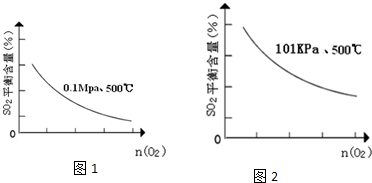
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
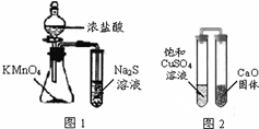
| A. | 下列有關實驗原理、操作或現象不正確的是圖1錐形瓶中滴入濃鹽酸后充滿黃綠色氣體,試管中出現淺黃色渾濁 | |
| B. | 圖2放置一段時間后,飽和CuSO4溶液中出現白色晶體 | |
| C. | 用玻璃棒蘸取某溶液做焰色反應實驗,火焰呈黃色說明該溶液中不含鉀元素 | |
| D. | 蒸餾時,將溫度計水銀球靠近蒸餾燒瓶支管口處 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com