
| A. | Na2CO3→NaOH | B. | BaCl2→Ba(OH)2 | C. | FeCl3→Fe(OH)3 | D. | CaCO3→CaCl2 |
分析 A.碳酸鈉與氫氧化鈣反應生成碳酸鈣和NaOH;
B.氯化鋇不能一步轉化為氫氧化鋇;
C.氯化鐵與堿反應生成氫氧化鐵;
D.碳酸鈣與鹽酸反應生成氯化鈣.
解答 解:A.Na2CO3$\stackrel{Ca(OH)_{2}}{→}$NaOH可一步轉化,故A不選;
B.BaCl2→Ba(OH)2不能一步轉化實現(xiàn),故B選;
C.FeCl3$\stackrel{NaOH/氨水等}{→}$Fe(OH)3可一步轉化,故C不選;
D.CaCO3$\stackrel{HCl}{→}$CaCl2可一步轉化,故D不選;
故選B.
點評 本題考查物質的性質及相互轉化,為高頻考點,把握物質的性質、發(fā)生的反應為解答的關鍵,側重分析與應用能力的考查,注意元素化合物知識的綜合應用,題目難度不大.


科目:高中化學 來源: 題型:選擇題
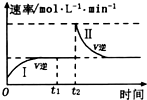 在某一恒溫體積可變的密閉容器中發(fā)生如下反應:A(g)+B(g)?2C(g)△H<0; t1時刻達到平衡后,在t2時刻改變某一條件,其反應過程(I、Ⅱ)如圖所示.下列說法中,一定不正確的是( )
在某一恒溫體積可變的密閉容器中發(fā)生如下反應:A(g)+B(g)?2C(g)△H<0; t1時刻達到平衡后,在t2時刻改變某一條件,其反應過程(I、Ⅱ)如圖所示.下列說法中,一定不正確的是( )| A. | 0~t1時,V正>V逆 | |
| B. | I、Ⅱ兩過程分別達到平衡時,A的體積分數(shù)Ⅰ>Ⅱ | |
| C. | t2時刻改變的條件可能是向密閉容器中加C物質 | |
| D. | Ⅰ、Ⅱ兩過程達到平衡時,平衡常數(shù)Ⅰ=Ⅱ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硫酸與氫氧化鋇在溶液中反應:Ba2++SO42-═BaSO4↓ | |
| B. | 少量金屬鈉投入到CuSO4溶液中:2Na+Cu2+═2Na++Cu↓ | |
| C. | BaCO3與鹽酸反應:CO32-+2H+═H2O+CO2↑ | |
| D. | 用Cl2將苦鹵中的Br-氧化:Cl2+2Br-═2Cl-+Br2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | N2是還原產物,且還原劑與氧化劑物質的量之比是2:3 | |
| B. | N2是氧化產物,且還原劑與氧化劑物質的量之比是2:3 | |
| C. | 每轉移6mol電子就生成22.4LN2 | |
| D. | NH4Cl是氧化產物,且還原劑與氧化劑物質的量之比是2:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 弱電解質在溶液中部分電離,存在電離平衡 | |
| B. | 同一弱電解質的溶液,當溫度或濃度不同時,其導電能力也不相同 | |
| C. | 電離常數(shù)(K)越小,表示弱電解質電離能力越弱 | |
| D. | 不同濃度的同一弱電解質,其電離常數(shù)(K)不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A原子:1s22s22p63s23p63d10 | B. | B2-:1s22s22p6 | ||
| C. | C2+:1s22s22p6 | D. | D原子:1s22s22p6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
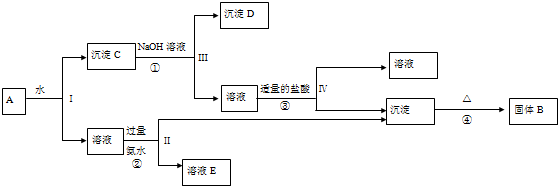
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 一定溫度下,在一固定體積的容器中,通入一定量的CO和H2O,
一定溫度下,在一固定體積的容器中,通入一定量的CO和H2O,| 時間(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
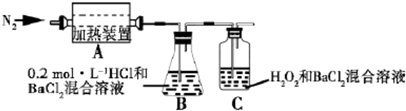
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com