
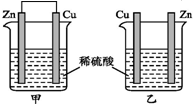
| A. | 兩燒杯中銅片表面均無氣泡產生 | B. | 甲中銅片是正極,乙中銅片是負極 | ||
| C. | 兩燒杯中溶液的酸性均減弱 | D. | 產生氣泡的速率甲比乙慢 |
分析 由圖可知,甲構成原電池,鋅作負極,失電子,銅作正極,H+在銅極上得電子生成H2,電池總反應式為:Zn+H2SO4=ZnSO4+H2↑.乙裝置中只是鋅片與稀硫酸間發生了置換反應:Zn+H2SO4=ZnSO4+H2↑,以此進行分析.
解答 解:A.甲是原電池,正極銅片上發生還原反應 2H++2e-=H2↑,乙裝置中在鋅片上發生反應 Zn+2H+=Zn2++H2↑,銅片上無氣體產生,故A錯誤;
B.甲裝置是原電池,銅片做正極,乙不是原電池,故B錯誤;
C.兩燒杯中的氫離子均發生反應,溶液中氫離子濃度減少,溶液的酸性均減弱,故C正確;
D.甲中構成原電池,加快反應速率,所以產生氣泡的速度甲比乙快,故D錯誤;
故選:C.
點評 本題考查原電池的有關知識,難度不大,注意把握原電池的構成條件及工作原理,有利于基礎知識的鞏固.


 口算能手系列答案
口算能手系列答案科目:高中化學 來源: 題型:多選題
| A. | 該溶液中氫離子的濃度:c(H+)=1×10-11 mol•L-1 | |
| B. | pH=7 的NH4Cl和NH3•H2O的混合溶液:c(Cl-)>c(NH4+)>c(H+)=c(OH-) | |
| C. | 濃度均為0.1 mol•L-1的NH3•H2O和NH4Cl溶液等體積混合后的堿性溶液中:c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-)>c(H+) | |
| D. | 0.1 mol•L-1的氨水與0.05 mol•L-1的 H2SO4溶液等體積混合后所得溶液中:2c(NH4+)+2c(NH3•H2O)=c(SO42-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇與濃氫溴酸反應:CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O | |
| B. | 溴乙烷與氫氧化鈉溶液共熱:CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr | |
| C. | 苯酚鈉中通入二氧化碳:2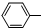 ONa+CO2+H2O→2 ONa+CO2+H2O→2 OH+Na2CO3 OH+Na2CO3 | |
| D. | 淀粉在稀硫酸作用下水解:(C6H10O5)n(淀粉)+nH2O$→_{△}^{稀硫酸}$nC6H12O6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
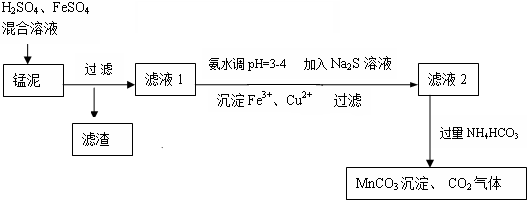
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定有乙烯 | B. | 可能有乙烯 | C. | 一定沒有甲烷 | D. | 可能有乙烷 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 質子數是94 | B. | 原子序數是239 | C. | 質量數是94 | D. | 中子數是239 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 8n | B. | 18n | C. | 14n | D. | 44n |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 與金屬鈉反應時,只有鍵①斷裂 | B. | 在Ag催化下與O2反應時,鍵①、③斷裂 | ||
| C. | 與CuO反應時,只有鍵①斷裂 | D. | 與濃硫酸共熱至170℃時,鍵②、⑤斷裂 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com