
【題目】下圖為元素周期表的一部分:

(1)元素③的基態原子軌道表示式為_________________。
(2)元素⑩原子的外圍電子排布式為__________。
(3)元素③④⑤的第一電離能由大到小的順序為___________(填元素符號),其簡單離子半徑由大到小的順序為______________(填離子符號)。
(4)⑤與⑧氣態氫化物中沸點較高的是_______(填化學式),原因是______________。
(5)以下組合的原子間反應最容易形成離子鍵的是_____(選填A、B、C、D,下同),最容易形成共價鍵的是_____,用電子式表示該共價化合物的形成過程______________。
A.和⑤ B.和⑤
C.⑤和⑥ D.⑥和⑧
(6)某些不同族元素的性質也有一定的相似性,如上表中元素⑦與元素②的單質及其化合物有相似的性質.寫出元素②的最高價氧化物與NaOH溶液反應的離子方程式_________________________________________________。
(7)根據下列五種元素的第一至第四電離能數據(單位:KJ·mol﹣1),回答下面各題:
元素代號 | I1 | I2 | I3 | I4 |
Q | 2080 | 4000 | 6100 | 9400 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能處于同一主族的是_________(填元素代號)。
②若T為第三周期元素,則T屬于________(填“s”、“p”、“d”、“ds”)區元素,Z是第三周期元素中原子半徑最小的主族元素,則T、Z形成的化合物屬于__(填“共價”或“離子”)化合物。
【答案】 ![]() 3d64s2 F>N>O N3﹣>O2﹣>F- HF HF能形成分子間氫鍵 C B
3d64s2 F>N>O N3﹣>O2﹣>F- HF HF能形成分子間氫鍵 C B ![]() 2OH﹣+BeO=BeO22﹣+H2O R 和U p 共價
2OH﹣+BeO=BeO22﹣+H2O R 和U p 共價
【解析】(1). ③為N元素,N是7號元素,基態原子電子排布式為:1s22s22p3,則基態原子軌道表示式為:![]() ,故答案為:
,故答案為:![]() ;
;
(2). ⑩為Fe元素,Fe是26號元素,原子的外圍電子排布式為:3d64s2,故答案為:3d64s2;
(3). 元素③④⑤分別為N、O、F,同一周期從左至右,第一電離能呈增大趨勢,則三種元素中F元素的第一電離能最大,N元素的基態原子電子排布式為:1s22s22p3,是一種半充滿的穩定結構,第一電離能N>O,所以N、O、F三種元素的第一電離能由大到小的順序為F>N>O,N、O、F三種元素的簡單離子具有相同的電子層結構,原子序數越大,離子半徑越小,所以N、O、F三種元素的簡單離子半徑由大到小的順序為:N3﹣>O2﹣>F﹣,故答案為:F>N>O;N3﹣>O2﹣>F﹣;
(4). 因HF分子之間存在氫鍵,所以HF的沸點高于HCl,故答案為:HF;HF能形成分子間氫鍵;
(5). 由各物質在周期表中的位置可知,①為H、②為Be、⑤為F、⑥為Na、⑧為Cl,五種元素中最活潑的金屬鈉和最活潑的非金屬氟之間最容易形成離子鍵,故為C項;非金屬元素之間最容易形成共價鍵,故為B項,該化合物為HF,H和F原子之間形成一個共用電子對,用電子式表示HF形成過程的式子為:![]() ,故答案為:C;B;
,故答案為:C;B;![]() ;
;
(6). Be和Al元素的單質及其化合物具有相似的性質,則BeO也具有兩性,BeO與NaOH溶液反應生成Na2BeO2和水,該反應的離子方程式為:2OH﹣+BeO=BeO22﹣+H2O,故答案為:2OH﹣+BeO=BeO22﹣+H2O;
(7).由元素的電離能可以看出,Q的電離能很大,可能為零族元素,R和U的第一電離能較小,第二電離能劇增,故表現+1價,最外層電子數為1,二者位于同一主族,E的第一、第二電離能較小,第三電離能劇增,故表現+2價,最外層電子數為2,T的第一、第二、第三電離能較小,第四電離能劇增,表現+3價,最外層電子數為3。
①. R和U的第一至第四電離能變化規律相似,即R和U最可能在同一主族,故答案為:R和U;
②. 由上述分析可知,T的第一、第二、第三電離能較小,第四電離能劇增,表現+3價,最外層電子數為3,若T為第三周期元素,則T為Al元素,Al元素基態原子的核外電子排布式為:1s22s22p63s23p1,屬于p區元素,Z是第三周期元素中原子半徑最小的主族元素,則Z是Cl元素,Al和Cl元素之間電負性相差較小,以共價鍵相結合形成AlCl3,所以AlCl3是共價化合物,故答案為:p;共價。


 浙江之星課時優化作業系列答案
浙江之星課時優化作業系列答案 激活思維優加課堂系列答案
激活思維優加課堂系列答案科目:高中化學 來源: 題型:
【題目】某實驗科研小組研制了一種從廢舊的含鎳催化劑(主要成分為NiO,另含Fe2O3、CaO、CuO、BaO等)回收鎳的新工藝。工藝流程如下圖:
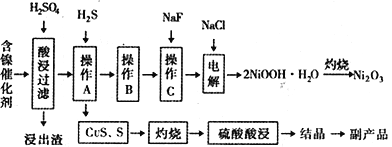
回答下列問題:
(1)浸出渣主要成分為CaSO4↓·2H2O和_______________兩種物質。
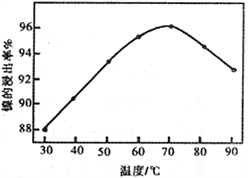
(2)右圖表示鎳的浸出率與溫度的關系,當浸出溫度高于70℃時,鎳的浸出率降低,浸出渣中Ni(OH)2含量增大,其原因是_____________________________。
(3)工藝流程中的“副產品”為________(填化學式)。
(4)已知有關氫氧化物開始沉淀和沉淀完全的pH 如下表:
氫氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
開始沉淀的pH | 1.5 | 6.5 | 7.7 |
沉淀完全的pH | 3.7 | 9.7 | 9.2 |
操作B是為了除去濾液中的鐵元素,某同學設計了如下實驗方案:向操作A所得的濾液中加入NaOH溶液,調節溶液pH為3.7~7.7,靜置,過濾。請對該實驗方案是否正確進行判斷并做出評價: ___________________________________(若原方案正確,請說明理由;若原方案錯誤,請加以改正)。
(5)操作C是為了除去溶液中的Ca2+,若控制溶液中F-濃度為3×10-3mol·L-1,則溶液中![]() =________________。(常溫時,Ksp(CaF2)=2.7×10-11)
=________________。(常溫時,Ksp(CaF2)=2.7×10-11)
(6)電解產生2NiOOH·H2O的原理分兩步:
①堿性條件下Cl-在陽極被氧化為ClO-;生產1mol ClO-,消耗OH-______________mol。
②Ni2+被ClO-氧化產生2NiOOH·H2O沉淀。則該步反應的離子方程式為_________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(一)2011年,內蒙古、新疆、浙江等地都要陸續召開各具特色的農博會,到時“生態農業”將成為農會人員關注的熱門話題。生態農業涉及農家肥料的綜合利用,某種肥料經發酵得到一種含甲烷、二氧化碳、氮氣的混合氣體。2.016 L(標準狀況)該氣體通過盛有紅熱CuO粉末的硬質玻璃管,發生的反應為:CH4+4CuO![]() CO2+2H2O+4Cu。當甲烷完全反應后,硬質玻璃管的質量減輕4.8 g。將反應后產生的氣體通入過量的澄清石灰水中,充分吸收,生成沉淀8.5 g。
CO2+2H2O+4Cu。當甲烷完全反應后,硬質玻璃管的質量減輕4.8 g。將反應后產生的氣體通入過量的澄清石灰水中,充分吸收,生成沉淀8.5 g。
(1)原混合氣體中甲烷的物質的量是________。
(2)原混合氣體中氮氣的體積分數為________。
(二)FeS與一定濃度的HNO3反應,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,當NO2、N2O4、、NO的物質的量之比為1﹕1﹕1時,實際參加反應的FeS與HNO3的物質的量之比為___________________
(三)某反應中反應物與生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一種未知物質X。
已知0.2 mol KBrO3在反應中得到1 mol電子生成X,請將氧化劑和還原劑的化學式及其配平后的系數填入下列方框中,并標出電子轉移的方向和數目。_________________
![]() +
+![]()
(四) 在一定條件下,分別以高錳酸鉀、氯酸鉀、過氧化氫(H2O2)、過氧化鈉為原料制取氧氣,當制得同溫、同壓下相同體積的O2時,四個反應中轉移的電子數之比為_____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是中學化學中常用于混合物的分離和提純的裝置,請根據裝置回答問題:

(1)從氯化鈉溶液中得到氯化鈉固體,選擇裝置____(填代表裝置圖的字母,下同);除去自來水中的Cl﹣等雜質,選擇裝置____;從碘水中提取I2,選擇裝置____,該分離方法的名稱為________。
(2)裝置A中①的名稱是____________,冷卻水的方向是______________,溫度計水銀球的位置是在_____________;裝置B在分液時裝置中的液體不能順利滴下,原因是___________________________。
(3)從碘水中提取碘時,不能選用的試劑是______。
A.酒精 B.苯 C.四氯化碳
若選擇試劑X(密度小于水的密度)從碘水中提取碘時,充分振蕩、靜置后,下層液體的顏色為__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有七種元素,其中A、B、C、D、E為短周期主族元素,F、G為第四周期元素,它們的原子序數依次增大。請根據下列相關信息,回答問題。
A元素的核外電子數和電子層數相等,也是宇宙中最豐富的元素 |
B元素原子的核外p電子數比s電子數少1 |
C原子的第一至第四電離能分別是 I1=738 kJ/mol;I2=1 451 kJ/mol;I3=7 733 kJ/mol;I4=10 540 kJ/mol |
D原子核外所有p軌道全滿或半滿 |
E元素的主族序數與周期數的差為4 |
F是前四周期中電負性最小的元素 |
G在周期表的第七列 |
(1)已知BA5為離子化合物,寫出其電子式______________________________。
(2)B基態原子中能量最高的電子,其電子云在空間有________個方向,原子軌道呈________形。
(3)某同學根據上述信息,推斷C基態原子的核外電子排布為![]() 該同學所畫的電子排布圖違背了_____________________________________。
該同學所畫的電子排布圖違背了_____________________________________。
(4)G位于________族________區,價電子排布式為________。
(5)檢驗F元素的方法是________,請用原子結構的知識解釋產生此現象的原因是_____________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某淡黃色粉末可在潛水艇中作為氧氣的來源,常被用作供氧劑。根據下圖所示轉化關系及現象填空:
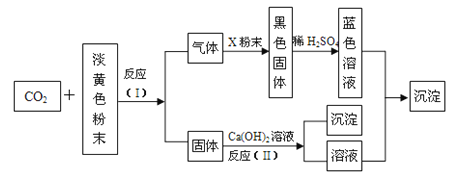
(1)該淡黃色粉末為__________________;
(2)X粉末的名稱或化學式為__________________;
(3)反應(I)的化學方程式為______________________________;
(4)反應(II)的化學方程式為_____________________________;
(5)反應(Ⅲ)的化學方程式為______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家剛剛發現了某種元素的原子,1個該原子質量是a g,一個12C原子質量是b g,NA是阿伏加德羅常數的值,下列說法正確的是
①該原子的相對原子質量為12a/b ②m g該原子的物質的量為 m/aNAmol
③該原子的摩爾質量是aNA g ④Wg該原子中含有W/a個該原子
⑤由已知信息可得:NA=12/a
A. ①②④ B. ①③ C. ②③ D. ③⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知某純堿(Na2CO3)試樣中含有NaCl雜質,為測定試樣中純堿的質量分數,可用下圖中的裝置進行實驗。
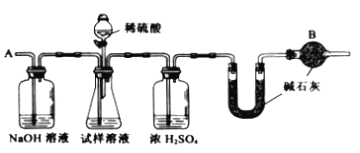
主要實驗步驟如下:
①按圖組裝儀器,并檢查裝置的氣密性;
②將a g試樣放入錐形瓶中,加適量蒸餾水溶解,得到試樣溶液;
③稱量盛有堿石灰(CaO與NaOH固體混合物)的U型管的質量,稱得為b g;
④從分液漏斗滴入6 mol·L-1 的硫酸,直到不再產生氣體時為止;
⑤從導管A處緩緩鼓入一定量的空氣;
⑥再次稱量盛有堿石灰的U型管的質量;
⑦重復步驟⑤和⑥的操作,直到U型管的質量基本不變,最終稱得為c g;
請填空和回答問題:
(1)裝置中干燥管B的作用是__________________________________________
(2)步驟⑤的目的是__________________________________________________
(3)步驟⑦的目的是__________________________________________________
(4)該試樣中純堿的質量分數的計算式為___________________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com