
分析 (1)0.01mol/L的NaOH溶液的pH為11,則c(H+)=1×10-11mol/L,c(OH-)=0.01mol/L,根據Kw=c(H+)×c(OH-)計算;
(2)混合溶液呈中性,且硫酸和氫氧化鈉都是強電解質,所以酸中氫離子物質的量和堿中氫氧根離子的物質的量相等.
解答 解:(1)0.01mol/L的NaOH溶液的pH為11,則c(H+)=1×10-11mol/L,c(OH-)=0.01mol/L,Kw=c(H+)×c(OH-)=1×10-13,
答:水的離子積常數KW是1×10-13;
(2)①混合溶液呈中性,且硫酸和氫氧化鈉都是強電解質,所以酸中氫離子物質的量和堿中氫氧根離子的物質的量相等,pH=a的NaOH溶液中氫氧根離子濃度=10 a-13 mol/L,pH=b的H2SO4溶液氫離子濃度=10-b mol/L,10 a-13 mol/L×VaL=10-b mol/L×VbL,且a=12,b=2,則Va:Vb=1:10,
答:Va:Vb為1:10;
②10 a-13 mol/L×VaL=10-b mol/L×VbL,且a+b=12,則Va:Vb=10:1,
答:Va:Vb為10:1.
點評 本題考查酸堿混合的計算,明確該溫度下的Kw及pH與濃度的換算是解答本題的關鍵,注意酸堿反應的實質即可解答,題目難度中等.


科目:高中化學 來源: 題型:解答題
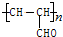 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
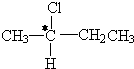 中帶*的C原子.若同一個碳原子上連著2個碳碳雙鍵(如C═C═C)時,分子極不穩定,不存在.某鏈烴C7H10的眾多同分異構體中:
中帶*的C原子.若同一個碳原子上連著2個碳碳雙鍵(如C═C═C)時,分子極不穩定,不存在.某鏈烴C7H10的眾多同分異構體中:
 、
、 .
.  .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 定容時仰視容量瓶的刻度線 | |
| B. | 在用蒸餾水洗滌燒杯時,洗滌液未全部轉移到容量瓶中 | |
| C. | 配制鹽酸溶液用量筒量取濃鹽酸時仰視刻度線 | |
| D. | 用來配制溶液的容量瓶用蒸餾水洗滌后未進行干燥處理 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 燃料電池總的離子反應方程式為:2Al+3HO2-═2AlO2-+2H2O | |
| B. | 電解時,Al消耗2.7g,則產生氮氣的體積為1.12L | |
| C. | 電極b是負極,且反應后該電極區pH增大 | |
| D. | 電解過程中,電子的流向由a→d,c→b. |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
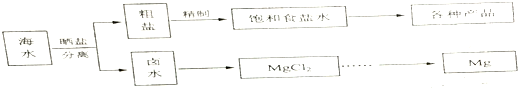
| 物質 | 開始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.6 |
| Mg(OH)2 | 9.8 | 11.1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 序號 | 物質(雜質) | 所用試劑 | 分離方法 |
| A | 溴苯(Br2) | 苯 | 萃取、分液 |
| B | 乙酸乙酯(乙酸) | 飽和碳酸鈉溶液 | 分液 |
| C | CH4(C2H4) | 酸性高錳酸鉀 | 洗氣 |
| D | 硝基苯(硝酸) | 氫氧化鈉溶液 | 過濾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com