
太陽能電池的發展已經進入了第三代。第一代為單晶硅太陽能電池,第二代為多晶硅、非晶硅等太陽能電池,第三代就是銅銦鎵硒CIGs(CIS中摻入Ga)等化合物薄膜太陽能電池以及薄膜Si系太陽能電池。
(1)亞銅離子(Cu+)基態時的價電子排布式表示為 。
(2)硒為第4周期元素,相鄰的元素有砷和溴,則3種元素的第一電離能從大到小順序為 (用元素符號表示)。
(3)Cu晶體的堆積方式是 (填堆積名稱),其配位數為 ;往Cu的硫酸鹽溶液中加入過量氨水,可生成[Cu(NH3)4]SO4,下列說法正確的是_____
A.[Cu (NH3)4]SO4中所含的化學鍵有離子鍵、極性鍵和配位鍵
B.在[Cu(NH3)4 ]2+中Cu2+給出孤對電子,NH3提供空軌道
C.[Cu (NH3)4]SO4組成元素中第一電離能最大的是氧元素
D.SO42-與PO43-互為等電子體,空間構型均為正四面體
(4)與鎵元素處于同一主族的硼元素具有缺電子性,其化合物往往具有加合性,因而硼酸(H3BO3)溶于水顯弱酸性,但它卻只是一元酸,可以用硼酸在水溶液中的電離平衡解釋它只是一元弱酸的原因。
①H3BO3中B的原子雜化類型為 ;
②寫出硼酸在水溶液中的電離方程式 。
(5)硅與碳是同一主族元素,其中石墨為混合型晶體,已知石墨的層 間距為335pm,C-C鍵長為142pm,計算石墨晶體密度(要求寫出計算過程,得出結果保留三位有效數字,NA為6.02×1023mol-1)

(1)3d10(1分)
(2)Br〉As〉Se(2分)
(3)12 (2分) 面心立方最密堆積 AD(2分)
(4)①sp2(2分)② (2分)
(2分)
(5)石墨的層間距為335pm,可以認為一層石墨的厚度是335pm。對某一層石墨中的一個六元環,正六邊形環的邊長是142pm,面積S=6×1/2×142×142sin(π/3)=52387.6pm2。環的厚度h=335pm那么一個環占有的體積V=Sh=52387.6×335=1.754×107pm3=1.754×10-23cm3。六元環中每個C原子都被3個環共用,一個環實際有2個C原子。一個環的質量m=2M/NA=2×12.01/(6.023×1023)=3.988×10-23g。
所以,石墨的密度ρ=m/V=3.988/1.754=2.27g/cm3。(4分)
【解析】
試題分析:(1)銅是29號元素,銅原子失去一個電子變成亞銅離子,所以亞銅離子核外有28個電子,根據構造原理寫出其核外電子排布式基態銅離子(Cu+)的價電子排布式為:3d10
(2)同一周期中元素的第一電離能隨著原子序數的增大而呈增大的趨勢,但第VA族元素最外層p軌道處于半充滿狀態較穩定,第一電離能大于其相鄰元素;As、Se、Br屬于同一周期且原子序數逐漸增大,這三種元素依次屬于第IVA族、第VA族、第VIA族,3種元素的第一電離能從大到小順序為Br>As>Se;
(3)金屬銅為面心立方堆積,配位數為12;在[Cu(NH3)4]SO4中含有離子鍵、極性鍵和配位鍵;配位鍵的形成:NH3給出孤對電子,Cu2+提供空軌道;同一周期中元素的第一電離能隨著原子序數的增大而呈增大的趨勢,但第VA族元素最外層p軌道處于半充滿狀態較穩定,第一電離能大于其相鄰元素;同一族中元素的第一電離能隨著原子序數的增大而呈減小的趨勢,所以第一電離能最大的為氮元素;選A、D;
(4)①H3BO3中B原子和三個羥基相連,具有具有平面三角的構形,B是sp2雜化;②H3BO3為缺電子化合物,溶于水后和水電離產生的OH-通過配位鍵結合形成[B(OH)4]-,故H3BO3的電離方程式為
考點:考查核外電子排布、第一電離能大小的比較、雜化方式的判斷、配位數的判斷、晶胞結構結合豐富想象力進行分析解答。.


科目:高中化學 來源: 題型:閱讀理解
 (2013?青島一模)[化學-物質結構與性質]
(2013?青島一模)[化學-物質結構與性質]查看答案和解析>>
科目:高中化學 來源: 題型:
 (2013?樂山三模)太陽能電池的發展已經進入了第三代.第一代為單晶硅太陽能電池,第二代為多晶硅、非晶硅等太陽能電池,第三代就是銅銦鎵硒CIGS(CIS中摻入Ga)等化合物薄膜太陽能電池以及薄膜Si系太陽能電池.
(2013?樂山三模)太陽能電池的發展已經進入了第三代.第一代為單晶硅太陽能電池,第二代為多晶硅、非晶硅等太陽能電池,第三代就是銅銦鎵硒CIGS(CIS中摻入Ga)等化合物薄膜太陽能電池以及薄膜Si系太陽能電池.

查看答案和解析>>
科目:高中化學 來源:2012-2013學年山東省青島市高三第一次模擬考試理綜化學試卷(解析版) 題型:填空題
太陽能電池的發展已經進入了第三代。第三代就是銅銦鎵硒CIGS等化合物薄膜太陽能電池以及薄膜Si系太陽能電池。完成下列填空:
(1)亞銅離子(Cu+)基態時的電子排布式為 ;
(2)硒為第4周期元素,相鄰的元素有砷和溴,則3種元素的第一電離能從大到小順序為 (用元素符號表示),用原子結構觀點加以解釋 ;
(3)與鎵元素處于同一主族的硼元素具有缺電子性(價電子數少于價層軌道數),其化合物可與具有孤對電子的分子或離子生成加合物,如BF3能與NH3反應生成BF3·NH3。 BF3·NH3中B原子的雜化軌道類型為 ,B與N之間形成 鍵;
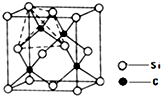
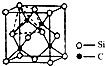
(4)單晶硅的結構與金剛石結構相似,若將金剛石晶體中一半的C原子換成Si原子且同種原子不成鍵,則得如圖所示的金剛砂(SiC)結構;在SiC中,每個C原子周圍最近的C原子數目為 。

查看答案和解析>>
科目:高中化學 來源:2012-2013學年江西省南昌市高三第三次模擬考試理綜化學試卷(解析版) 題型:填空題
太陽能電池的發展已經進入了第三代。第一代為單晶硅太陽能電池,第二代為多晶硅、非晶硅等太陽能電池,第三代就是銅銦鎵硒CIGS(CIS中摻人Ga)等化合物薄膜太陽能電池以及薄膜Si系太陽能電池。
(1)鎵的基態原子的電子排布式是___ 。
(2)硒為第4周期元素,相鄰的元素有砷和溴,則3種元素的第一電離能從大到小順序為 (用元素符號表示)。
(3)H2Se的酸性比H2S____(填“強”或“弱”)。氣態SeO3分子的立體構型為____ 。
(4)硅烷(SinH2n+2)的沸點與其相對分子質量的變化關系如圖所示,呈現這種變化關系的原因是 。

(5)與鎵元素處于同一主族的硼元素具有缺電子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能與水反應生成[B(OH)4]—而體現一元弱酸的性質,則[B(OH)4]—中B的原子雜化類型為 。
(6)金屬Cu單獨與氨水或單獨與過氧化氫都不能反應,但可與氨水和過氧化氫的混合溶液反應,其原因是____,反應的離子方程式為 。
(7)一種銅金合金晶體具有面心立方最密堆積的結構。在晶脆中,Au原子位于頂點,Cu原子位于面心,則該合金中Au原子與Cu原子個數之比為 ,若該晶胞的邊長為a pm,則合金的密度為 g·cm-3(已知lpm=10-12m,只要求列算式,不必計算出數值,阿伏加塞羅常數為NA)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com