
【題目】某學生用0.200 0 mol·L-1的標準NaOH溶液滴定未知濃度的鹽酸,其操作如下:
①用蒸餾水洗滌堿式滴定管,并立即注入NaOH溶液至“0”刻度線以上;
②固定好滴定管并使滴定管尖嘴處充滿液體;
③調節液面至“0”或“0”刻度線以下,并記下讀數;
④移取20.00 mL待測液注入潔凈的還存有少量蒸餾水的錐形瓶中,并加入3滴酚酞試液;
⑤用標準液滴定至終點,記下滴定管液面讀數。
請回答下列問題:
(1)以上步驟有錯誤的是____。
(2)用標準的NaOH溶液滴定待測的鹽酸時,左手握_______(填“酸式”或“堿式”)滴定管的活塞,右手搖動錐形瓶,眼睛注視_______________判斷滴定終點的現象是____________________。
(3)若測定結果偏高,其原因可能是_____。
a.配制標準溶液的固體NaOH中混有KOH雜質
b.滴定終點讀數時,仰視滴定管的刻度,其他操作正確
c.盛裝待測液的錐形瓶用蒸餾水洗過后未用待測液潤洗
d.滴定管滴定前無氣泡,滴定后有氣泡
(4)如圖是某次滴定時的滴定管中的液面,其讀數為_____mL。
![]()
(5)根據下列數據,請計算待測鹽酸的濃度:_________mol·L-1。
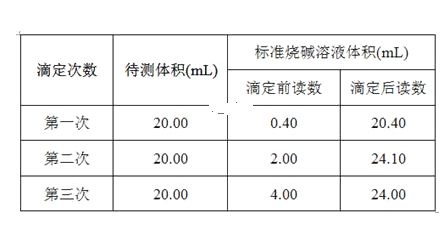
【答案】① 堿式 錐形瓶中的溶液顏色變化 滴入最后一滴NaOH溶液時,溶液剛好由無色變為淺紅色,且半分鐘內不褪色 ab 22.60 0.200 0
【解析】
(1)根據堿式滴定管在裝液前應用所裝液體進行潤洗;
(2)滴定時標準NaOH應裝在堿式滴定管中,眼睛注視錐形瓶內溶液顏色變化,滴定終點時溶液顏色由無色突變為紅色,且半分鐘內不褪色;
(3)根據![]() 分析不當操作對V(標準)×的影響,以此判斷濃度的誤差;
分析不當操作對V(標準)×的影響,以此判斷濃度的誤差;
(4)根據滴定管的結構小數在上、大數在下和精確度為0.01mL解答;
(5)分析表中數據有效性,依據![]() 計算待測液濃度。
計算待測液濃度。
(1)根據堿式滴定管在裝液前應用所裝液體進行潤洗,用蒸餾水洗滌堿式滴定管,并立即注入NaOH溶液至“0”刻度線以上是錯誤的,
故答案為:①
(2)滴定時標準NaOH應裝在堿式滴定管中,滴定時左手握滴定管,右手搖動錐形瓶,眼睛注視錐形瓶內溶液顏色變化,強堿滴定強酸時達到終點時無色變為淺紅色,且半分鐘內不褪色,
故答案為:堿式 ; 錐形瓶中的溶液顏色變化; 滴入最后一滴NaOH溶液時,溶液剛好由無色變為淺紅色,且半分鐘內不褪色;
(3)a.配制標準溶液的固體NaOH中混有KOH雜質,標準溶液中氫氧根離子的濃度偏小,消耗的V(標準)增大,測定結果偏高,故a正確;
b.滴定終點讀數時,仰視滴定管的刻度,讀取消耗的V(標準)偏大,測定結果偏高,故b正確;
c.盛裝待測液的錐形瓶用蒸餾水洗過后未用待測液潤洗,測定結果不受影響,故c錯誤;
d.滴定管滴定前無氣泡,滴定后有氣泡V(標準)偏小,測定結果偏低,故d錯誤
故答案選ab。
(4)依據滴定管構造及精確度可知圖中液面讀數為:22.60;
故答案為:22.60;
(5)三次消耗標準液體積分別為:20.00,22.10,20.00,第二組數據誤差較大,應舍棄,則消耗標準液平均體積為:20.00mL,待測液濃度為: 0.2000 mol·L-1×20.00ml÷20.00ml=0.200 0 mol·L-1,
故答案為:0.2000。


 勵耘書業暑假銜接寧波出版社系列答案
勵耘書業暑假銜接寧波出版社系列答案科目:高中化學 來源: 題型:
【題目】D是一種催眠藥,F是一種香料,它們的合成路線如下:

(1)A的化學名稱是___,C中含氧官能團的名稱為___。
(2)F的結構簡式為___。
(3)A生成B的化學方程式為___。
(4)寫出C合成D的第二個反應的化學方程式___。
(5)同時滿足下列條件的E的同分異構體有___種(不含立體異構)。
①遇FeCl3溶液發生顯色反應 ②能發生銀鏡反應
(6)以乙炔和甲醛為起始原料,選用必要的無機試劑合成1,3-丁二烯,寫出合成路線(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)。___
HC≡CH![]()

![]()
![]() CH2=CHCH=CH2
CH2=CHCH=CH2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,HA的電離常數Ka=1×10-6,向20 mL濃度為0.01 mol·L-1的HA溶液中逐滴加入0.01mol·L-1的NaOH溶液,溶液的pH與加入NaOH溶液的體積之間的關系如圖所示,下列說法正確的是( )
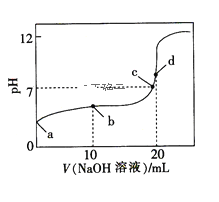
A.a點對應溶液的pH約為4,且溶液中只存在HA的電離平衡
B.b點對應溶液中:c(Na+)>c(A-)>c(HA)>c(H+)>c(OH-)
C.d點對應溶液中:c(OH-)-c(H+)=c(A-)
D.a、b、c、d四點對應的溶液中水的電離程度:a<b<c<d
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】幾種短周期元素的原子半徑及主要化合價如表:
元素代號 | X | Y | Z | W | Q |
原子半徑 | 160 | 143 | 70 | 66 | 104 |
主要化合價 |
|
|
|
|
|
下列選項正確的是( )
A.X、Y元素的金屬性![]()
B.一定條件下,Z單質與W的常見單質直接生成![]()
C.Y的最高價氧化物對應的水化物能溶于氨水
D.Q與W形成的一種化合物可用作紙張漂白劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】美國科學家目前開發出了一種新技術,將能放射出![]() 粒子的砹原子裝入形狀類似DNA螺旋結構的碳納米管中,這種肉眼看不見的微型“核彈”可以搜索、確認并定向摧毀身體任何部位的癌細胞.下列有關說法中正確的是( )
粒子的砹原子裝入形狀類似DNA螺旋結構的碳納米管中,這種肉眼看不見的微型“核彈”可以搜索、確認并定向摧毀身體任何部位的癌細胞.下列有關說法中正確的是( )
A.放射性At原子中,核外電子與核內中子數之差為133
B.根據元素周期律推知:砹單質是![]() 種有色固體,AgAt是一種不溶于水的固體
種有色固體,AgAt是一種不溶于水的固體
C.類似DNA螺旋結構的碳納米管是一種高分子化合物
D.構成碳納米管的微粒直徑在![]() 之間,它實際上是一種膠體
之間,它實際上是一種膠體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA代表阿伏加德羅常數的數值。則下列有關敘述正確的共有
A.1.4g乙烯與丙烯的混合氣體含有NA個碳原子
B.精煉銅,若陽極失去2NA個電子,則陰極增重64g
C.在1L 0.1mol/L的Na2CO3溶液中,陰離子總數小于0.1NA
D.將1L 2mol/L的FeCl3溶液加入到沸水中,加熱使之完全反應,所得氫氧化鐵膠體粒子數為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】4種相鄰主族短周期元素的相對位置如表,元素x的原子核外電子數是m的2倍,y的氧化物具有兩性.![]() 稱為擬鹵素,性質與鹵素相似.下列說法不正確的是( )
稱為擬鹵素,性質與鹵素相似.下列說法不正確的是( )
M | N | ||
X | Y |
A.X位于三周期IIA,其單質可采用電解熔融![]() 制備
制備
B.元素最高價氧化物的水化物中,酸性最強的是![]()
C.氣體分子![]() 的電子式為
的電子式為![]()
D.![]() 其與氫氧化鈉溶液反應的化學方程式為
其與氫氧化鈉溶液反應的化學方程式為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在t ℃時,AgBr在水中的沉淀溶解平衡曲線如圖所示。又知t ℃時AgCl的Ksp=4×10-10 mol2·L-2,下列說法不正確的是
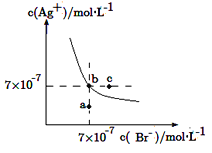
A.在t ℃時,AgBr的Ksp為4.9×10-13 mol2·L-2
B.在AgBr飽和溶液中加入NaBr固體,可使溶液由b點到c點
C.圖中a點對應的是AgBr的不飽和溶液
D.在t ℃時,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)的平衡常數K≈816
AgBr(s)+Cl-(aq)的平衡常數K≈816
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com