
| A. | 乙醇完全燃燒生成水 | |
| B. | 乙醇容易揮發 | |
| C. | 乙醇能與水以任意比例互溶 | |
| D. | 0.1mol乙醇與足量金屬鈉反應生成0.05molH2 |
科目:高中化學 來源: 題型:解答題
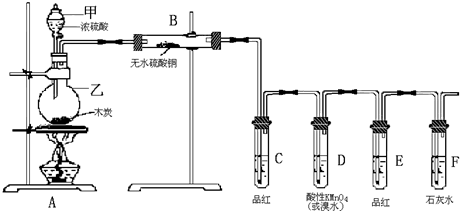
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在該溶液中:Na+、SO42-、CH2O、Mg2+可以大量共存 | |
| B. | 該溶液中Fe3+的檢驗:Fe3++3SCN-=Fe(SCN)3↓ | |
| C. | 與NaHCO3溶液混合:Fe3++3HCO3-=Fe(OH)3↓+3CO2↑ | |
| D. | 每腐蝕32gCu需要1mol/L該溶液500mL |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有①② | B. | 只有①③ | C. | 只有③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KI溶液中:Ca2+、Na+、ClO-、Cl- | |
| B. | 滴入酚酞試液顯紅色的溶液中:Al3+、K+、AlO2-、SO42- | |
| C. | c(H+)=10-12mol•L-1的溶液中:K+、Na+、NO3-、Cl- | |
| D. | 加入鋁粉產生氫氣的溶液中:Na+、Mg2+、HCO3-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將CO2通往入溶有少量氨的BaCl2溶液中,無白色沉淀生成 | |
| B. | 常溫下,稀釋0.1mol/L的醋酸,溶液中所有離子濃度均下降 | |
| C. | 等體積等濃度的CH3COOH與NaOH溶液混合后,溶液中離子濃度:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | AgCl在同濃度的CaCl2和NaCl溶液中的溶解度相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X、M兩種元素只能形成X2M型化合物 | |
| B. | 元素W和M的某些單質可作為水處理中的消毒劑 | |
| C. | 元素Y、Z、W的單質晶體屬于同種類型的晶體 | |
| D. | 由于W、Z、M元素的氫化物相對分子質量依次減小,所以其沸點依次降低 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com