
【題目】我國預計在2020年前后建成自己的載人空間站。為了實現空間站的零排放,循環利用人體呼出的CO2并提供O2,我國科學家設計了一種裝置(如下圖),實現了“太陽能一電能一化學能”轉化,總反應方程式為2CO2=2CO+O2 。關于該裝置的下列說法不正確的是

裝置a 裝置b
附:⊕表示陽離子,Θ表示陰離子
A. 裝置a將太陽能轉化為電能,裝置b將電能轉化為化學能
B. 工作過程中OH-向Y電極周圍移動
C. 人體呼出的氣體參與X電極的反應:CO2+2e-+H2O=CO+2OH-
D. 反應完畢后恢復到原溫度,裝置b中電解質溶液的堿性減弱
科目:高中化學 來源: 題型:
【題目】近年來AIST報告正在研制一種“高容量、低成本”鋰-銅空氣燃料電池。該電池通過一種復雜的銅腐蝕“現象”產生電力,其中放電過程為2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列說法不正確的是( )

A. 放電時,Li+透過固體電解質向Cu極移動
B. 放電時,負極的電極反應式為Cu2O+H2O+2e-=2Cu+2OH-
C. 通空氣時,銅被腐蝕,表面產生Cu2O
D. 整個反應過程中,銅相當于催化劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學設計如下實驗方案,以分離KCl和BaCl2兩種固體混合物,試回答下列問題:

供選試劑:Na2SO4溶液、K2CO3溶液、K2SO4溶液、鹽酸
(1)操作①的名稱是________,操作②的名稱是____________。
(2)試劑a是____________(填化學式,下同),試劑b是__________,固體B是____________。
(3)加入試劑a所發生反應的化學方程式為__________________________________。
加入試劑b所發生反應的化學方程式為____________________________________。
(4)該方案能否達到實驗目的:__________________________(填“能”或“不能”)。若不能,應如何改進?(若能,此問不用回答)__________。
(5)若要測定原混合物中BaCl2的質量分數,除了要準確稱量混合物的質量外,至少還要獲得的數據是____的質量。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】觀察下列比例模型,每個模型表示的分子均由C、H、O中的兩種或三種構成。對各模型表示的物質的相關敘述正確的是( )
比例模型 | 對模型表示的物質的相關敘述 | |
A |
| 將形狀、大小均相同的金屬鈉分別投入盛有0.1 mol/L的該物質的水溶液、無水乙醇和水的燒杯中,盛該物質的燒杯中產生氣泡的速率最慢 |
B |
| 將灼熱的銅絲反復插入盛有該物質的試管中,觀察到銅絲由黑色變為光亮的紅色并產生有刺激性氣味的物質。此反應體現了該物質的氧化性 |
C |
| 在分液漏斗中加入該物質與碘水的混合液,充分振蕩,碘水褪色,此時發生了取代反應 |
D |
| 該物質及其碳原子數小于10的同系物中,一氯代物只有一種(不考慮立體異構)的物質共有4種 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有①甲烷、②乙烯、③苯、④乙酸、⑤葡萄糖5種有機物,請用序號或按題中要求作答:
(1)分子中所有原子一定都共面的是________。
(2)含氫量最高的有機化合物是________,其電子式為________。
(3)完全燃燒后生成的CO2和水的物質的量之比為1∶1的化合物是________。
(4)其中含有兩種不同官能團的有機物是________,官能團的名稱分別為________和________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2017年11月聯合國氣候大會在德國波恩開幕,CO2的回收利用再一次提上了日程。
I利用CO2制取丙烯(C3H6)
(1)用CO2催化加氫可制取丙烯的原理為:3CO2(g)+9H2(g) ![]() C3H6(g)+6H2O(g) △H。
C3H6(g)+6H2O(g) △H。
已知熱化學方程式如下
①2C2H6(g)+9O2(g)=6CO2(g)+6H2O(l) △H1;
②2H2O(g)=2H2(g)+O2(g) ΔH2;
③H2O(g)==H2O(l) △H3;
則制取丙烯反應的△H= ______(用△H1、△H2、△H3表示)。
(2)以稀磷酸為電解質溶液,以石墨為電極,利用太陽能電池將CO2轉化為丙烯的工作原理如下圖所示。
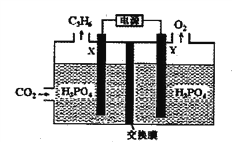
①電解池中的交換膜為_______ :(填“陰”或“陽")離子交換膜,通過交換的離子是_______(填離子符號)。
②陰極的電極反應為_____________________________。
II.利用CO2制取二甲醚(CH3OCH3)
(3)將燃煤廢氣中的CO2轉化為二甲醚的反應原理為:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g)。已知一定條件下,該反應中CO2的平衡轉化率隨溫度、投料
CH3OCH3(g)+3H2O(g)。已知一定條件下,該反應中CO2的平衡轉化率隨溫度、投料
比n(H2)/n(CO2)]的變化曲線如下左圖:
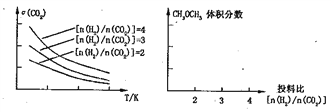
①在其他條件不變時,在右圖中畫出平衡時CH3OCH3的體積分數隨投料比n(H2)/n(CO2)交化的曲線圖____________。
②某溫度下將2.0molCO2(g)和6.0molH2(g)充入容積為2L的密閉容器中,反應到達平衡時改變壓強和溫度,平衡體系中CH3OCH3(g)的物質的量分數變化情況如下圖所示,關于溫度和壓強的關系判斷正確的是____________。
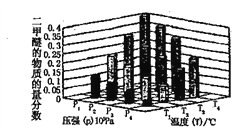
A.P4>P3>P2>P1 B .T4>T3>T2>T1 C.P1>P2>P3>P4 D. T1>T2>T3>T4.
III利用CO2制取甲醇(CH3OH)
用CO2催化加氫制取甲醇的反應為CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H=-b kJ·mol—1(b>0)。T℃時,將 1 mol CO2和4molH2充入的密閉溶液中,測得H2的物質的量隨時間變化如圖中實線所示
CH3OH(g)+H2O(g) △H=-b kJ·mol—1(b>0)。T℃時,將 1 mol CO2和4molH2充入的密閉溶液中,測得H2的物質的量隨時間變化如圖中實線所示
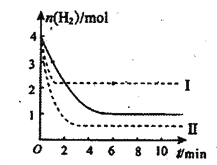
(4)不能證明該反應達到化學平衡狀態的是___________。
A.氣體的總壓強不變
B. CH3 OH(g)和H2O(g)的物質的量之比不變
C.混合氣體的密度不再不變
D.單位時間內斷裂3NA個H—H健同時形成2NA個C=O鍵
(5)僅改變某個反應條件再進行兩次實驗,測得H2的物質的量隨時間變化如圖中虛線I、II所示。曲線Ⅱ對應的實驗條件改變是_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數,下列說法正確的是( )
①標準狀況下,11.2 L以任意比例混合的氮氣和氧氣所含的原子數為NA
②同溫同壓下,體積相同的氫氣和氬氣所含的分子數相等
③1 L 2 mol·L-1的AlCl3溶液中含氯離子為6NA
④標準狀況下,22.4 L H2O中分子數為NA
⑤32 g O2和O3混合氣體中含有原子數為2NA
A. ①②③⑤ B. ①②③④
C. ①③④ D. ③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質中,能與Fe3+反應,且能證明Fe3+具有氧化性的是( )
①SCN﹣;②Fe;③Fe2+;④Cu;⑤Zn;⑥OH﹣ .
A.①②③
B.②④⑤
C.①③⑥
D.①②⑤
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com