
 字詞句篇與同步作文達標系列答案
字詞句篇與同步作文達標系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 瑞典皇家科學院宣布,將2010年諾貝爾物理學獎授予 英國曼徹斯特大學科學家安德烈?海姆和康斯坦丁?諾沃肖洛夫,以表彰他們在石墨烯材料方面的卓越研究.石墨烯是由碳原子構成的單層片狀結構的新材料.具有原子級的厚度、優異的電學性能、出色的化學穩定性和熱力學穩定性.制備石墨烯方法有石墨剝離法、化學氣相沉積法等.石墨烯的球棍模型及分子結構如圖1所示.
瑞典皇家科學院宣布,將2010年諾貝爾物理學獎授予 英國曼徹斯特大學科學家安德烈?海姆和康斯坦丁?諾沃肖洛夫,以表彰他們在石墨烯材料方面的卓越研究.石墨烯是由碳原子構成的單層片狀結構的新材料.具有原子級的厚度、優異的電學性能、出色的化學穩定性和熱力學穩定性.制備石墨烯方法有石墨剝離法、化學氣相沉積法等.石墨烯的球棍模型及分子結構如圖1所示.查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 元素 | Al | B | Be | C | Cl | F | Li |
| X | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | Fe |
| X | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 | 1.8 |


查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
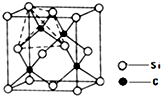 (2013?青島一模)[化學-物質結構與性質]
(2013?青島一模)[化學-物質結構與性質]查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com