
【題目】(1)相同溫度下等物濃度的下列溶液中,A.NH4C1 B.NH4HCO3 C.NH4HSO4 D.(NH4)2SO4
① pH值由大到小的順序是___________________(用對應的字母填寫)。
② NH4+離子濃度由大到小的順序是___________________(用對應的字母填寫)。
(2)25℃向50 mL 0.018 mol·L-1 的 AgNO3溶液中加入50 mL 0.020 mol·L-l的鹽酸,生成沉淀。己知該溫度下AgCl的Ksp =l.0×l0-10,忽略溶液的體積變化,請計算:
① 完全沉淀后,溶液中c(Ag+)=_____________。
② 完全沉淀后,溶液的pH=____________。
(3)弱酸及其鹽在水中存在多種平衡關系。己知NaA水溶液呈堿性,常溫下將0.l mol NaA和0.05 mol HCl溶于水,得到1 L溶液。
① 己知該混合溶液為弱酸性,則溶液中離子濃度由大到小的順序為___________________。
② 向該混合物中再加0.03mol NaOH,溶液中n(A-) +n(OH-)-n(H+) =________。
(4)三氯化鐵是一種重要的化合物,可以用來腐蝕電路板。某腐蝕廢液中含有0.5 mol·L-1 Fe3+和0.26 mol·L-1 Cu2+,欲使Fe3+完全沉淀[c(Fe3+) ≤ 4×l0-5 mol·L-1 ]而Cu2+不沉淀,則需控制溶液pH的范圍為_________。[KspCu(OH)2 = 2.6×l0-19;KspFe(OH)3 = 4×l0-38]
【答案】 B、A、D、C D、C、A、B 1.0×10-7 mol/L 2 c(Na+) > c(A-) > c(Cl-) > c(H+) > c(OH-) 0.08mol 3 ≤pH≤5
【解析】(1)A.銨根離子水解,溶液呈酸性;B.碳酸氫根離子促進銨根離子水解,酸性較氯化銨溶液酸性弱;C.電離出氫離子,并抑制銨根離子水解,顯強酸性;D.銨根離子水解,水解程度不大,銨根離子濃度最大,酸性比氯化銨溶液的酸性強,但是比硫酸氫銨的酸性弱。
①pH值由大到小的順序是: B、A、D、C ,正確答案: B、A、D、C 。
②NH4+離子濃度由大到小的順序是D、C、A、B ;正確答案D、C、A、B。
(2)①向50 mL 0.018 mol·L-1 的 AgNO3溶液中加入50 mL 0.020 mol·L-l的鹽酸, 混合后兩者濃度分別為c(Ag+)=0.018/2=0.009 mol·L-l、c(Cl-)=0.02/2=0.01mol·L-l,由于Ag+與Cl-為等物質的量反應,因此Cl-過量,濃度為c(Cl-)=0.01-0.009=0.001 mol·L-l,根據Ksp =l.0×l0-10,則c(Ag+)= l.0×l0-10/0.001=1.0×10-7 mol/L;正確答案:1.0×10-7 mol/L。
②沉淀生成后,氫離子濃度c=0.02/2=0.01 mol/L,所以溶液的pH=2;正確答案:2。
(3)①常溫下將0.l mol NaA和0.05 mol HCl溶于水,得到1 L溶液,所得溶液中含有:0.05 molNaA、0.05molHA、0.05molNaCl;己知該混合溶液為弱酸性,同濃度溶液中HA電離大于![]() 離子的水解, c(A-) > c(Cl-)、c(H+) > c(OH-),則溶液中離子濃度大小為:c(Na+) > c(A-) > c(Cl-) > c(H+) > c(OH-);正確答案:c(Na+) > c(A-) > c(Cl-) > c(H+) > c(OH-)。
離子的水解, c(A-) > c(Cl-)、c(H+) > c(OH-),則溶液中離子濃度大小為:c(Na+) > c(A-) > c(Cl-) > c(H+) > c(OH-);正確答案:c(Na+) > c(A-) > c(Cl-) > c(H+) > c(OH-)。
②向該混合物中再加0.03mol NaOH,酸堿發生中和后,混合液中含有0.05molNaCl、0.08molNaA、0.02 molHA,根據混合液中電荷守恒可得:n(A-) +n(OH-)+ c(Cl-)= c(Na+)+ n(H+),則n(A-) +n(OH-)-n(H+) =c(Na+)-c(Cl-)=0.05+0.08-0.05=0.08 mol;正確答案:0.08 mol。
(4)根據![]() ,當
,當![]() 完全沉淀
完全沉淀![]() 時
時![]() ,此時溶液
,此時溶液![]() ,當
,當![]() 開始沉淀時,根據
開始沉淀時,根據![]() ,
,![]() ,此時溶液
,此時溶液![]() ,則需控制溶液
,則需控制溶液![]() 的范圍為3 ≤pH≤5;正確答案:3 ≤pH≤5。
的范圍為3 ≤pH≤5;正確答案:3 ≤pH≤5。


 全能測控期末小狀元系列答案
全能測控期末小狀元系列答案科目:高中化學 來源: 題型:
【題目】取Na2CO3和NaHCO3的混合粉末樣品22.1g,將其加熱到質量不再改變,冷卻后稱固體質量為15.9g。則原混合物中Na2CO3的質量為
A. 4.2g B. 5.3g C. 8.4 g D. 10.6 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】奶粉中蛋白質含量的測定往往采用“凱氏定氮法”,其原理是食品與硫酸和催化劑一同加熱,使蛋白質分解,分解的氨與硫酸結合生成硫酸銨。然后堿化蒸餾使氨游離,用硼酸吸收后再以硫酸或鹽酸標準溶液滴定,根據酸的消耗量乘以換算系數,即為蛋白質含量。
操作步驟:
①樣品處理:準確稱取一定量的固體樣品奶粉,移入干燥的燒杯中,經過一系列的處理,待冷卻后移入一定體積的容量瓶中。
②NH3的蒸餾和吸收:把制得的溶液(取一定量),通過定氮裝置,經過一系列的反應,使氨變成硫酸銨,再經過堿化蒸餾后,氨即成為游離態,游離氨經硼酸吸收。
③氨的滴定:用標準鹽酸溶液滴定所生成的硼酸銨,由消耗的鹽酸標準液計算出總氮量,再折算為粗蛋白含量。
請回答下列問題:
(1)在樣品的處理過程中使用到了容量瓶,怎樣檢查容量瓶是否漏水_________。
(2)在配制過程中,下列哪項操作可能使配制的溶液的濃度偏大_______。
A.燒杯中溶液轉移到容量瓶中時,未洗滌燒杯 B.定容時,俯視刻度線
C.定容時,仰視刻度線 D.移液時,有少量液體濺出
(3)若稱取樣品的質量為1.5g,共配制100mL的溶液,取其中的20mL,經過一系列處理后,使N轉變為硼酸銨然后用0.1mol·L-1鹽酸滴定,其用去鹽酸的體積為23.0mL,則該樣品中N的含量為________。
(滴定過程中涉及到的反應方程式:(NH4)2B4O7+2HCl+5H2O=2NH4Cl+4H3BO3)
(4)一些不法奶農利用“凱氏定氮法”只檢測氮元素的含量而得出蛋白質的含量這個檢測法的缺點,以便牛奶檢測時蛋白質的含量達標,而往牛奶中添加三聚氰胺(C3N6H6)。則三聚氰胺中氮的含量為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】漢黃芩素是傳統中草藥黃芩的有效成分之一,對腫瘤細胞的殺傷有獨特作用。下列有 關漢黃芩素的敘述正確的是

A. 漢黃芩素的分子式為 C16H13O5
B. 該物質遇 FeCl3 溶液顯色
C. 1 mol 該物質與溴水反應,最多消耗 1 mol Br2
D. 與足量 H2 發生加成反應后,該分子中官能團的種類減少 1 種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知2SO2(g)+O2(g)![]() 2SO3(g) △H=-197 kJ·mol-1,向同溫、同體積的三個密閉容器中分別充入氣體:(甲)2 mol SO2 和1 mol O2;(乙) 1 mol SO2 和0.5 mol O2;(丙) 2 mol SO3;恒溫、恒容下反應達平衡時,下列關系一定正確的是
2SO3(g) △H=-197 kJ·mol-1,向同溫、同體積的三個密閉容器中分別充入氣體:(甲)2 mol SO2 和1 mol O2;(乙) 1 mol SO2 和0.5 mol O2;(丙) 2 mol SO3;恒溫、恒容下反應達平衡時,下列關系一定正確的是
A. 若c(SO2)與c(O2)之比為k,則:k甲=k丙>k乙
B. 反應放出或吸收熱量的數值Q:Q甲=Q丙>2Q乙
C. 容器內壓強P:P甲=P丙>2P乙
D. SO3的質量m:m甲=m丙>2m乙
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某回學用下列裝置完成了濃硫酸和SO2性質實驗(夾持裝置已省略)
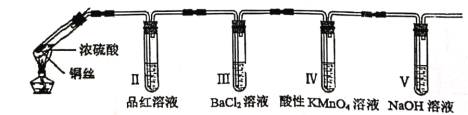
下列說法錯誤的是
A. 反應后,試管Ⅰ中出現白色固體,將其放入水中,溶液顯藍色
B. 試管Ⅱ中品紅溶液逐漸褪色,對其加熱溶液又恢復紅色
C. 試管Ⅳ中高錳酸鉀褪色,體現了SO2的漂白性
D. 試管Ⅴ可以改為裝有堿石灰的干燥管
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物H是一種有機光電材料中間體。實驗室由芳香化合物A制備H的一種合成路線如下:
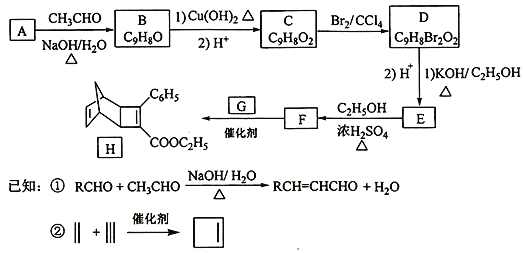
回答下列問題:
(1)A的化學名稱為__________。
(2)由C生成D和E生成F的反應類型分別為__________、_________。
(3)E的結構簡式為____________。
(4)G為甲苯的同分異構體,由F生成H的化學方程式為___________。
(5)芳香化合物X是F的同分異構體,X能與飽和碳酸氫鈉溶液反應放出CO2,其核磁共振氫譜顯示有4種不同化學環境的氫,峰面積比為6∶2∶1∶1,寫出2種符合要求的X的結構簡式____________。
(6)寫出用環戊烷和2-丁炔為原料制備化合物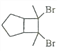 的合成路線________(其他試劑任選)。
的合成路線________(其他試劑任選)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列熱化學方程式中的ΔH能表示物質燃燒熱的是(假設數據均正確)
A. C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=+1 367 kJ·mol-1
B. 2CO (g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
C. H2 (g)+1/2O2(g)= H2O(g ) ΔH=-285.8 kJ·mol-1
D. S(s)+O2(g)=SO2(g) ΔH=-296.95 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈷酸鋰電池應用廣泛,電池正極材料主要含有LiCoO2、導電劑乙炔黑、鋁箔及少量Fe,可通過下列實驗方法回收鈷、鋰。
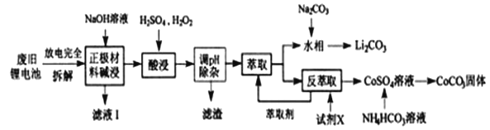
幾種金屬離子沉淀完全(離子濃度為10-5mo/L)的pH如下表:
離子 | Fe3+ | Al3+ | Fe2+ | Co2+ |
溶液pH | 3.2 | 4.7 | 9.0 | 9.2 |
回答下列問題:
(1)濾液I的主要成分是_________。
(2)已知:氧化性Co3+>H2O2>Fe3+,“酸浸”過程中H2O2所起主要作用是________不能用鹽酸代替硫酸,原因是:__________。“調節pH”除去的離子主要有Al3+和_____。
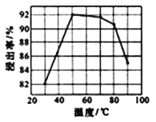
(3)酸浸時浸出率隨溫度變化如圖所示,溫度升高至50℃以上時浸出率下降的原因是_________。
(4)“萃取”和“反萃取“可簡單表示為:Co2++2(HA)2![]() Co(HA2)2+2H+,則反萃取過程加入的試劑X是____________。
Co(HA2)2+2H+,則反萃取過程加入的試劑X是____________。
(5)向CoSO4溶液中加入NH4HCO3溶液,發生反應的離子方程式為_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com