
【題目】磺酰氯(SO2Cl2)是一種有機氯化劑,也是鋰電池正極活性物質。已知磺酰氯是一種無色液體,熔點-54.1℃,沸點69.1℃,遇水發生劇烈水解,且產生白霧。
(1)SO2Cl2水解的方程式為_______________________________________________
(2)某學習小組的同學依據反應:SO2(g)+ Cl2(g)![]() SO2Cl2(g);△H <0,設計制備磺酰氯裝置如圖:
SO2Cl2(g);△H <0,設計制備磺酰氯裝置如圖:
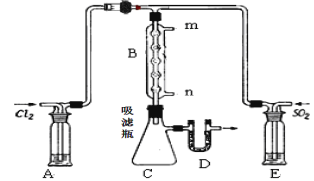
①E中所用的試劑為________________
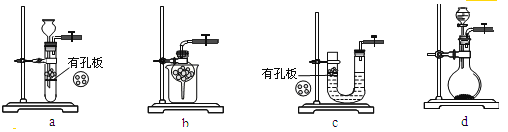
②實驗室用Na2SO3和硫酸制備SO2,可選用的氣體發生裝置是____(選填編號);檢查該裝置氣密性的操作是:關閉止水夾,再___________________________________
③B處反應管內五球中玻璃棉上的活性炭的作用為:_______________________D處U形管中盛放的試劑為_________________,作用 :________________________
(3)已知:以下三個反應的反應熱,a、b、c均為正值
①SO2(g)+Cl2(g)+SCl2(g) ![]() 2SOCl2(g) △H=-akJ·mol-1
2SOCl2(g) △H=-akJ·mol-1
②SO2Cl2(g)+SCl2(g) ![]() 2SOCl2(g) △H=-bkJ·mol-1
2SOCl2(g) △H=-bkJ·mol-1
③SO2Cl2(l) ![]() SO2Cl2(g) △H= + ckJ·mol-1
SO2Cl2(g) △H= + ckJ·mol-1
則反應:SO2(g)+Cl2(g) ![]() SO2Cl2(l) △H=______________kJ·mol-1(用含a、b、c的代數式表示);該反應平衡常數表達式為K=___________。從化學平衡移動角度分析,反應管通水冷卻的目的為____
SO2Cl2(l) △H=______________kJ·mol-1(用含a、b、c的代數式表示);該反應平衡常數表達式為K=___________。從化學平衡移動角度分析,反應管通水冷卻的目的為____
【答案】SO2Cl2+2H2O=H2SO4+2HCl 濃硫酸 d 打開分液漏斗活塞加水,一段時間后,如水無法滴入說明氣密性良好 催化劑 堿石灰 吸收尾氣,防止空氣中的水蒸氣進入C (b-a-c) 1/ c(SO2)·c(Cl2) 將產物冷卻,分離出來,有利于平衡正向移動
【解析】
(1)SO2Cl2遇水發生劇烈水解,且產生白霧,白霧是水解生成HCl與空氣中水蒸氣結合所致,則-SO2-基團結合2個-OH生成H2SO4;
(2)①E中盛放的液體用于干燥二氧化硫;
②因為Na2SO3易溶于水,a、b、c裝置均不能選用,實驗室用Na2SO3和硫酸制備SO2,可選用的氣體發生裝置是d;關閉止水夾,若氣密性很好,則分液漏斗中水不能滴入燒瓶中;
③B處反應管內五球中玻璃棉上的活性炭對氯氣和二氧化硫的反應起催化作用;D處U形管中盛放的固體干燥劑,可能是固體堿石灰;
(3)根據蓋斯定律計算分析;根據平衡常數表達式定義書寫,依據化學平衡原理回答即可。
(1)SO2Cl2遇水發生劇烈水解,且產生白霧,白霧是水解生成HCl與空氣中水蒸氣結合所致,則-SO2-基團結合2個-OH生成H2SO4,反應方程式為:SO2Cl2+2H2O=H2SO4+2HCl,故答案為:SO2Cl2+2H2O=H2SO4+2HCl;
(2)①E中盛放的液體用于干燥二氧化硫,可以用濃硫酸干燥二氧化硫,故答案為:濃硫酸;
②因為Na2SO3易溶于水,a、b、c裝置均不能選用,實驗室用Na2SO3和硫酸制備SO2,可選用的氣體發生裝置是d;檢查該裝置氣密性的操作是:關閉止水夾,若氣密性很好,則分液漏斗中水不能滴入燒瓶中,故答案為:d;打開分液漏斗活塞加水,一段時間后,如水無法滴入說明氣密性良好;
③B處反應管內五球中玻璃棉上的活性炭對氯氣和二氧化硫的反應起催化作用,D處U形管中盛放的固體干燥劑,可能是固體堿石灰,故答案為:催化劑;堿石灰;吸收尾氣,防止空氣中的水蒸氣進入C;
(3)①SO2(g)+Cl2(g)+SCl2(g)2SOCl2(g)△H=-akJmol-1
②SO2Cl2(g)+SCl2(g)2SOCl2(g)△H=-bkJmol-1
③SO2Cl2(l)SO2Cl2(g)△H=+ckJmol-1
根據蓋斯定律①-②-③得:SO2(g)+Cl2(g)SO2Cl2(l)△H=-(a-b+c )kJmol-1,平衡常數K=![]() ,依據化學平衡移動原理解釋為:反應管中通入冷凝水,將產物冷卻,分離出來,有利于平衡正向移動,故答案為:-(a+c-b);
,依據化學平衡移動原理解釋為:反應管中通入冷凝水,將產物冷卻,分離出來,有利于平衡正向移動,故答案為:-(a+c-b);![]() ;將產物冷卻,分離出來,有利于平衡正向移動。
;將產物冷卻,分離出來,有利于平衡正向移動。


科目:高中化學 來源: 題型:
【題目】室溫下,將0.1molL-1NaOH溶液逐滴滴入10mL0.1molL-1NH4HSO4溶液中,溶液的pH與NaOH溶液體積關系如圖所示:下列關系中,不正確的是
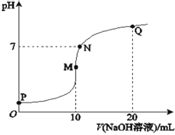
A.M點c(Na+)>c(NH4+)
B.N點c(NH4+)+c(Na+)=2c(SO42-)
C.Q點c(NH4+)+c(NH3H2O)=c(Na+)
D.M、N、Q三點中,水的電離程度M>N>Q
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A的產量可以用于衡量一個國家的石油化工發展水平。B和D是生活中兩種常見的有機物,D是食醋的主要成分。相互轉化關系如圖所示。
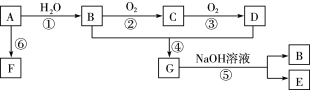
(1)A的結構簡式是______,D中官能團名稱是:______。
(2)在制備G的實驗中,反應條件是_____,為了除去產物中的雜質所用的試劑是_____。
(3)用于鑒別A和甲烷的一種試劑是________。
(4)寫出下列反應的化學方程式:①:__________,④:________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,取濃度相同的NaOH和HCl溶液,以3∶2體積比相混合,所得溶液的pH等于12,則原溶液的濃度為
A.0.01mol·L-1B.0.017mol·L-1
C.0.05mol·L-1D.0.50mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用如圖所示的裝置和其他必要的儀器用品,完成下列實驗。

已知2NH3+3CuO![]() N2+3Cu+3H2O,該實驗證明氨氣具有還原性。
N2+3Cu+3H2O,該實驗證明氨氣具有還原性。
(1)堿石灰的作用是______________,倒扣漏斗的作用是___________________。
(2)濃氨水與固體NaOH接觸,會逸出大量氨氣原因是______________________。
(3)硬質玻璃管中可觀察到的實驗現象是_________________________________。
(4)常溫下,若氨水與稀硫酸恰好完全中和,則所得溶液中各離子濃度的大小順序為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上利用軟錳礦(主要成分為MnO2,同時含少量鐵、鋁等的化合物)制備硫酸錳的常見流程如下:
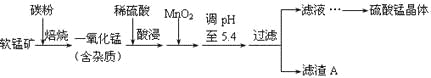
部分金屬陽離子以氫氧化物形式完全沉淀時溶液的pH見下表:
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
pH | 5.2 | 3.2 | 9.7 | 10.4 |
(1)一氧化錳用硫酸酸浸時發生的主要反應的離子方程式為____________________。酸浸后加入MnO2將溶液中的Fe2+氧化成Fe3+,其目的是___________。
(2)濾渣A的成分除MnO2外,還有_______________。
(3)MnO2是制造堿性鋅錳電池的基本原料,放電時負極的電極反應式為________。工業上以石墨為電極電解酸化的MnSO4溶液生產MnO2,陽極的電極反應式為_________,當陰極產生4.48L(標況)氣體時,MnO2的理論產量為______g。
(4)錳的三種難溶化合物的溶度積:Ksp(MnCO3)=1.8×10-11,Ksp[Mn(OH)2]=1.9×10-13,Ksp(MnS)=2.0×10-13,則上述三種難溶物的飽和溶液中,Mn2+濃度由大到小的順序是_______>_______>_______(填寫化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】據媒體報道,法國一家公司Tiamat日前研發出比當前廣泛使用的鋰電池成本更低、壽命更長、充電速度更快的鈉離子電池,預計從2020年開始實現工業生產。該電池的負極材料為Na2Co2TeO6(制備原料為Na2CO3、Co3O4和TeO2),電解液為NaClO4的碳酸丙烯酯溶液。回答下列問題:
(1)Co 屬于元素周期表中______區元素,其基態原子的價電子排布式為______。
(2)基態Na原子中,核外電子占據的原子軌道總數為______,最高能層電子云輪廓圖形狀為_____
(3)結合題中信息判斷:C、O、Cl的電負性由小到大的順序為______(用元素符號表示)。
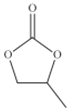
(4)ClO4 -的幾何構型為______;碳酸丙烯酯的結構簡式如圖所示,則其中碳原子的雜化軌道類型為______,1mol碳酸丙烯酯中![]() 鍵的數目為______。
鍵的數目為______。
(5)[Co(H2O)6]3+的幾何構型為正八面體形,配體是______,該配離子包含的作用力為______(填選項字母)。
A.離子鍵B.金屬鍵C.配位鍵D.氫鍵E.極性鍵
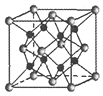
(6)Na和O形成的離子化合物的晶胞結構如圖所示,晶胞中O的配位數為______,該晶胞的密度為ρg/cm3,阿伏加德羅常數的值為NA,則Na與O之間的最短距離為______nm(用含ρ、NA的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】磷和砷的相關化合物在化工、醫藥、材料等領域有著廣泛的應用。回答下列問題:
(1)紅磷是巨型共價分子,無定型結構,下列方法能證明紅磷是非晶體的是_____。
A.質譜法 B.原子發射光譜法 C.核磁共振譜法 D.X射線行射法
(2)基態As原子的核外電子排布式為_____,As原子的逐級電離能數據如下:
第一電離能 | 第二電離能 | 第三電離能 | 第四電離能 | 第五電離能 | 第六電離能 |
947.0 | 1798 | 2735 | 4837 | 6043 | 12310 |
為什么第五電離能與第六電離能相差較大_____。
(3)黑磷是新型二維半導體材料,具有片層結構(如下圖所示),P原子的雜化形式為_____,層與層之間的相互作用為_____。
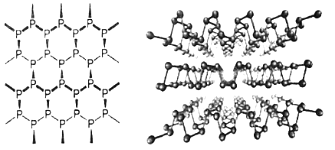
(4)GaAs的熔點為1238℃,且熔融狀態不導電,其晶胞結構如下圖所示,該晶體的類型為_____,每個As原子周圍最近的As原子數目為_____,與同一個Ga原子距離最近的As原子構成的空間構型為_____,一個GaAs晶胞中配位鍵的數目為_____。
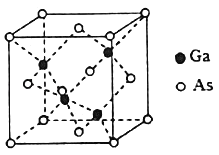
(5)已知GaAs的密度為dg/cm3,摩爾質量為Mg/mol,阿伏加德羅常數用NA表示,則晶胞中最近的As和Ga原子核間距為_____ nm(列式表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com