
【題目】用下圖所示裝置進行實驗,將少量液體甲逐滴加入到固體乙中,試管中試劑為丙,則下表中現象與結論均正確的是
選項 | 甲 | 乙 | 丙 | 試管中現象 |
A | 濃鹽酸 | 二氧化錳 | 石蕊溶液 | 先變紅后褪色 |
B | 濃氨水 | 生石灰 | A1Cl3溶液 | 先沉淀后消失 |
C | 醋酸 | 碳酸鈣 | BaC12溶液 | 變渾濁 |
D | 濃硝酸 | 銅 | 水 | 試管口出現紅棕色 |
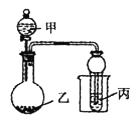
A. A B. B C. C D. D
【答案】D
【解析】
A.濃鹽酸與MnO2在加熱時發生反應產生Cl2。該裝置為加熱,反應不能發生。故A錯誤;
B.把濃氨水滴加在生石灰上,由于CaO與水發生反應,消耗水,產生的Ca(OH)2溶解放熱,會加速氨水的分解,產生氨氣。把氨氣通入到A1Cl3溶液中,發生反應:Al3++3NH3+3H2O=3NH4++Al(OH)3↓。因為NH3·H2O是弱堿,不能溶解產生的Al(OH)3沉淀。因此現象有誤。故B錯誤;
C.把醋酸加入到碳酸鈣中,發生反應:2CH3COOH+CaCO3=(CH3COO)2Ca+ H2O+ CO2↑。把氣體通入到BaC12溶液中時,因為酸性HCl>H2CO3。所以不會發生反應,試管中不會出現渾濁現象。故C錯誤;
D.濃硝酸在常溫下與Cu發生反應:Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O 。3NO2+H2O = 2HNO3+NO。O2+2NO=2NO2。NO2是紅棕色的氣體。故D正確。
故選D。


 海淀黃岡名師導航系列答案
海淀黃岡名師導航系列答案 普通高中同步練習冊系列答案
普通高中同步練習冊系列答案科目:高中化學 來源: 題型:
【題目】完成下列流程圖。
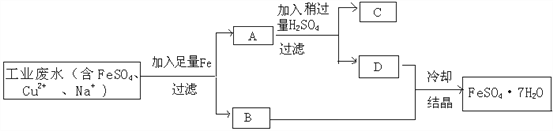
(1)其中,濾渣A中有______________,濾液D中溶質有________________。(填化學式)
(2))加入Fe的目的是_______________________________________。(用化學方程式表示)
(3)加入H2SO4的目的是____________________________________。(用化學方程式表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國傳統文化是人類文明的瑰寶,古代文獻中記載了大量古代化學的研究成果。回答下面問題。
(1)我國最原始的陶瓷約出現在距今12000年前,制作瓷器所用的原料是高嶺士,其晶體化學式是Al4[Si4O10](OH)8,用氧化物表示其組成為____。
(2)《本草綱目》中記載:“(火藥)乃焰消( KNO3)、硫磺、杉木炭所合,以為烽燧銃機諸藥者。”反應原理為:S+2KNO3+3C![]() K2S+N2↑+2CO2↑,該反應的氧化劑是____ ,反應轉移4mol電子時,被S氧化的C有____mol。
K2S+N2↑+2CO2↑,該反應的氧化劑是____ ,反應轉移4mol電子時,被S氧化的C有____mol。
(3)我國古代中藥學著作《新修本草》記載的藥物有844種,其中有關“青礬”的描述為:“本來綠色,新出窟未見風者,正如瑁璃…燒之赤色…。”我國早期科技叢書《物理小適-金石類》 記載有加熱青礬時的景象:“青礬廠氣熏人,衣服當之易爛,載木不盛。”青礬就是綠礬( FeSO4·7H2O)。根據以上信息,寫出“青礬”受熱分解的化學方程式____
(4)中國古代第一部藥物學專著《神農本革經》記載:“石硫磺(S)…主陰蝕疽痔惡血,堅筋骨,除頭禿,能化金銀銅鐵奇物。”根據以上信息,得出硫磺(S)具有的性質或用途是 _____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應原理在工業生產中具有十分重要的意義。
(1)工業生產可以用NH3(g)與CO2(g)經兩步反應生成尿素,兩步反應的能量變化示意圖如下:

則NH3(g)與CO2(g)反應生成尿素的熱化學方程式為___________________________。
(2)已知反應Fe(s)+CO2(g) ![]() FeO(s)+CO(g) ΔH=a kJ·mol-1。測得在不同溫度下,該反應的平衡常數K隨溫度的變化如下:
FeO(s)+CO(g) ΔH=a kJ·mol-1。測得在不同溫度下,該反應的平衡常數K隨溫度的變化如下:
溫度(℃) | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
①該反應的化學平衡常數K的表達式為____________,a________0(填“>”、“<”或“=”)。在500 ℃ 2 L密閉容器中進行反應,Fe和CO2的起始量均為4 mol,則5 min后達到平衡時CO2的轉化率為________,生成CO的平均速率v(CO)為_______________。
②700 ℃反應達到平衡后,要使反應速率增大且平衡向右移動, 可采取的措施有 ___________。
(3)利用CO與H2可直接合成甲醇,下圖是由“甲醇-空氣”形成的綠色燃料電池的工作原理示意圖,寫出以石墨為電極的電池工作時負極的電極反應式_____________________,利用該電池電解1L 0.5mol/L的CuSO4溶液,當消耗560mLO2(標準狀況下)時,電解后溶液的pH=_________(溶液電解前后體積的變化忽略不計)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化碘的化學式為ICl,性質和溴非常相似。下列關于ICl的有關說法中不正確的是( )
A. I與Cl之間形成的化學鍵為共價鍵
B. ICl分子為共價化合物分子
C. 該物質在反應中通常體現氧化性
D. ICl在反應ICl+2NaOH![]() NaCl+NaIO+H2O中作氧化劑
NaCl+NaIO+H2O中作氧化劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】磷酸鐵鋰電池應用廣泛。該鋰電池將鋰嵌入碳材料,含Li+導電固體為電解質;電解質中遷移介質是一種有機聚合物,其單體之一M結構簡式如下圖:

M的結構簡式
電池反應為:LiC6+FePO4![]() LiFePO4+6C
LiFePO4+6C
下列說法正確的是
A.放電時,體系中的Li+向負極移動
B.放電時,FePO4作正極發生氧化反應
C.充電時,與電源正極相連的電極反應為:LiFePO4-e-==Li++FePO4
D.1 mol有機物M與足量NaOH溶液反應,消耗2 mol NaOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.銅的化學性質活潑,不宜用銅制作盛食品的器皿
B.銅的導電能力不如鋁
C.由于Cu2+有氧化性,所以用CuSO4來配制農藥
D.因為Cu2+能使蛋白質變性,所以銅鹽溶液有毒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】寫出或完成下列熱化學方程式。
(1)0.5molCH4完全燃燒生成CO2和液態水時,放出445kJ 的熱量。寫出CH4燃燒的熱化學方程式_____。
(2)通常人們把拆開1mol某化學鍵吸收的能量看成該化學鍵的鍵能。下表是一些化學鍵的鍵能。
化學鍵 | C-H | C-F | H-F | F-F |
鍵能kJ/mol | 414 | 489 | 565 | 155 |
根據鍵能數據估算下列反應:CH4(g) + 4F2(g)=CF4(g) + 4HF(g)的反應熱△H為_____。
(3)1840年瑞士的化學家蓋斯(Hess)在總結大量實驗事實(熱化學實驗數據)的基礎上提出:“定壓或定容條件下的任意化學反應,在不做其它功時,不論是一步完成的還是幾步完成的,其熱效應總是相同的(反應熱的總值相等)。”
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3
請寫出CO還原FeO的熱化學方程式:_____。
(4)在恒溫(500K)、體積為1.0L 的密閉容器中通入1.0 mol N2和1.0 mol H2發生合成氨反應N2 + 3H2![]() 2NH3,20 min 后達到平衡,測得反應放出的熱量為18.4 kJ,混合氣體的物質的量為1.6 mol,該反應的熱化學方程式為_____。
2NH3,20 min 后達到平衡,測得反應放出的熱量為18.4 kJ,混合氣體的物質的量為1.6 mol,該反應的熱化學方程式為_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com