
【題目】金剛烷是一種重要的化工原料,工業上可通過下列途徑制備。請回答下列有關問題:
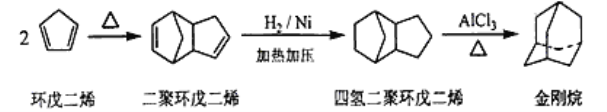
(1)環戊二烯分子中最多有____________個原子共平面。
(2)金剛烷的分子式為_________,其分子中的—CH2—基團有______個,金剛烷的一氯代物有______種。
(3)由環戊二烯生成二聚環戊二烯的反應類型是_______。
(4)已知烯烴能發生如下反應:![]() RCHO+R’CHO,請寫出下列反應產物的結構簡式:
RCHO+R’CHO,請寫出下列反應產物的結構簡式: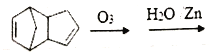 _________________,該產物中官能團的名稱是___________________。
_________________,該產物中官能團的名稱是___________________。
【答案】 9 C10H16 6 2 加成 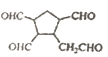 醛基
醛基
【解析】(1)C=C為平面結構,與雙鍵碳直接相連的原子一定在同一平面內;(2)由結構可知金剛烷分子中有6個CH2,其中4個被三個環共用;(3)DCPD與順丁烯二酸發生如下反應,生成順丁烯二酸DCPD酯,由反應可知,順丁烯二酸中的一個C=C斷裂,DCPD 可以和某些醇發生類似的反應,利用產物分析反應物;(4)由信息可知,碳碳雙鍵的碳上含H原子被氧化為醛,以此分析。
(1)C=C為平面結構,與雙鍵碳直接相連的原子一定在同一平面內,則5個C和4個H共9個原子在同一平面內;(2)由結構可知金剛烷的分子式為C10H16,分子中有6個CH2,其中4個被三個環共用,金剛烷中有兩種不同環境下的氫原子,故其一氯代物有2種;(3)DCPD與順丁烯二酸發生如下反應,生成順丁烯二酸DCPD酯,由反應可知,順丁烯二酸中的一個C=C斷裂,則發生加成反應,由DCPD 可以和某些醇發生類似的反應,根據生成物的結構可知,反應物為 、CH3CHOHCH2OH,故答案為:加成反應;(4)由信息可知,碳碳雙鍵的碳上含H原子被氧化為醛,則發生
、CH3CHOHCH2OH,故答案為:加成反應;(4)由信息可知,碳碳雙鍵的碳上含H原子被氧化為醛,則發生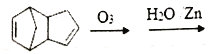
 ,
, 中官能團的名稱是醛基。
中官能團的名稱是醛基。


 王后雄學案教材完全解讀系列答案
王后雄學案教材完全解讀系列答案 海淀課時新作業金榜卷系列答案
海淀課時新作業金榜卷系列答案科目:高中化學 來源: 題型:
【題目】世上萬物、神奇可測,其性質與變化是物質的組成與結構發生了變化的結果。回答下列問題。
(1)根據雜化軌道理論判斷,下列分子的空間構型是V形的是_____(填字母)。
A.BeCl2 B.H2O C.HCHO D.CS2
(2)原子序數小于36的元素Q和T,在周期表中既位于同一周期又位于同一族,且T的原子序數比Q多2。T的基態原子的外圍電子(價電子)排布式為____,Q2+的未成對電子數是_____。
(3)銅及其合金是人類最早使用的金屬材料,Cu2+能與NH3形成配位數為4的配合物[Cu(NH3)4]SO4。
①制元素在周期表中的位置是______,[Cu(NH3)4]SO4中,N、O、S三種元素的第一電離能由大到小的順序為______。
②[Cu(NH3)4]SO4中,存在的化學鍵的類型有______(填字母)。
A離子鍵 B金屬鍵 C.配位鍵 D.非極性鍵 E極性鍵
③NH3中N原子的雜化軌道類型是______,寫出一種與SO42-互為等電子體的分子的化學式:_ ______。
④[Cu(NH3)4]2+具有對稱的空間構型,[Cu(NH3)4]2+中的兩個NH3被兩個Cl-取代,能得到兩種不同結構的產物.則[Cu(NH3)4]2+的空間構型為_________。
(4)氧與銅形成的某種離子晶體的晶胞如圖所示。則該化合物的化學式為_____,如果該晶體的密度為ρg/cm3,則該晶體內銅離子與氧離子間的最近距離為_____(用含ρ的代數式表示,其中阿伏加德羅常數用NA表示)cm。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將1.92gCu和一定量的濃HNO3反應,隨著Cu的不斷減少,反應生成氣體的顏色逐漸變淺,當Cu反應完畢時,共收集到氣體1.12L(標準狀況,忽略N2O4),則反應中消耗HNO3的物質的量為
A. 1molB. 0.05molC. 1.05molD. 0.11mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組研究溶液中AgNO3和Na2S的反應。
實驗 | 試劑 | 現象 | |
| 試管 | 滴管 | |
(pH = 4) |
(pH = 9) | 出現黑色沉淀 | |
(1)用離子方程式解釋Na2S溶液pH > 7的原因:________。
(2)實驗小組同學認為黑色沉淀中可能含有Ag2O、Ag2S或Ag,設計實驗驗證。
已知:i.濃硝酸能將Ag2S轉化為![]() 和
和![]() ;
;
ii.Ag2O能溶解在濃氨水中形成銀氨溶液,而Ag2S和Ag均不能。
① 設計并實施如下實驗,證實沉淀中含有Ag2S。

試劑1和試劑2分別是_________、_________。
現象1和現象2分別是_________、_________。
② 設計并實施如下實驗,證實沉淀中不含有Ag2O,將實驗操作和現象補充完整。
實驗操作 | 實驗現象 | |
步驟i | 取少量銀氨溶液,向其中滴加鹽酸 | 出現白色沉淀 |
步驟ii | 取少量洗滌后的黑色沉淀,____________ | ____________ |
③ 經檢驗,沉淀不含有Ag。

(3)實驗小組同學認為AgNO3溶液具有氧化性,在一定條件下能夠氧化Na2S,設計實驗進行研究(實驗裝置如右圖所示),測得電壓為a(![]() )。
)。
對AgNO3溶液中氧化![]() 的物質進行推測:
的物質進行推測:
假設1: ![]() 的AgNO3溶液中
的AgNO3溶液中![]() 氧化了
氧化了![]() ;
;
假設2: ![]() 的AgNO3溶液中
的AgNO3溶液中![]() 氧化了
氧化了![]() 。
。
利用右圖裝置繼續研究(已知:電壓大小反映了物質氧化還原性強弱的差異;物質氧化性與還原性強弱差異越大,電壓越大)。
① 將![]() 的AgNO3溶液替換為_______溶液,記錄電壓為b(
的AgNO3溶液替換為_______溶液,記錄電壓為b(![]() )。
)。
② 上述實驗證實了氧化![]() 的物質中一定包含
的物質中一定包含![]() ,其證據是______。
,其證據是______。
實驗結論:AgNO3溶液與Na2S溶液的反應類型與反應條件有關。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組擬取苦鹵的濃縮液(富含K+、Mg2+、Br-、SO42-、Cl-等)來制取較純凈的氯化鉀晶體及液溴,設計了如下流程:
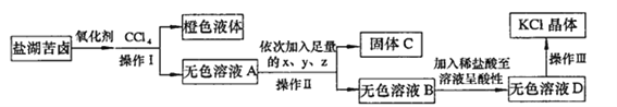
回答以下問題:
(1)操作I的名稱是__________________。從橙色液體中分離出溴,所采取的操作需要的主要玻璃儀器除酒精燈、溫度計、錐形瓶外,還需要
_________________________。
(2)試劑z的化學式為_____________;檢驗SO42-已除盡的方法是_____________________________。
(3)無色溶液B中加入稀鹽酸至溶液呈酸性,發生反應的離子方程式為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在離子 RO3n 中, 共有 x 個核外電子,R 原子的質量數為 A,則 R 原子核內含有的中子數目是( )
A. A-x+n+24 B. A-x+n+48
C. A-x-n-24 D. A+x-n-24
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示為元素周期表的一部分,其中X、Y、Z、W為四種短周期元素。Z元素原子核外K層與M層上的電子數相等,W元素的主族序數和周期數相同。下列說法中正確的是( )
![]()
A. Y元素的最高價氧化物對應的水化物的化學式為H3YO4
B. Y的最簡單氣態氫化物的水溶液顯弱堿性
C. 原子半徑由小到大的順序為X<Z<Y<W
D. X、Z兩種元素的氧化物中所含化學鍵的類型相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物的結構簡式如圖所示,下列說法正確的是( )

A. 1mol該物質可以和4molNaOH反應
B. 分子中含有六種官能團
C. 可發生加成反應、中和反應、水解反應、酯化反應、氧化反應和消去反應
D. 在水溶液中該有機物中的羥基和羧基均能電離出氫離子
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com