
分析 (1)降低溫度,平衡逆移,Cl2的轉化率減小;v正減小;
(2)保持容器體積不變,加入He,對反應無影響,所以HCl的物質的量不變;
(3)保持容器壓強不變,加入He,體積變大,反應物所占分壓減小,平衡正移,則O2的體積分數增大;
(4)若溫度和體積不變,反應從Cl2和H2O開始至平衡,在這個變化過程中,容器的體積不變,氣體的總質量也不變,氣體總物質的量增大,所以相對分子質量減小;
(5)加入催化劑,影響化學反應速率但不影響化學平衡,所以O2的物質的量不變.
解答 解:(1)該反應的正方向為吸熱反應,所以降低溫度,平衡逆移,Cl2的轉化率 減小;v正減小;故答案為:減小;減小;
(2)保持容器體積不變,加入He,容器體積不變,各物質的濃度不變,所以對反應無影響,所以HCl的物質的量不變,故答案為:不變;
(3)保持容器壓強不變,加入He,體積變大,反應物所占分壓減小,平衡正移,則O2的體積分數增大;故答案為:增大;
(4)若溫度和體積不變,反應從Cl2和H2O開始至平衡,在這個變化過程中,容器的體積不變,氣體的總質量也不變,$\overline{M}$=$\frac{m}{n}$,氣體總物質的量增大,所以相對分子質量減小;
故答案為:減小;
(5)加入催化劑,影響化學反應速率但不影響化學平衡,所以O2的物質的量不變,故答案為:不變.
點評 本題考查了溫度、壓強對化學平衡的影響,注意平衡移動對總物質的量、平均分子量的影響,掌握基礎是關鍵,題目較簡單.


科目:高中化學 來源: 題型:選擇題
| A. | CH2=CH2+Br2 | B. | CH2=CH-CH2-CH3+HCl | ||
| C. | CH3-CH=CH2+H2O | D. | nCH2=CH-CH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
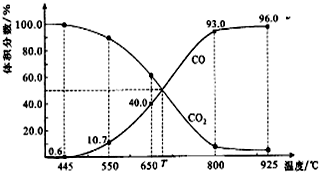
| A. | 550℃時,若充入惰性氣體,v正,v逆均減小,平衡不移動 | |
| B. | 650℃時,反應達平衡后CO2的轉化率為25.0% | |
| C. | T℃時,若充入等體積的CO2和CO,平衡向逆反應方向移動 | |
| D. | 該反應為吸熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 請回答下列問題:
請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
| X | Y | ||
| Z | W | M |
 ;
; ;
;查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com