
 .
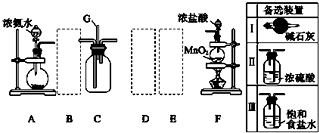
. 分析 (1)二氧化錳在加熱條件下能夠氧化濃鹽酸反應生成氯氣、氯化錳和水;
(2)濃氨水具有揮發性,生石灰或固體氫氧化鈉或者堿石灰混合能夠得到氨氣;
(3)氨氣為堿性氣體,應選擇堿性干燥劑;從F中制取的氯氣中含有氯化氫、水,氯氣在飽和食鹽水中溶解度不大,氯化氫易溶于水,選用飽和食鹽水除去氯化氫,氯氣能夠與堿反應,應選擇酸性干燥劑;
(4)依據氯氣密度大于空氣,氨氣密度小于空氣,要使二者充分混合,應讓氨氣通入到瓶底部,讓氯氣通入到瓶上;
(5)氯氣與氨氣發生氧化還原反應生成氮氣和氯化氫,氨氣和氯化氫氣體反應生成白煙氯化銨,依據得失電子守恒規律計算氧化劑與還原劑的物質的量之比;
根據公式n=$\frac{N}{{N}_{A}}$來計算阿伏加德羅數常數;
(6)氨氣極易溶于水,可以用水吸收,氯氣能夠與氫氧化鈉溶于反應,用氫氧化鈉吸收過量氯氣.
解答 解:(1)二氧化錳與濃鹽酸反應生成氯氣、氯化錳和水,離子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
故答案為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)由圖可知,為固體與液體不加熱裝置,則為濃氨水與生石灰或固體氫氧化鈉、堿石灰混合得到氨氣,
故可選用的試劑為:生石灰或固體氫氧化鈉、堿石灰;
故選:ABE;
(3)氨氣為堿性氣體,要除去氨氣中的水,應選擇堿石灰做干燥劑,選用裝置Ⅰ;
從F中制取才氯氣含有氯化氫,水,依次通過盛有飽和食鹽水、濃硫酸的洗氣瓶分別除去氯化氫和水,應選擇裝置為:Ⅱ,Ⅲ;
故答案為:Ⅰ,Ⅱ,Ⅲ;
(4)氨氣密度比氯氣的小,通入C裝置的兩根導管左邊較長(導氨氣)、右邊較短(導氯氣),可以保證二者充分混合,
故答案為:使密度較大的Cl2和密度較小的NH3較快地混合均勻;
(5)過量的氯氣可以和氨氣之間反應生成氮氣和氯化銨,即3Cl2+8NH3═N2+6NH4Cl;
反應中3mol氯氣全部被還原,8mol氯氣中只有2mol氨氣中的氮元素化合價升高,被氧化,所以:氧化劑與還原劑的物質的量之比:3:2;
由反應方程式可知Cl2→2NH4Cl,化合價降低得到2個電子,所以1molCl2的2mol電子,所以當有a mol氯氣參加反應時,轉移的電子的物質的量為2amol,已知轉移的電子總數為b個,則N=n•NA,即b=2a•NA,所以NA=$\frac{b}{2a}$,故答案為:8NH3+3Cl2═6NH4Cl+N2;3:2;$\frac{b}{2a}$;
(6)從G中逸出的氣體中含有NH3或Cl2,均可用NaOH溶液吸收,為了防止倒吸,要用倒扣的漏斗,
故答案為:在G連接導管,直接把尾氣通往盛有NaOH溶液的燒杯中.
點評 本題考查了氯氣、氨氣的實驗室制備及性質檢驗,把握實驗裝置的作用、物質的性質為解答的關鍵,題目難度中等.


 天天練口算系列答案
天天練口算系列答案科目:高中化學 來源: 題型:選擇題
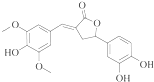
| A. | 分子中含有三種含氧官能團 | |
| B. | 1 mol該化合物最多能與6molNaOH反應 | |
| C. | 既可以發生取代反應,又能夠發生加成反應 | |
| D. | 既能與FeC13發生顯色反應,也能和Na2CO3反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗或實驗操作 | 現象 | 實驗結論 | |
| A | 用大理石和鹽酸反應制取CO2 氣體,立即通入一定濃度的Na2SiO3溶液中 | 出現白色沉淀 | H2CO3的酸性比H2SiO3的酸性強 |
| B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 出現白色沉淀 | 原溶液中含有SO42-、SO32-、HSO3-中的一種或幾種 |
| C | 將純Zn片與純Cu片用導線連接,浸入到稀硫酸溶液中 | Cu片表面產生大量氣泡 | 金屬性:Zn>Cu |
| D |  | 左邊棉球變為橙色,右邊棉球變為藍色 | 氧化性: Cl2>Br2>I2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
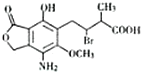 某有機物M的結構簡式如圖所示,若等物質的量的M在一定條件下分別與金屬鈉、氫氧化鈉溶液、碳酸氫鈉溶液反應,則消耗的鈉、氫氧化鈉、碳酸氫鈉的物質的量之比為( )
某有機物M的結構簡式如圖所示,若等物質的量的M在一定條件下分別與金屬鈉、氫氧化鈉溶液、碳酸氫鈉溶液反應,則消耗的鈉、氫氧化鈉、碳酸氫鈉的物質的量之比為( )| A. | 1:1:1 | B. | 2:4:1 | C. | 1:2:1 | D. | 1:2:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe(OH)3溶于氫碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | 向NaAlO2溶液中通入過量CO2制Al(OH)3:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| C. | 用Ag作電極電解硝酸銀溶液:4Ag++2H2O $\frac{\underline{\;通電\;}}{\;}$ 4Ag+O2↑+4H+ | |
| D. | 向AgCl懸濁液中加入飽和NaI溶液反應的離子方程式:AgCl+I-═AgI+Cl- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com