
【題目】其他條件不變,增大反應物的濃度能增大反應速率的原因是
A. 單位體積內分子數增多 B. 單位體積內活化分子數增多
C. 活化分子百分數增大 D. 單位體積內有效碰撞的次數增多
科目:高中化學 來源: 題型:
【題目】在溫度相同、容積均為2 L的3個恒容密閉容器中,按不同方式投入反應物,保持恒溫,測得反應達到平衡時的有關數據如下。下列說法正確的是( )
已知N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1
2NH3(g) ΔH=-92.4 kJ·mol-1
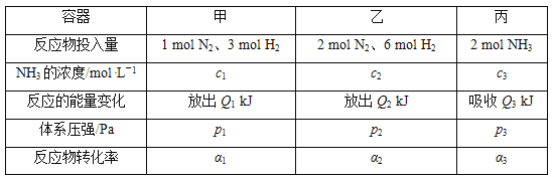
A. 2p1=2p3<p2
B. 達到平衡時丙容器中NH3的體積分數最大
C. α2+α3<1
D. Q1+Q3=92.4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機化合物M的結構簡式如下圖所示,有關該化合物的敘述正確的是( )

A. 屬于芳香烴B. 分子式為:C11H14O2
C. 最多有11個碳原子共面D. 能發生化學反應的類型只有2種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)了解用藥常識,有利于自我保健。現有下列藥物:
A.阿司匹林(乙酰水楊酸) B.青霉素 C.抗酸藥(氫氧化鋁) D.麻黃堿
①可治療支氣管哮喘,但不宜過多服用的藥物是____________。(填字母)
②治療胃酸過多,但患有嚴重的胃潰瘍,應該選擇___________。(填字母)
③一種重要的抗生素類藥,有阻止多種細菌生長的功能,該藥物是____________。(填字母)
④能使發熱的病人體溫降至正常,并起到緩解疼痛的作用,該藥物是___________。(填字母)
(2)防治環境污染,改善生態環境已成為全球的共識。
①今年入冬以來,全國多個省市出現嚴重的霧霾天氣。導致霧霾形成的主要污染物是_______(填字母)。
A.SO2 B.NO2 C.PM2.5
②垃圾應分類收集。導致“白色污染”的生活垃圾應放置于貼有________ (填字母)標志的垃圾筒內。

③工業廢水需處理達標后才能排放。下列廢水處理的方法合理的是____________。
A.用中和法除去廢水中的酸
B.用混凝劑除去廢水中的重金屬離子
C.用氯氣除去廢水中的懸浮物
(3)全世界每年因鋼鐵銹蝕造成大量的損失。某學生欲探究在蒸餾水、氯化鈉溶液和醋酸溶液三種條件下鐵銹蝕的快慢,設計了如下實驗。
實驗序號 | Ⅰ | Ⅱ | Ⅲ |
實驗內容 |
|
|
|
請回答:
①在一周的觀察過程中,他發現實驗序號為______的試管中鐵釘銹蝕速度最慢。
②下列防止鋼鐵銹蝕的措施不合理的是__________(填字母)。
A.在自行車的鋼圈表面鍍鎳
B.在地下鋼鐵管道上連接銅塊
C.改變金屬內部結構制成不銹鋼
③炒過菜的鐵鍋未及時洗凈(殘液中含NaCl),第二天便會因腐蝕出現紅褐色銹斑。試回答:鐵鍋的腐蝕主要是由__________________腐蝕造成的。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化碳的捕集、利用是我國能源領域的一個重要戰略方向。
(1)科學家提出由CO2制取C的太陽能工藝如圖所示。

①若“重整系統”發生的反應中n(FeO)/n(CO2)=6,則FexOy的化學式為____________。
②“熱分解系統”中每分解1mol FexOy,轉移電子的物質的量為________。
(2)工業上用CO2和H2反應合成二甲醚。已知:CO2(g)+ 3H2(g)═CH3OH(g)+ H2O(g) △H1=-53.7kJ/mol,CH3OCH3(g)+H2O(g) ═ 2CH3OH(g) △H2=+23.4kJ/mol,則2CO2(g)+ 6H2(g)![]() CH3OCH3(g)+3H2O(g) △H3=______kJ/mol。
CH3OCH3(g)+3H2O(g) △H3=______kJ/mol。
①一定條件下,上述合成甲醚的反應達到平衡狀態后,若改變反應的某一個條件,下列變化能說明平衡一定向正反應方向移動的是_____(填代號)。
a.逆反應速率先增大后減小 b.H2的轉化率增大
c.反應物的體積百分含量減小 d.容器中的nCO2/nH2值變小
②在某壓強下,合成甲醚的反應在不同溫度、不同投料比時,CO2的轉化率如圖所示。T1溫度下,將6 mol CO2和12molH2充入2L的密閉容器中,5 min后反應達到平衡狀態,則0~5min內的平均反應速率v(CH3OCH3) =___;KA、KB、KC三者之間的大小關系為_____。
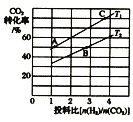
(3)常溫下,用氨水吸收CO2可得到NH4HCO3溶液,在NH4HCO3溶液中:c (NH4+)_____c(HCO3-)(填“>”、“<”或“=”);反應NH4++HCO3-+H2O![]() NH3·H2O+H2CO3的平衡常數K=__________________。(已知常溫下NH3·H2O的電離平衡常數Kb=2×10-5,H2CO3的電離平衡常數K1=4×10-7mol·L-1,K2=4×10-11mol·L-1)
NH3·H2O+H2CO3的平衡常數K=__________________。(已知常溫下NH3·H2O的電離平衡常數Kb=2×10-5,H2CO3的電離平衡常數K1=4×10-7mol·L-1,K2=4×10-11mol·L-1)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】管道工人曾經用濃氨水檢查氯氣管道是否漏氣。已知能發生如下反應(在有水蒸氣存在的條件下):2NH3+3Cl2=6HCl+N2。下列說法錯誤的是( )
A.若管道漏氣,遇氨就會產生白煙
B.該反應屬于復分解反應
C.該反應屬于氧化還原反應
D.該反應中Cl2是氧化劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知斷開1molH-H鍵吸收的能量為436KJ,形成1molH-N鍵放出的能量為391KJ,根據化學方程式N2+3H2![]() 2NH3,反應完1molN2放出的能量為924KJ,則斷開1molN≡N鍵吸收的能量是
2NH3,反應完1molN2放出的能量為924KJ,則斷開1molN≡N鍵吸收的能量是
A.431KJ B.649KJ C.869KJ D.945.6KJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉膠體,選擇適當的試劑和方法從中提純出NaCl晶體。相應的實驗過程如圖:
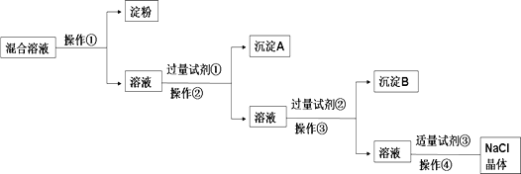
(1)寫出上述實驗過程中所用試劑:試劑①____;試劑③____。
(2)判斷試劑①已過量的方法是:_____。
(3)操作①是利用半透膜進行分離提純,操作①的實驗結果:淀粉___(填“能”或“不能”)透過半透膜。
(4)操作④的名稱是____,其中玻璃棒的作用是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA表示阿伏加德羅常數的數值。下列的說法中,正確的是( )
A. 4.6g金屬鈉由原子完全變為Na+ 離子時,失去的電子數為0.1NA
B. NA 個氧氣分子與NA 個氫氣分子的質量比為8︰1
C. 0.2 NA個硫酸分子與19.6g磷酸(相對分子質量:98)含有相同的氧原子數
D. 22.4L的氮氣所含有的原子數為2NA
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com