
【題目】化合物F是從我國特產植物中提取的一種生物堿,其人工合成路線如圖:
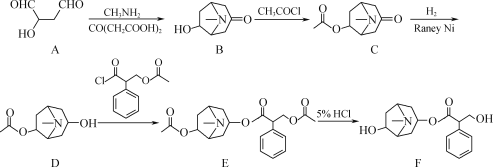
(1)A中含氧官能團的名稱為___和___。
(2)C→D的反應類型為___。
(3)E→F的過程中,會有副產物X(分子式為C8H15NO2)生成,寫出X的結構簡式:___。
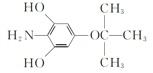
(4)C的一種同分異構體同時滿足下列條件,寫出該同分異構體的結構簡式:__。
①分子中有醚鍵;
②能與FeCl3溶液發生顯色反應,能與鹽酸反應;
③有4種不同化學環境的氫且數目比為9∶2∶2∶2。
(5)已知:R—O—R′+2HBr![]() R—Br+R′—Br十H2O(R、R′表示烴基)。
R—Br+R′—Br十H2O(R、R′表示烴基)。
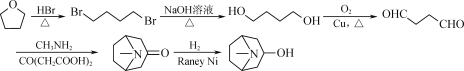
寫出以![]() 、CH3NH2和CO(CH2COOH)2為原料制備
、CH3NH2和CO(CH2COOH)2為原料制備![]() 的合成路線流程圖___(無機試劑任用,合成路線流程圖示例見本題題干)。
的合成路線流程圖___(無機試劑任用,合成路線流程圖示例見本題題干)。
【答案】羥基 醛基 還原反應 ![]()
 或
或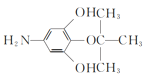
【解析】
化合物A(![]() )與CH3NH2、CO(CH2COOH)2反應生成化合物B(
)與CH3NH2、CO(CH2COOH)2反應生成化合物B(![]() ),B的羥基H與CH3COCl的酰氯發生取代,生成C(
),B的羥基H與CH3COCl的酰氯發生取代,生成C(![]() ),C的羰基在RaneyNi的催化下加H2還原,生成D(
),C的羰基在RaneyNi的催化下加H2還原,生成D(![]() ),D的羥基H與
),D的羥基H與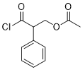 的酰氯發生取代,生成E(
的酰氯發生取代,生成E(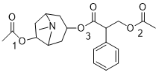 ),E的左邊(1號位)和右邊(2號位)的兩個酯基在HCl的作用下水解得到最終產物F。
),E的左邊(1號位)和右邊(2號位)的兩個酯基在HCl的作用下水解得到最終產物F。
(1)A中有一個羥基,兩個醛基,故含氧官能團為羥基和醛基;
(2)有機化學中加氫或去氧的反應叫做還原反應,故C→D的反應類型為加成反應;
(3)E→F的過程中,由于反應條件是酯基水解的條件,化合物E(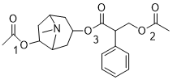 )中間(3處)的酯基也可能水解,生成
)中間(3處)的酯基也可能水解,生成![]() ;
;
(4)①分子中有醚鍵,說明分子中有-O-;
②能與FeCl3溶液發生顯色反應,說明有酚羥基,即有苯環;能與鹽酸反應說明分子中有氨基(-NH2);
③只有4種不同化學環境的氫,說明該分子對稱性較強,數目比為9∶2∶2∶2說明該分子四種環境的氫分別為9、2、2、2。9個相同的氫,說明分子中有三個-CH3,三個2分別是-NH2的氫,苯環的氫和兩個酚-OH的氫;
綜上所述,結構簡式為 或
或 ;
;
(5)可以根據逆向合成法推理,根據題目的流程,要想得到![]() ,可以由
,可以由![]() 與H2反應制得,
與H2反應制得,![]() 可以由流程中的第一步的方法合成,用
可以由流程中的第一步的方法合成,用![]() 、CH3NH2、CO(CH2COOH)2三者反應制得,
、CH3NH2、CO(CH2COOH)2三者反應制得,![]() 由
由![]() 催化氧化制得,
催化氧化制得,![]() 由
由![]() 水解制得,
水解制得,![]() 可根據已知的提示,由
可根據已知的提示,由![]() 與HBr反應制得,流程為:
與HBr反應制得,流程為: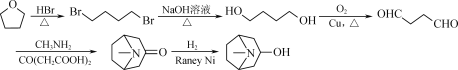


 中考利劍中考試卷匯編系列答案
中考利劍中考試卷匯編系列答案 教育世家狀元卷系列答案
教育世家狀元卷系列答案 黃岡課堂作業本系列答案
黃岡課堂作業本系列答案 單元加期末復習先鋒大考卷系列答案
單元加期末復習先鋒大考卷系列答案科目:高中化學 來源: 題型:
【題目】25℃時,向25 mL 0.100 0 mol L-l的BOH溶液中逐滴滴入同濃度的一元弱酸HA的溶液,所得溶液PH與加入HA溶液的體積的關系曲線如圖所示,則下列說法正確的是( )
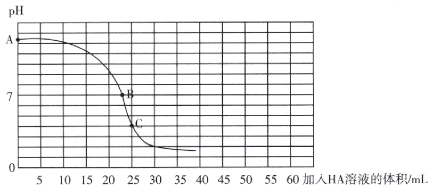
A.BOH的電離方程式為BOH =B++OH-
B.可選擇酚酞作指示劑,滴定終點時,溶液恰好在B點從無色變為粉紅色,且30秒內不恢復原色
C.Ka(HA)<Kb(BOH)
D.加入HA溶液的體積為50 ml時,c(B+)+2c(BOH)+c(OH-)=c(HA)+c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.下圖所示是實驗中常用的幾種儀器,請根據要求填空。
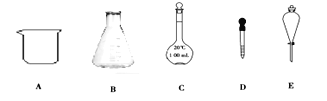
(1)在上述五種儀器中,配制一定物質的量濃度的溶液實驗中需要使用哪些儀器:________(填序號),不需要使用的儀器是:_______(填名稱)。
(2)下列關于儀器C的使用方法中,正確的是________(填下列選項的編號)。
a.使用前應檢查是否漏液 b.使用前必須烘干
c.不能用作物質反應或溶解的容器 d.熱溶液可直接轉移到其中
Ⅱ.實驗室要配制90 mL 0.100 mol·L-1 Na2CO3溶液,請回答下列問題:
(1)配制過程中需要用到的儀器除托盤天平(帶砝碼,精確度0.1g)、膠頭滴管、量筒、藥匙、燒杯外,還需要的儀器有:________________。
(2)若用Na2CO3·10H2O來配制溶液,需要稱量晶體的質量為________g。
(3)經查閱資料知,碳酸鈉固體與NaOH相似,在空氣中要潮解,在稱量時,需要注意選擇用___________盛裝Na2CO3固體。
(4)在配制過程中,下列情況會引起誤差偏高的是___________。
a.晶體失去了部分結晶水
b.定容時仰視刻度線
c.未冷卻至室溫就將溶液轉移到容量瓶并定容
d.定容后塞上瓶塞倒轉搖勻,靜置后,液面低于刻度線,再加水至刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)在一固定容積的密閉容器中進行如下反應:CO2(g)+H2(g)![]() CO(g)+H2O(g),其平衡常數K和溫度T的關系如下:
CO(g)+H2O(g),其平衡常數K和溫度T的關系如下:
T/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
①K的表達式為____________________;
②該反應的正反應為__________反應(“吸熱”或“放熱”);
③下列選項中,能判斷該反應已經達到化學平衡狀態的是____________(填字母代號)。
A.容器中壓強不變 B.混合氣體中CO濃度不變
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(2)下列化合物:①HCl ②NaOH ③CH3COOH ④NH3·H2O ⑤CH3COONa ⑥NH4Cl,溶液呈堿性的有__________(填序號);常溫下0.01 mol/L HCl溶液的pH=________;pH=11的CH3COONa溶液中由水電離產生的c(OH-)=________。
(3)已知在Cu2+、Mg2+、Fe2+濃度相同的溶液中,其開始沉淀時的pH如下:
離子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
①若向該溶液中滴加NaOH溶液,則先沉淀的是 ____________(填離子符號);
②判斷Ksp[Mg(OH)2]____________Ksp[Fe(OH)2](填“>”、“=”或“<”)。
(4)電解裝置如圖所示:
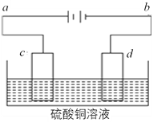
①當用惰性電極電解時,d電極的反應式為____________;
②若用此裝置進行鐵上鍍銅,已知鍍層金屬采用純銅且電鍍前兩電極材料質量相等,電鍍一段時間后對電極進行稱量發現兩極質量差為16 g,則電路中轉移的電子為____________mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從樟科植物枝葉提取的精油中含有下列甲、乙、丙三種成分:


(1)寫出物質甲中含氧官能團的名稱:________________________。
(2)由甲轉化為乙需經下列過程(已略去各步反應的無關產物,下同):

其中反應Ⅰ的反應類型為_____________,反應Ⅱ的化學方程式為____________(注明反應條件)。
(3)已知:RCH===CHR′![]() RCHO+R′CHO;
RCHO+R′CHO;
2HCHO![]() HCOOH+CH3OH
HCOOH+CH3OH
由乙制丙的一種合成路線圖如下(A~F均為有機物,圖中Mr表示相對分子質量):

①物質B化學名稱為________________,下列物質能與C反應的是________(選填序號)。
a.銀氨溶液 b.溴水 c.Na2CO3溶液 d.酸性KMnO4溶液
②寫出E→F化學方程式_______________________________________________。
③D的同分異構體中同時滿足下列要求的有________種。
a.遇FeCl3溶液顯示特征顏色
b.1molD能與2molNaOH溶液反應
c.核磁共振氫譜圖中有四個峰,峰面積之比為3:2:2:1
④綜上分析,丙的結構簡式為__________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NaClO溶液是一種紡織工業用漂白劑,可用一定比例NaOH、Na2CO3的混合溶液和Cl2反應制備。
(1)NaHCO3的存在能增強NaClO溶液的穩定性。Cl2與混合溶液中Na2CO3反應制備NaClO,同時生成NaHCO3,其化學方程式為___。
(2)NaClO溶液中若含有NaClO3會影響產品的品質。測定堿性NaClO樣品中NaClO3物質的量濃度的方法如下:取20.00mLNaClO溶液試樣,加入過量H2O2,充分反應后,加熱煮沸,冷卻至室溫,加入硫酸酸化,再加入0.1000mol·L-1FeSO4標準溶液30.00mL,充分反應后,用0.01000mol·L-1酸性K2Cr2O7溶液滴定過量的FeSO4溶液至終點(Cr2O72-被還原為Cr3+),消耗該溶液25.00mL。
已知:ClO3-在堿性條件下性質穩定,在酸性條件下表現出強氧化性;ClO3-+Fe2++H+—Cl-+Fe3++H2O(未配平)。
①加入過量H2O2的目的是__。
②實驗中若缺少加熱煮沸步驟,所測NaClO3物質的量濃度會有較大誤差,原因可能是___(答出一個即可)。
③計算樣品中NaClO3物質的量濃度___(寫出計算過程)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2.0mol PC13和1.0mol Cl2充入體積不變的密閉容器中,在一定條件下發生下述反應: PCl3(g)+Cl2(g) ![]() PCl5(g)達平衡時,PCl5為0.40mol,如果此時移走1.0mol PCl3和0.5mol Cl2,在相同溫度下再達平衡時PCl3的物質的量是
PCl5(g)達平衡時,PCl5為0.40mol,如果此時移走1.0mol PCl3和0.5mol Cl2,在相同溫度下再達平衡時PCl3的物質的量是
A.0.40molB.0.20mol
C.大于0.80mol,小于1.6molD.小于0.80mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化碳的捕集和轉化是科學研究中的熱點問題。我國科研人員提出了以Ni/Al2O3為催化劑,由 CO2(g)和H2(g)轉化為CH4(g)和H2O(g)的反應歷程,其示意圖如下:
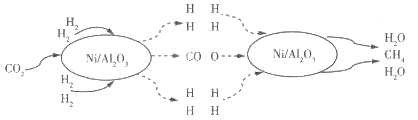
(1)該可逆反應的化學方程式為_________。使用催化劑Ni/Al2O3_________ (填“能”或“不能”)提髙CO2的平衡轉化率。
(2)300℃下,在一恒容密閉容器中充入一定量的CO2與H2,發生上述反應,一段時間后反應達平衡,若其他條件不變,溫度從300℃升至500℃,反應重新達到平衡時,H2的體積分數增加。下列說法錯誤的是_________(填標號)。
A.該反應的![]()
B.平衡常數大小:![]()
C.300℃下,減小![]() 的值,
的值,![]() 的平衡轉化率升高
的平衡轉化率升高
D.反應達到平衡時化![]()
(3)在一定條件下,反應體系中CO2的平衡轉化率a( CO2)與L和X的關系如圖所示,L和X表示溫度或壓強。
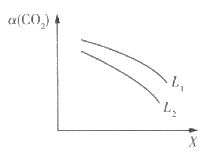
①X表示的物理量是___________。
②L1_____________L2(填“<”“>”),判斷理由是______________________________________。
(4)向1 L恒容密閉容器中加入4.0 mol H2(g),1.0 mol CO2,控制條件(催化劑為 Ni/AI2O3、溫度為T1)使之發生上述反應,測得容器內氣體的壓強隨時間的變化如圖所示。
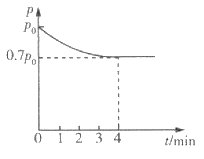
①4 min時CO2的轉化率為___________。
②T1溫度下該反應的化學平衡常數為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】五種短周期元素在周期表中的位置如圖所示,其中R元素原子的最外層電子數等于其電子層數的2倍,下列判斷正確的是
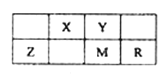
A. 元素的非金屬性次序為:Y>X>M
B. 氣態氫化物穩定性:M>R
C. Z的氧化物可以做光導纖維
D. 最D高價氧化物對應水化物的酸性:Y>X
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com