
【題目】某同學在研究Fe與H2SO4的反應時,進行了如下實驗。
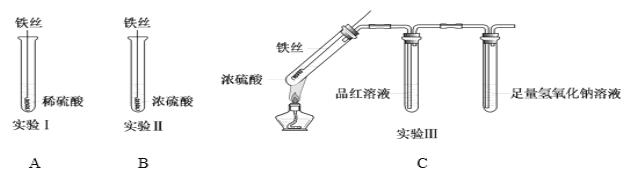
(1)實驗Ⅰ中,鐵與稀硫酸反應的離子方程式為__________________________________。
(2)實驗Ⅱ中,鐵絲表面迅速變黑,反應很快停止,其原因是________________________________。
(3)實驗Ⅲ中,加熱后產生大量氣體,中間試管中品紅溶液的紅色褪去,最終未檢測到可燃性氣體。最后裝NaOH溶液試管中反應的離子方程式是_________________________________。
(4)對比實驗Ⅰ、Ⅱ和Ⅲ,同學們得出以下結論:
①濃硫酸和稀硫酸都具有氧化性,但原因不同。濃硫酸的氧化性源于+6價的硫元素,稀硫酸的氧化性源于______。
②造成反應多樣性的主要因素有________________________。
【答案】Fe+2H+=Fe2++H2↑ 鐵表面生成致密的氧化膜,阻止反應進一步進行 SO2+2OH—=SO32-+H2O +1價的氫元素 反應物的濃度、溫度
【解析】
(1)Fe和稀硫酸反應生成硫酸亞鐵和氫氣;
(2)濃硫酸具有強氧化性,發生鈍化;
(3)產生氣體使品紅褪色和D處始終未檢測到可燃性氣體進行分析;
(4)①濃硫酸和稀硫酸都具有氧化性,但原因不同,濃硫酸的氧化性表現在+6價的硫元素上,稀硫酸的氧化性表現在+1價的氫元素上;
②影響反應產物多樣性的因素有濃度、溫度、反應物的量等.
(1)Fe和稀硫酸反應生成硫酸亞鐵和氫氣,離子方程式為Fe+2H+=Fe2++H2↑;
正確答案:Fe+2H+=Fe2++H2↑;
(2)濃硫酸具有強氧化性,生成致密的氧化膜覆蓋在Fe的表面,發生鈍化;
正確答案:鐵表面生成致密的氧化膜,阻止反應進一步進行;
(3)產生氣體使品紅褪色和D處始終未檢測到可燃性氣體可推斷A中產生的氣體為SO2,裝置C的作用是吸收SO2防止污染環境;
正確答案:SO2+2OH—= SO32-+H2O
(4①濃硫酸和稀硫酸都具有氧化性,但原因不同,濃硫酸的氧化性表現在+6價的硫元素上,稀硫酸的氧化性表現在+1價的氫(H+)元素上,
正確答案:+1價的氫元素;
②影響反應產物多樣性的因素有濃度、溫度、反應物的量等
正確答案:反應物的濃度、溫度。


科目:高中化學 來源: 題型:
【題目】下圖是周期表中短周期的一部分,A、B、C三種元素的原子核外電子數之和等于B的質量數,B元素的原子核內質子數等于中子數,下列敘述正確的是( )

A. B為第二周期的元素
B. C為VA族元素
C. 三種元素都為非金屬元素
D. B是三者中化學性質最活潑的非金屬
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中正確的是( )
A. 用鼻子對著盛有氯氣的瓶口,就可以嗅到氯氣的氣味 B. 氯氣有漂白性
C. 用排水集氣法便可以收集到純凈的氯氣 D. 自來水常用氯氣來殺菌、消毒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向20 mL 0.1mol/L的K2CO3溶液中逐滴加入0.1mol/L的稀鹽酸40mL,溶液中含碳元素的各種微粒(CO2因逸出未畫出)的物質的量分數隨溶液pH變化的情況如下圖所示。下列說法正確的是
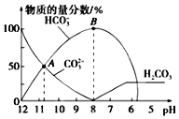
A. 隨著稀鹽酸的加入,溶液中c(HCO3-)·c(OH-)/c(CO32-)保持不變
B. 根據A點計算,Ka2(H2CO3)的數量級為10-3
C. B點所處的溶液中:c(K+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
D. 當pH約為8時,溶液中開始放出CO2氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】-Fe2O3是一種具有磁性、催化等作用的納米材料,以硫鐵礦燒渣等為原料生產制備-Fe2O3的流程如下:
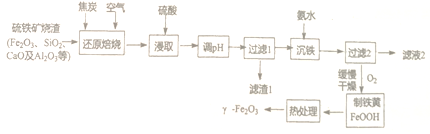
已知:“還原焙燒”的主要反應為:3C+2O2![]() 3CO↑+CO2↑,Fe2O3+CO
3CO↑+CO2↑,Fe2O3+CO![]() 2FeO + CO2
2FeO + CO2
回答下列問題:
(1)“浸取”前需將焙燒生成的混合物粉碎,其目的是_____________________。
(2)“濾渣1”除了CaSO4外還有_______________。
(3)常溫下Ksp[Al(OH)3]=1.3×10-33。當常溫下溶液pH=6時,c(Al3+)=____________。
(4)“過濾2”時需用蒸餾水洗滌,能證明己洗滌干凈的方法是______________;
(5)沉淀緩慢氧化為鐵黃的化學方程式為_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將鈉放入盛有空氣的密閉容器中,生成Na2O還是Na2O2是由下列哪項因素所決定的( )
A.反應溫度B.空氣的量C.鈉粒的大小D.鈉的狀態(s、l)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,將Cl2通入NaOH溶液中,反應得到NaCl、NaClO、NaClO3的混合溶液,經測定ClO-與ClO3-的物質的量濃度之比為1∶3,則此反應中氧化劑與還原劑的物質的量之比是( )
A.21∶5B.11∶3C.4∶1D.1∶4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物G(分子式為C13H18O2)是一種香料,如圖是該香料的一種合成路線。

已知:
①E能發生銀鏡反應,在一定條件下,1 mol E能與2 mol H2反應生成F;
②R—CH===CH2![]() R—CH2CH2OH;
R—CH2CH2OH;
③有機物D的摩爾質量為88 g·mol-1,其核磁共振氫譜有3組峰;
④有機物F是苯甲醇的同系物,苯環上只有一個無支鏈的側鏈。
回答下列問題:
(1)用系統命名法命名有機物B________________;
(2)E的結構簡式為__________________________;
(3)C與新制Cu(OH)2反應的化學方程式為____________________________;
(4)已知有機物甲符合下列條件:①為芳香族化合物;②與F互為同分異構體;③能被催化氧化成醛。符合上述條件的有機物甲有________種,寫出一種滿足苯環上有3個側鏈,且核磁共振氫譜有5組峰,峰面積比為6∶2∶2∶1∶1的有機物的結構簡式____________________;
(5)以丙烯等為原料合成D的路線如下:

X的結構簡式為_______,步驟Ⅱ的反應條件為___________,步驟Ⅳ的反應類型為______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com