
【題目】【化學―選修2:化學與技術】以硫鐵礦(主要成分為FeS2)為原料制取硫酸,其礦渣可用來煉鐵。生產工藝示意圖如下:
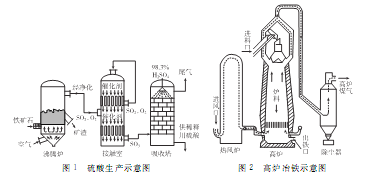
(1)配平煅燒硫鐵礦的反應方程式:______FeS2+________O2→_____Fe2O3+______SO2。實際生產中向沸騰爐通入的空氣量要大于鍛燒硫鐵礦所需空氣量.其目的是____________________。接觸室和熱風爐中都裝有熱交換器,可用反應的余熱將通入的氣體加熱,這樣做的好處是_____________________。
(2)生產硫酸時,吸收塔中用98.3%的硫酸吸收而不用水吸收SO3的原因是______________。用含FeS280%的硫鐵礦生產硫酸,如果煅燒時有5%的硫損失,SO2轉變成SO3的轉化率為80%,那么生產98%的濃硫酸3噸,則需要這種硫鐵礦___________噸。
(3)CO還原Fe2O3的冶鐵過程中,反應物、生成物和溫度之間的關系如圖所示.
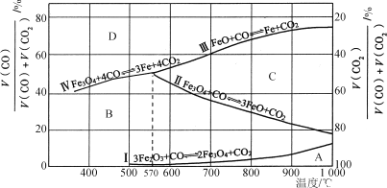
(圖中Ⅰ、Ⅱ、Ⅲ、Ⅳ四條曲線是四個化學反應平衡時的氣相組成對溫度作圖得到的;A、B、C、D四個區域分別是Fe2O3、Fe3O4、FeO、Fe穩定存在的區域)
①冶煉高爐產生的高爐煤氣的主要成分有__________和剩余的CO。
②據圖分析,下列說法正確的是________(填字母)。
a.溫度低于570 ℃時,Fe2O3還原焙燒的產物中不含FeO
b.溫度越高,Fe2O3還原焙燒得到的固體物質組成中Fe元素的質量分數越高
c.Fe2O3還原焙燒過程中及時除去CO2有利于提高Fe的產率
③800℃時,混合氣體中CO2體積分數為40%時,Fe2O3用CO還原焙燒反應的化學方程式為____________。
【答案】(1)4、11、2、8提高FeS2的利用率(或使FeS2充分反應,2分)充分利用反應放出的熱量,降低生產成本;
(2)防止產生酸霧,使SO3能夠被充分吸收2.96;
(3)①N2、CO2 ②ac ③Fe2O3+CO![]() 2FeO+CO2
2FeO+CO2
【解析】
試題分析:(l)FeS2中鐵元素由+2價升高到+3價,硫元素由-1價升高到+4價,FeS2共升高11價,O2共降低2×2=4價,根據電子得失守恒可配平得4FeS2+11O2![]() 2Fe2O3 +8SO2;工業生產中要考慮經濟效益,故充分利用原料和充分利用能源都能夠降低生產成本。
2Fe2O3 +8SO2;工業生產中要考慮經濟效益,故充分利用原料和充分利用能源都能夠降低生產成本。
(2)濃硫酸吸水會放出大量的熱,若用水吸收SO3會形成酸霧,降低吸收效率;根據反應前后硫元素守恒思想可列等式進行計算。設需要這種黃鐵礦的質量是x,則:
FeS2 2H2S04
120 98×2
x×80%×(1- 5%)×80% 3t×98%
所以120×3t×98%=x×80%×(1—5%)×80%×98×2,解得x=2.96(噸);
(3)①由CO還原Fe2O3的冶鐵過程的反應物、生成物關系圖可知,高爐冶鐵過程中會有CO、CO2、Fe3O4、FeO、Fe等物質生成,另外通入的空氣中的氮氣不會參加反應,所以冶煉高爐產生的高爐煤氣的主要成分有N2、CO2和剩余的CO。
②a、由圖可知,FeO在C區穩定,對應的溫度高于570℃,a正確;b、鐵元素的質量分數由高到低為:Fe>FeO>Fe304>Fe2O3,對于反應Ⅱ知,升高溫度時,C02體積分數減小,即升溫平衡逆向移動,FeO轉化成Fe3O4,鐵元素的質量分數減小,所以含量不僅與溫度有關,還與CO氣體的比例有關,b錯誤;c、分離CO2可使四個反應的平衡均正向移動,有利于Fe含量的增加,c正確。答案選ac;
③由圖可知,“800℃、CO2體積分數為40%”時,在C區,此時為FeO的穩定區域,故產物為FeO,反應的方程式是Fe2O3+CO![]() 2FeO+CO2。
2FeO+CO2。


科目:高中化學 來源: 題型:
【題目】下列表格中各項分類都正確的一組是( )
純凈物 | 混合物 | 電解質 | 非電解質 | |
A | 冰水混合物 | CuSO45H2O | 液態KNO3 | 蔗糖 |
B | CaO | 海水 | 銅 | 酒精 |
C | 液氯 | 鋁合金 | AgCl | CO2 |
D | 氫氧化鈉 | 空氣 | Na2SO4溶液 | 食醋 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從海水中提取蒸餾水、溴、食鹽過程過如下:
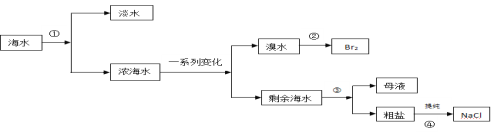
(1)從海水中獲取淡水的方法實驗操作是 ,需要的玻璃儀器有:酒精燈、溫度計、牛角管、冷凝管、 。
(2)從溴水中獲得單質溴時,采用的方法是萃取、 、蒸餾。操作是 、過濾。
下列可選作萃取劑的是
A.酒精 B.苯 C.CCl4
(3)粗鹽含有Ca2+、Mg2+、SO42-等離子,為除去以上雜質離子,可加入①Na2CO3溶液②BaCl2溶液NaOH溶液④過濾⑤稀鹽酸。錯誤的操作順序是
A.①②③④⑤ B. ②①③④⑤ C.③②①④⑤ D. ②③①④⑤
(4)實驗室用上述方法制得的NaCl配制240ml 0.1mol/LNaCl溶液。需要用托盤天平稱量NaCl固體 g。配制時,一般可分為以下幾個步驟:①稱量②計算③溶解④搖勻⑤轉移⑥洗滌⑦定容⑧冷卻。其正確的操作順序為 。
配制過程中,下列情況會使配制結果偏高的是(填序號)
①定容時俯視刻度線觀察液面
②容量瓶使用時未干燥
③定容后經振蕩、搖勻、靜置,發現液面低于刻度線,再加蒸餾水補至刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)250 mL密度為1.1 g·cm-3、質量分數為24.5%的硫酸跟鐵屑充分反應。計算生成H2的體積(標準狀況)(給出必要的計算過程)
(2)上述反應中轉移電子數目為多少?
(3)亞硝酸鈉(NaNO2)具有致癌作用,許多腌制食品中含NaNO2。酸性KMnO4溶液與亞硝酸鈉反應的離子反應為 MnO4-+NO2-+H+→Mn2+ + NO3-+H2O(未配平),下列敘述錯誤的( )
A.生成1mol Mn2+,轉移電子為5mol
B.該反應中氮元素被氧化
C.配平后,水的化學計量數為3
D.反應中氧化產物與還原產物的物質的量之比為2:5
(4)向NaOH溶液中逐漸滴入Mg(HCO3)2溶液至沉淀完全的離子方程______________
(5)現有銅片、鋅片、導線、小燈泡![]() 、電流表
、電流表![]() 、硫酸銅溶液及燒杯
、硫酸銅溶液及燒杯![]() ,設計實驗證明氧化還原反應中有電子轉移。要求畫圖表示及必要的文字說明。
,設計實驗證明氧化還原反應中有電子轉移。要求畫圖表示及必要的文字說明。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
①用托盤天平稱取3.7g食鹽
②用量筒量取8.62mL鹽酸
③用廣泛pH試紙測得溶液的pH是2.5,其中數據合理的是
A. ① B. ② C. ①③ D. ②③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家開發出一種新型鋰—氧電池,其能量密度極高,效率達90%以上。電池中添加碘化鋰(LiI)和微量水,工作原理如圖所示,總反應為:O2+4LiI+2H2O2I2+4LiOH

對于該電池的下列說法不正確的是( )
A.放電時負極上I- 被氧化
B.充電時Li+從陽極區移向陰極區
C.充電時陰極反應為LiOH+e-==Li+OH-
D.放電時正極反應為O2+2H2O+4Li++4e-==4LiOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式中,正確的是
A.氧化鐵和稀硫酸反應:Fe2O3+6H+=2Fe2++3H2O
B.鋅與鹽酸的反應:Zn+2H++2Cl-=Zn2++2Cl-+H2↑
C.石灰石與鹽酸反應:CaCO3+2H+=Ca2++CO2↑+H2O
D.NH4HCO3溶液與過量KOH濃溶液共熱:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】200 mL硝酸與一定量鋁鐵合金反應生成 3.36 L NO(標況),向反應后的溶液中加入150 mL 3 mol·L1的NaOH溶液,使鋁鐵元素恰好全部轉化為沉淀,則原硝酸的濃度是
A.3 mol·L1 B.2.25 mol·L1 C.1. 5 mol·L1 D.無法計算
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏伽德羅常數的值。下列有關敘述正確的是( )
A. 標況下,11.2L氟化氫中含有的分子數目為0.5NA
B. 室溫下,21.0g乙烯和丁烯的混合氣體中所含的碳原子數目是NA
C. 室溫下,2L 0.05mol/L的NH4NO3溶液中所含有的氮原子數目是0.2NA
D. 22.4L Cl2與足量NaOH溶液反應時轉移的電子數為NA
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com