
| A. | O2是還原劑 | B. | NH3是氧化劑 | C. | O2失去電子 | D. | NH3發生氧化反應 |
科目:高中化學 來源: 題型:選擇題
| A. | 在燒杯中溶解溶質,攪拌時不慎濺出少量溶液 | |
| B. | 未將洗滌燒杯內壁的溶液轉移入容量瓶 | |
| C. | 容量瓶中所配的溶液液面未到刻度線便停止加水 | |
| D. | 將燒杯中溶液轉移到容量瓶之前,容量瓶中有少量蒸餾水 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2SO4、BaCl2、NaNO3、NaCl | B. | AgNO3、CaCl2、KNO3、MgCl2 | ||
| C. | Na2SO4、Na2CO3、BaCl2、HCl | D. | NaOH、BaCl2、KNO3、Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | Ca(OH)2=Ca2++(OH)2 | B. | FeCl3═Fe2++3Cl | ||
| C. | H2SO4=2H++SO42- | D. | Al(SO4)3═2Al3++3SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 區分的物質 | 區分方法 |
| A | 蒸餾水和自來水 | ①蒸發 ②看顏色 |
| B | 食鹽和面堿(Na2CO3) | ①加食醋 ②加石灰水 |
| C | 黃金和黃銅(假黃金) | ①灼燒 ②測密度 |
| D | 黑醋和醬油 | ①聞氣味 ②嘗味道 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | (CN)2+CH4$\stackrel{一定條件}{→}$CH3CN+HCN | B. | (CN)2+CH2=CH2→NC-CH2-CH2-CN | ||
| C. | (CN)2+2Br${\;}^{{\;}^{-}}$→2CN-+Br2 | D. | (CN)2+2OH-→CN-+CNO-+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | AlCl3溶液與燒堿溶液反應,當n(OH-):n(Al3+)=7:2時,2Al3++7OH-=Al(OH)3↓+AlO2-+2H2O | |
| B. | 向飽和Na2CO3溶液中通入過量的CO2:CO32-+CO2+H2O=2HCO3- | |
| C. | CuCl2溶液與NaHS溶液反應,當n(CuCl2):n(NaHS)=1:2時,Cu2++2HS-=CuS↓+H2S↑ | |
| D. | Fe與稀硝酸反應,當n(Fe):n(HNO3)=1:2時,3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
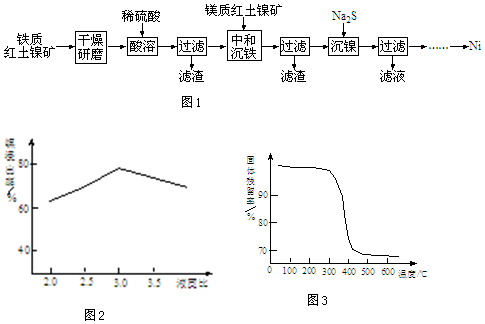
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com