


科目:高中化學 來源: 題型:
| A、整個反應階段平均速率:醋酸>鹽酸 |
| B、反應所需時間:醋酸>鹽酸 |
| C、參加反應的鋅的質量:鹽酸<醋酸 |
| D、開始反應速率:鹽酸>醋酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:
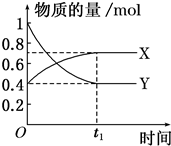
查看答案和解析>>
科目:高中化學 來源: 題型:
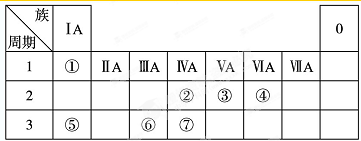
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 序號 | 氧化劑 | 還原劑 | 其他反應物 | 氧化產物 | 還原產物 |
| ① | Cl2 | FeBr2 | Cl- | ||
| ② | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| ③ | KClO3 | 濃鹽酸 | Cl2 |
| A、表中①組反應可能有一種或兩種元素被氧化 |
| B、表中②組反應的離子方程式是2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O |
| C、表中③組反應的還原產物是KCl,電子轉移數目是6e- |
| D、氧化性強弱比較:KClO3>Fe3+>Cl2>Br2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 項目 | 結果 | 正常范圍參考值 | 單位 | |
| 1 | 紅細胞計數 | 2.3 | 3.5~5 | 1×1012/L |
| 2 | 血紅蛋白 | 75 | 110~150 | g/L |
| 3 | 血小板計數 | 205.5 | 100~300 | 109/L |
| A、碘 | B、硒 | C、鐵 | D、鋅 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com