
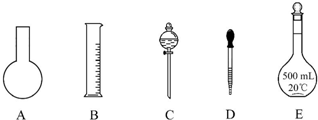
分析 (1)根據配制一定物質的量濃度溶液用到儀器選擇;根據配制溶液的體積選擇容量瓶的規格;
(2)容量瓶不能稀釋濃溶液、不能用于溶解固體、儲存溶液等,是配制一定物質的量濃度溶液的專用儀器;
(3)分析操作對溶質的物質的量和溶液體積的影響,依據C=$\frac{n}{V}$進行誤差分析;
(4)根據c=$\frac{1000ρω}{M}$計算出該濃硫酸的物質的量濃度,再根據配制過程中溶質硫酸的物質的量不變計算出需要濃硫酸的體積;依據濃硫酸稀釋的正確操作解答.
解答 解:(1)配制一定物質的量濃度溶液用的儀器有:托盤天平、藥匙、燒杯、筒量、玻璃棒、容量瓶、膠頭滴管,不需要的儀器有燒瓶和分液漏斗,要配置450ml溶液應選擇500ml容量瓶;還缺少的儀器:燒杯、玻璃棒;
故答案為:A、C; 燒杯、玻璃棒;
(2)容量瓶只能用來配制一定體積準確濃度的溶液,不能配制或測量容量瓶規格以下的任意體積的液體,不能稀釋或溶解藥品,不能用來加熱溶解固體溶質,故選BCE;
故答案為:BCE;
(3)在實驗中其他操作均正確,若定容時仰視刻度線,導致溶液體積偏大,溶液濃度偏小;
若NaOH溶液在轉移至容量瓶時未經冷卻,冷卻后,溶液體積偏小,溶液濃度偏大;
故答案為:小于;大于;
(4)分數為98%、密度為1.84g•cm-3的濃硫酸的濃度為:c=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,
配制過程中硫酸的物質的量不變,則需要該濃硫酸的體積為:$\frac{0.5mol/L×0.5L}{18.4mol/L}$=13.6mL;
濃硫酸稀釋的正確操作:將濃硫酸沿器壁緩緩倒入水中,并用玻璃棒不斷攪拌;
故答案為:13.6;將濃硫酸沿器壁緩緩倒入水中,并用玻璃棒不斷攪拌.
點評 本題考查了物質的量濃度的計算,題目難度中等,明確物質的量濃度與溶質質量分數的關系為解答關鍵,注意掌握稀釋定律在化學計算中的應用方法,試題培養了學生的化學計算能力.


科目:高中化學 來源: 題型:解答題
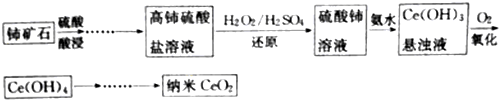
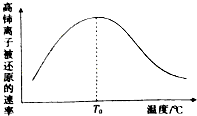
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 單質硅用于制造芯片和光導纖維 | |
| B. | 84消毒液的有效成分是NaClO | |
| C. | SO2具有漂白性,通入紫色石蕊溶液中能使溶液先變紅后褪色 | |
| D. | 普通玻璃的組成可用Na2O•CaO•6SiO2表示,是純凈物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
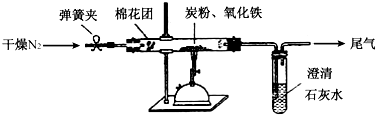
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(H+) | B. | Kb(NH3•H2O) | ||
| C. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(N{{H}_{4}}^{+})}$ | D. | c(NH4+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com