
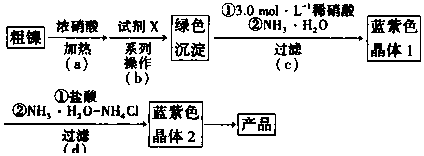
| Fe3+ | Cr3+ | Ni2+ | |
| 開始沉淀pH | 1.5 | 4.3 | 6.9 |
| 完全沉淀pH | 2.8 | 5.6 | 8.9 |
分析 由實驗流程及物質的性質可知,濃硝酸加熱后離子主要有Ni2+、Cr3+、Fe3+,再加入試劑x調節溶液的pH約為6,使Cr3+、Fe3+完全沉淀,而Ni2+未開始沉淀,過濾后再繼續加入X調節pH以得到綠色沉淀即Ni(OH)2,在加入稀硝酸、氨水,冰水浴結晶,過濾得到Ni(NH3)6(NO3)2的藍紫色晶體1,再加入鹽酸、氨水和氯化銨的混合溶液,再冰水浴結晶,過濾得到Ni(NH3)6Cl2的藍紫色晶體2,最終得到產品,據此分析;
(1)根據配制一定物質的量濃度溶液用到儀器所需要的最主要儀器來選擇;
(2)Ni和濃硝酸在加熱條件下反應生成Ni(NO3)2、NO2和H2O;
(3)①根據以上分析,加入試劑x調節溶液的pH約為6主要是除去鐵、鉻雜質;
②根據試劑x的作用調節pH值到8.9得到綠色沉淀分析;
(4)根據冰水浴環境下即降低溫度以降低產物的溶解度而析出分析;
(5)①根據滴定終點結合Ni(NH3)6Cl2+6HCl=NiCl2+6NH4Cl計算NH3的質量分數;
②適當提高稱量產品的質量,數據過大能進一步提高測定準確度,進行平行試驗取平均值能進一步提高測定準確度.
解答 解:(1)實驗需要配制3.0mol•L-1稀硝酸250mL.需要的玻璃儀器除了有燒杯、量筒、玻璃棒,膠頭滴管,還有250mL容量瓶,故答案為:250mL容量瓶;
(2)Ni和濃硝酸在加熱條件下反應生成Ni(NO3)2、NO2和H2O,化學方程式為,Ni+4(濃)HNO3$\frac{\underline{\;\;△\;\;}}{\;}$Ni(NO3)2+2NO2↑+2H2O,
故答案為:Ni+4(濃)HNO3$\frac{\underline{\;\;△\;\;}}{\;}$Ni(NO3)2+2NO2↑+2H2O;
(3)①根據以上分析,加入試劑x調節溶液的pH約為6主要是使Cr3+、Fe3+完全沉淀,而Ni2+未開始沉淀,故答案為:使Cr3+、Fe3+完全沉淀,而Ni2+未開始沉淀;
②試劑x的作用是先調節pH約為6,后又要調節pH以得到綠色沉淀即要調到8.9,所以只有NaOH符合,故選:C;
故答案為:檢驗SO42-的操作為:取少量溶液Z于試管中,然后加鹽酸,無沉淀產生,再加氯化鋇溶液,有白色沉淀產生,證明有SO42-;
(4)冰水浴環境下其作用除了可以減少氨水的揮發,還有可以降低溫度以降低產物的溶解度而析出,故答案為:降低溫度以降低產物的溶解度而析出;
(5)①根據滴定,則不加入樣品比加入mg產品多消耗氫氧化鈉為(V2-V1)×10-3×0.500mol,所以mg產品NH3的物質的量為(V2-V1)×10-3×0.500mol,則NH3的質量分數為$\frac{(V{\;}_{2}-V{\;}_{1})×10{\;}^{-3}×0.500mol×17g/mol}{mg}$×100%=$\frac{(V{\;}_{2}-V{\;}_{1})×10{\;}^{-3}×8.5}{m}$×100%,故答案為:$\frac{(V{\;}_{2}-V{\;}_{1})×10{\;}^{-3}×8.5}{m}$×100%;
②適當提高稱量產品的質量,數據過大能進一步提高測定準確度,進行平行試驗取平均值能進一步提高測定準確度,而用H2SO4溶液替代鹽酸、用酚酞替代甲基橙對實驗基本沒影響,故選:AD.
點評 本題主要考查了物質的制備及其相關組分的含量的測定等知識,較為綜合,掌握實驗方案的設計原理是解答的關鍵,題目難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KClO3在反應中得到電子 | |
| B. | ClO2中氯的化合價為+4價 | |
| C. | 在反應中H2C2O4是還原劑 | |
| D. | 1 mol KClO3參加反應有2mol電子轉移 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 人工腎臟可用間接電化學方法除去代謝產物中的尿素[CO(NH2)2],原理如圖.下列有關說法正確的是( )
人工腎臟可用間接電化學方法除去代謝產物中的尿素[CO(NH2)2],原理如圖.下列有關說法正確的是( )| A. | A為電源的負極 | |
| B. | 電解結束后,陰極室溶液的pH與電解前相比將不變 | |
| C. | 陽極室中發生的電極反應為2H++2e-═H2↑ | |
| D. | 若兩極共收集到氣體13.44 L(標準狀況),則除去的尿素為18g(忽略氣體的溶解) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
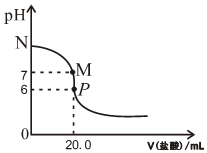 298K時,在20.0mL0.20mol•L-1氨水中滴入0.20mol•L-1的鹽酸,溶液的pH與所加鹽酸的體積關系如圖所示.
298K時,在20.0mL0.20mol•L-1氨水中滴入0.20mol•L-1的鹽酸,溶液的pH與所加鹽酸的體積關系如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ksp(CaF2)隨溫度和濃度的變化而變化 | |
| B. | 向1 L0.2 mol•L-1 HF溶液中加入1 L 0.2 mol•L-1 CaCl2溶液,沒有沉淀產生 | |
| C. | AgCl不溶于水,不能轉化為AgI | |
| D. | 常溫AgCl若在NaI溶液中開始轉化為AgI,NaI濃度必須不低于$\frac{1}{\sqrt{1.8}}$×10-11 mol•L-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com