
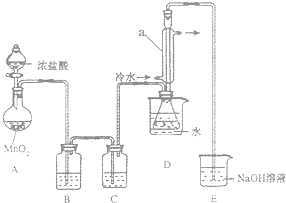
 S2Cl2是一種金黃色易揮發的液體,常用作橡膠硫化劑.某化學興趣小組 擬設計實驗制備少量的S2Cl2,査閱資料知S2Cl2在水中易發生歧化反應(一部分硫元素化 合價升高,另一部分化合價降低).加熱條件下硫單質和干燥、純凈的Cl2反應即可生成S2Cl2,反應的化學方程式為:2S+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$S2Cl2.
S2Cl2是一種金黃色易揮發的液體,常用作橡膠硫化劑.某化學興趣小組 擬設計實驗制備少量的S2Cl2,査閱資料知S2Cl2在水中易發生歧化反應(一部分硫元素化 合價升高,另一部分化合價降低).加熱條件下硫單質和干燥、純凈的Cl2反應即可生成S2Cl2,反應的化學方程式為:2S+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$S2Cl2.| 物質 | S | S2Cl2 |
| 沸點/℃ | 445 | 138 |
| 熔點/℃ | 113 | -76 |
分析 制取原理是:裝置A先是二氧化錳和濃鹽酸之間反應得到氯氣,但是氯氣中混有HCl和水,裝置B應該先用飽和食鹽水除去HCl,裝置C再用濃硫酸干燥氯氣,裝置D讓氯氣和硫在一定溫度下發生反應:2S+Cl2$\frac{\underline{\;95~100℃\;}}{\;}$S2Cl2,為了控制反應的溫度,采用熱水浴加熱的方法,根據S2Cl2的熔沸點數據,采用冷凝回流的辦法將之收集即可,裝置E試驗中的氯氣要進行尾氣處理,可以用氫氧化鈉來吸收,據此答題.
(1)該實驗需制備氣體,為保證實驗的順利進行,需檢查裝置的氣密性;
(2)制備氯氣需加熱,制備S2Cl2需加熱;
(3)B除去氯氣中的氯化氫,C干燥氯氣,據此分析選擇的藥品;
(4)裝置D中儀器a的作用是冷凝回流、導氣;
(5)S2Cl2和S的沸點不同,可用蒸餾的方法分離;
(6)氯氣中有水,S2Cl2與水反應,有黃色單質硫沉淀生成;
(7)有黃綠色剌激性氣體產生為氯氣,+1價氯和-1價氯發生價態歸中反應.
解答 解:(1)由于裝置中有氣體產生和反應,所以連接好實驗裝置后的第一步實驗操作是檢查裝置的氣密性,
故答案為:檢查裝置的氣密性;
(2)濃鹽酸與二氧化錳制氯氣需要加熱,氯氣和二硫化碳反應應控制在95~100℃,要用水浴加熱,所以實驗中需要加熱的儀器是AD,
故答案為:AD;
(3)根據上面的分析可知,裝置B、C中的試劑分別是飽和食鹽水、濃硫酸,
故答案為:飽和食鹽水、濃硫酸;
(4)裝置D中儀器a是冷凝管,其作用是冷凝回流、導氣,
故答案為:冷凝回流、導氣;
(5)反應結束后從錐形瓶內混合物主要為S2Cl2和S的混合物,根據題中信息可知,S2Cl2和S的沸點不同,所以從混合物中分離出產品的方法是蒸餾,
故答案為:蒸餾;
(6)若實驗過程中缺少C裝置,不經過干燥,氯氣中有水,S2Cl2與水反應,有黃色單質硫沉淀生成,反應的化學方程式為:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑,
故答案為:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑;
(7)E燒杯中吸收了氯氣的氫氧化鈉溶液中含有氯化鈉、次氯酸鈉,向其中加入濃鹽酸,則在酸性環境下,氯離子和次氯酸根離子之間可以發生歸中反應得到氯氣,反應為:ClO-+2H++Cl-=Cl2↑+H2O,
故答案為:ClO-+2H++Cl-=Cl2↑+H2O.
點評 本題考查了氯氣實驗室制備方法,雜質氣體除雜的裝置選擇和試劑選擇,題干信息的應用分析,電子式書寫,化學方程式書寫方法,混合物分離的方法判斷,題目難度中等.


科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
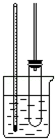 硝基苯的實驗室制備主要步驟如下:
硝基苯的實驗室制備主要步驟如下: .
. +3HNO3$→_{△}^{濃硫酸}$
+3HNO3$→_{△}^{濃硫酸}$ +3H2O.
+3H2O.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
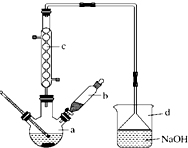 溴苯是一種化工原料,實驗室合成溴苯的裝置示意圖如圖所示,物質的有關數據信息如表,請按下列合成步驟回答問題:
溴苯是一種化工原料,實驗室合成溴苯的裝置示意圖如圖所示,物質的有關數據信息如表,請按下列合成步驟回答問題:| 苯 | 溴 | 溴苯 | |
| 密度/g?cm-3 | 0.88 | 3.10 | 1.50 |
| 沸點/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | H2O分子中H-O的鍵能為462kJ?mol-1 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-480 kJ?mol-1 | |
| C. | H2的燃燒熱為240 kJ?mol-1 | |
| D. | 欲分解2molH2O(l),至少需要提供4×462kJ的熱量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | +2(a-b-c) kJ•mol-1 | B. | +2(b-a) kJ•mol-1 | ||
| C. | +(b+c-a) kJ•mol-1 | D. | +(a+b) kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com