
【題目】在體積為2L的恒容密閉容器中充入一定量的SO2和O2,發生反應:2SO2(g)+O2(g) ![]() 2SO3(g)反應在三種不同的條件下進行,反應物SO2的物質的量(mol)隨反應時間(min)的變化情況如下表所示:
2SO3(g)反應在三種不同的條件下進行,反應物SO2的物質的量(mol)隨反應時間(min)的變化情況如下表所示:

(1)對照實驗1,實驗2改變的某一外界條件可能是_______。
(2)反應達平衡后,向實驗2中加入少量的18O2,一段時間18O后可能存在于哪些物質中________(填選項)。
A 只存在氧氣 B 只存在三氧化硫 C 只存在反應物 D 存在反應物與生成物
(3)實驗3中,在5~15min時段,用O2表示的平均反應速率為______ mol/(L·min)。
(4)若將實驗1置于絕熱體系中,測得實驗到達平衡的時間比原來縮短了,則參加反應的SO2和O2的總能量______(填“>”、“<”或“=”)生成的SO3的總能量。
(5)能說明實驗3達到平衡狀態的標志是_______(任寫一條)。
【答案】加入催化劑 D 0.005 > 各物質的物質的量不再改變(或各物質的物質的量濃度不再改變等合理答案)
【解析】
(1)對照實驗1,實驗2的數據,起始時反應物SO2的物質的量相同,但實驗2建立平衡需要的時間短,平衡時SO2的物質的量相同,結合影響化學反應速率的因素分析解答;
(2) 2SO2(g)+O2(g)![]() 2SO3(g)反應同時向正反應和逆反應方向進行,據此分析解答;
2SO3(g)反應同時向正反應和逆反應方向進行,據此分析解答;
(3)根據二氧化硫的變化量結合方程式計算出氧氣的變化量,再根據v=![]() 計算;
計算;
(4)在絕熱體系中氣體的溫度與反應的熱效應有關,結合影響化學反應速率的因素分析解答;
(5)根據平衡狀態的特征分析解答。
(1)對照實驗1,實驗2的數據,起始時反應物SO2的物質的量相同,但實驗2建立平衡需要的時間短,平衡時SO2的物質的量相同,因此改變的某一外界條件可能是實驗2加入了催化劑,故答案為:加入催化劑;
(2) 2SO2(g)+O2(g)![]() 2SO3(g)反應達平衡后,向實驗2中加入少量的18O2,一段時間18O會出現在二氧化硫、氧氣和三氧化硫三種物質中,故選D;
2SO3(g)反應達平衡后,向實驗2中加入少量的18O2,一段時間18O會出現在二氧化硫、氧氣和三氧化硫三種物質中,故選D;
(3)實驗3中,在5~15min時段,二氧化硫的物質的量的變化量為0.2mol,則氧氣的物質的量變化量為0.1mol,用O2表示的平均反應速率為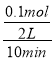 =0.005mol/(L·min),故答案為:0.005;
=0.005mol/(L·min),故答案為:0.005;
(4)若將實驗1置于絕熱體系中,測得實驗到達平衡的時間比原來縮短了,說明反應速率加快,是因為反應放熱,使得容器內氣體的溫度升高,因此參加反應的SO2和O2的總能量大于生成的SO3的總能量,故答案為:>;
(5)根據平衡狀態的特征,能說明實驗3達到平衡狀態的標志有:各物質的物質的量不再改變、各物質的濃度不再改變、氣體的壓強不再改變等,故答案為:各物質的物質的量不再改變(或各物質的物質的量濃度不再改變等)。


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案科目:高中化學 來源: 題型:
【題目】下列有關物質的敘述中不正確的是( )
A. 苯與少量溴水混合,充分振蕩、靜置后,上層液體為橙紅色,下層液體接近無色
B. (CH3)3CCH2Br在NaOH的醇溶液中加熱不能發生消去反應
C. 乙烯、乙炔、聚乙烯 均能使溴水褪色
D. 等質量的C2H4、聚乙烯(![]() 分別完全燃燒,消耗O2的物質的量相同
分別完全燃燒,消耗O2的物質的量相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】液體燃料電池相比于氣體燃料電池具有體積小等優點。一種以液態肼(N2H4)為燃料的電池裝置如圖所示,該電池用空氣中的氧氣作為氧化劑,KOH溶液作為電解質溶液。下列關于該電池的敘述正確的是
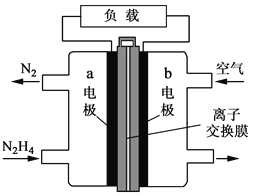
A. b極發生氧化反應
B. a極的反應式:N2H4+4OH--4e-=N2↑+4H2O
C. 放電時,電流從a極經過負載流向b極
D. 其中的離子交換膜需選用陽離子交換膜
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學課外興趣小組為探究銅跟濃硫酸的反應情況,用如圖所示裝置進行有關實驗:

(1)B是用來收集實驗中產生的氣體的裝置,但未將導管畫全,請在圖上把導管補充完整_________。
(2)實驗中他們取6.4 g銅片和12 mL 18 mol·L1濃硫酸放在圓底燒瓶中共熱,直到反應完畢,最后發現燒瓶中還有銅片剩余,該小組學生根據所學的化學知識認為還有一定量的硫酸剩余。
①寫出銅跟濃硫酸反應的化學方程式:__________________;
②為什么有一定量的余酸但未能使銅片完全溶解,你認為原因是__________________;
③下列藥品中能夠用來證明反應結束后的燒瓶中確有余酸的是________(填編號)。
A.鐵粉 B.BaCl2溶液 C.銀粉 D.Na2CO3溶液
(3)裝置C中試管D內盛裝的是品紅溶液,當B中氣體收集滿后,有可能觀察到的現象是_____________,待反應結束后,向C中燒杯內加入沸水,D中觀察到的現象是_____________。
(4)實驗裝置C有可能造成環境污染,試用最簡單的方法加以解決,__________________(實驗用品自選)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機化合物“利尿酸”是一種常見的興奮劑,其分子結構如下圖,下列說法正確的是

A. 利尿酸是芳香烴
B. 利尿酸與AgNO3溶液反應有白色沉淀生成
C. 一定條件下,利尿酸能發生取代反應、加成反應和酯化反應
D. 1mol利尿酸與飽和碳酸鈉溶液反應能放出1 mol CO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室中需要配制0.2mol/L的NaCl溶液960mL,配制時應選用的容量瓶的規格和稱取的質量分別是 ( )
A. 960mL,11.12g B. 1000mL,11.7g
C. 1000mL,117g D. 任意規格,111.2g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】雙羥基鋁碳酸鈉是醫療上常用的一種抑酸劑,其化學式是NaAl(OH)2CO![]() 。關于該物質的說法正確的是( )
。關于該物質的說法正確的是( )
A. 該物質屬于兩性氫氧化物
B. 該物質是Al(OH)3和Na2CO3的混合物
C. 1 mol NaAl(OH)2CO3最多可消耗3 mol H![]()
D. 該藥劑不適合于胃潰瘍患者服用
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知阿伏加德羅常數的值為NA。下列說法正確的是( )
A. 標準狀況下,2.24LCCl4含有的共價鍵數為0.4NA
B. 常溫下,14 g的![]() 含中子數目為6NA
含中子數目為6NA
C. 用鉑電極電解100 mL 1 mol L-1的CuSO4溶液足夠長時間,轉移電子數一定為0.2NA
D. 將含3NA個離子的Na2O2固體溶于水配成1L溶液,所得溶液中Na+的濃度為2mol/L
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com