
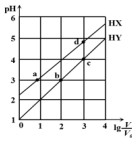
 在濃度均為0.1mol/L、體積均為V0的HX、HY,分別加水稀釋至體積V,pH隨lg$\frac{V}{{V}_{0}}$的變化關系如圖所示.下列敘述正確的是( )
在濃度均為0.1mol/L、體積均為V0的HX、HY,分別加水稀釋至體積V,pH隨lg$\frac{V}{{V}_{0}}$的變化關系如圖所示.下列敘述正確的是( )| A. | a、b兩點的溶液中:c(X-)>c(Y-) | |
| B. | 相同溫度下,電離常數K(HX):d>a | |
| C. | 溶液中水的電離程度:d>c>b>a | |
| D. | lg$\frac{V}{{V}_{0}}$=2時,若同時微熱兩種液體(不考慮HX、HY和H2O的揮發),則$\frac{c({X}^{-})}{c({Y}^{-})}$ 增大 |
分析 A.根據圖知,lg$\frac{V}{{V}_{0}}$=0時,HX的pH>1,說明HX部分電離為弱電解質,HY的pH=1,說明HY完全電離,為強電解質;
B.平衡常數只隨溫度變化,不隨濃度變化,相同溫度下,酸的電離平衡常數不變;
C.酸或堿抑制水電離,酸中氫離子濃度越小其抑制水電離程度越小;
D.lg$\frac{V}{{V}_{0}}$=2,若同時微熱兩種溶液(不考慮HX、HY和H2O的揮發),n(X-)增大,n(Y-)不變,二者溶液體積相等.
解答 解:A.根據圖知,lg$\frac{V}{{V}_{0}}$=0時,HX的pH>1,說明HX部分電離為弱電解質,HY的pH=1,說明HY完全電離,為強電解質,HY的酸性大于HX,a、b兩點的溶液中:c(X-)<c(Y-),故A錯誤;
B.酸的電離平衡常數只與溫度有關,所以相同溫度下,電離常數K( HX):a=d,故B錯誤;
C.酸或堿抑制水電離,酸中氫離子濃度越小其抑制水電離程度越小,根據圖知,b溶液中氫離子濃度等于a,則水電離程度a=b,溶液中氫離子濃度:a=b>d>c,所以溶液中水的電離程度:a=b<d<c,故C錯誤;
D.lg$\frac{V}{{V}_{0}}$=2,若同時微熱兩種溶液(不考慮HX、HY和H2O的揮發),n(X-)增大,n(Y-)不變,二者溶液體積相等,所以$\frac{\frac{n({X}^{-})}{V}}{\frac{n({Y}^{-})}{V}}$=$\frac{c({X}^{-})}{c({Y}^{-})}$變大,故D正確;
故選D.
點評 本題考查弱電解質電離,為高頻考點,側重考查學生分析推斷及識圖能力,正確判斷兩種酸的強弱是解本題關鍵,注意:酸的電離平衡常數只與溫度有關,與溶液濃度無關,易錯選項是D,題目難度中等.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 任何烷烴分子中碳氫原子個數比都是相同的 | |
| B. | 烷烴的沸點隨碳原子數增加而逐漸升高 | |
| C. | 丙烷與Cl2發生取代反應后生成的一氯代物不只是一種 | |
| D. | 正丁烷的熔點、沸點比異丁烷的高 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
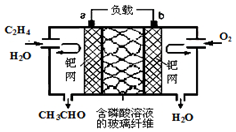 乙烯催化氧化成乙醛可設計成如圖所示的燃料電池,其總反應為:2CH2=CH2+O2→2CH3CHO.下列有關說法正確的是( )
乙烯催化氧化成乙醛可設計成如圖所示的燃料電池,其總反應為:2CH2=CH2+O2→2CH3CHO.下列有關說法正確的是( )| A. | 該裝置能量轉化形式是電能轉化為化學能 | |
| B. | 負極反應式為:CH2=CH2-2e-+H2O=CH3CHO+2H+ | |
| C. | 每有0.1 mol O2反應,則向負極遷移的H+的物質的量為0.4 mol | |
| D. | 電子移動方向:電極a→磷酸溶液→電極b |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
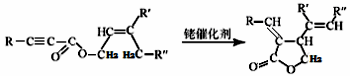 (R、R‘、R“表示氫、烷基或芳基)
(R、R‘、R“表示氫、烷基或芳基)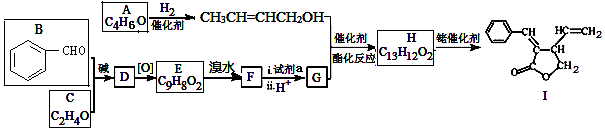
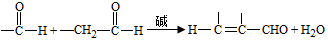
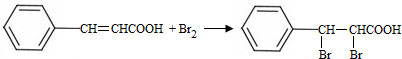 ;試劑a 是NaOH、醇溶液.
;試劑a 是NaOH、醇溶液.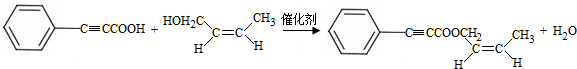 .
.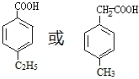 (寫出一種即可).
(寫出一種即可).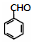 和CH3CHO為原料合成
和CH3CHO為原料合成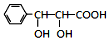 的合成路線流程圖:
的合成路線流程圖: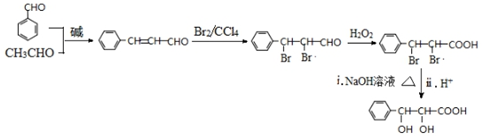 .(其它試劑任選,合成路線常用的表示方式為:CH3CH2OH$→_{170℃}^{濃H_{2}SO_{4}}$CH2=CH2$\stackrel{Br_{2}}{→}$
.(其它試劑任選,合成路線常用的表示方式為:CH3CH2OH$→_{170℃}^{濃H_{2}SO_{4}}$CH2=CH2$\stackrel{Br_{2}}{→}$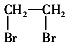 )
)查看答案和解析>>
科目:高中化學 來源: 題型:解答題
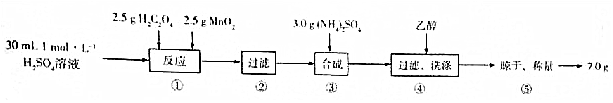
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳酸氫鈉與過量的氫氧化鈣溶液反應:HCO3-+OH-+Ca2+═CaCO3↓+H2O | |
| B. | 過氧化鈉與水的反應:2 O22-+2H2O═4 OH-+O2↑ | |
| C. | 碳酸鈣加入醋酸CO32-+2CH3COOH═CO2↑+2CH3COO-+H2O | |
| D. | 鐵與稀鹽酸的反應:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com