
【題目】某化學興趣小組設計了圖示實驗裝置(圖中省略了夾持儀器)來測定某鐵碳合金中鐵的質量分數。
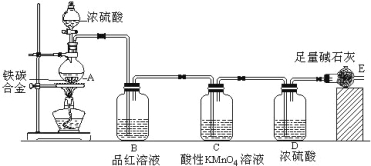
(1)m g鐵碳合金中加入過量濃硫酸,未點燃酒精燈前,A、B均無明顯現象,其原因是:
①常溫下碳與濃硫酸不反應;② 。
(2)寫出加熱時A中碳與濃硫酸發生反應的化學方程式 。
(3)C裝置的作用 。
(4)該小組同學設計的實驗裝置存在缺陷,有關該實驗裝置及實驗過程中,下列因素可能會導致鐵質量分數測量值偏低的是 。
A.A中反應不完全
B.E中堿石灰會吸收空氣中的CO2和H2O
C.反應生成的SO2部分被E中堿石灰吸收
D.反應完全后,還有CO2氣體滯留在裝置體系中
【答案】(1)常溫下Fe遇濃硫酸發生鈍化
(2)C+2H2SO4(濃)![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(3)除盡反應產物中的SO2氣體
(4)BC
【解析】
試題分析:由裝置圖可知,該實驗原理:通過測定干燥管E的質量增重確定二氧化碳的質量,根據二氧化碳的質量計算鐵碳合金中碳的質量,進而計算鐵的質量,再計算合金中鐵的質量分數.故二氧化硫會影響二氧化碳的測定,進入干燥管E的氣體應除去二氧化硫、且干燥.
(1)常溫下,鐵與濃硫酸反應生成一層致密的氧化物保護膜,阻止內金屬繼續與濃硫酸反應,發生鈍化現象;
(2)碳與濃硫酸在加熱的條件下生成二氧化硫、二氧化碳、水,反應方程式為C+2H2SO4(濃)![]() CO2↑+2SO2↑+2H2O;
CO2↑+2SO2↑+2H2O;
(3)A中生成的氣體含有CO2、2SO2,SO2具有漂白性,能使品紅溶液褪色,C裝置的作用為除盡反應產物中的SO2氣體,防止影響二氧化碳的質量測定;
(4)A.A中反應不完全,導致測定二氧化碳質量減小,鐵質量分數增大,故A錯誤;B.E中堿石灰會吸收空氣中的CO2和H2O,導致測定碳質量增大,合金中鐵質量分數減小,故B正確;C.反應生成的SO2部分被E中堿石灰吸收,導致測定碳質量增大,合金中鐵質量分數減小,故C正確;D.裝置內殘留部分二氧化碳,未能被裝置E完全吸收,導致測量的二氧化碳的質量偏小,即合金中碳元素的質量偏小,鐵元素的質量增大,故D錯誤;故答案為BC。


 奪冠金卷全能練考系列答案
奪冠金卷全能練考系列答案科目:高中化學 來源: 題型:
【題目】X、Y、Z三種元素的離子都和氬原子具有相同的電子層排布。X元素單質能在氫氣中燃燒,產生蒼白色火焰;Y元素氫化物的分子式是H2Y,其最高氧化物含有40%的Y;Z元素的離子具有紫色的焰色反應。
(1)根據以上條件,推斷元素名稱:X:_____,Y:_____,Z:________。
(2)X、Y、Z最高價氧化物對應的水化物的酸性由強到弱的順序是________。
(3)用電子式表示Z2Y的形成過程:___________,其化合物中化學鍵的類型是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學生研究小組欲探究CuSO4溶液與Na2CO3溶液混合產生的藍綠色沉淀組成,小組進行下列實驗探究。
【提出假設】
假設1:沉淀為Cu(OH)2
假設2:沉淀為
假設3:沉淀為堿式碳酸銅[化學式可表示為nCuCO3mCu(OH)2]
【查閱資料】無論是哪一種沉淀受熱均易分解(假設均不含結晶水)。
【物質成分探究】
步驟1:將所得懸濁液過濾,用蒸餾水洗滌,再用無水乙醇洗滌
步驟2:甲同學取一定量固體,用氣密性良好的右圖裝置(夾持儀器未畫出)進行定性實驗。
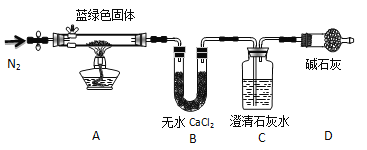
請回答下列問題:
(1)假設2中的沉淀為 。
(2)假設1中沉淀為Cu(OH)2的理論依據是 。
(3)無水乙醇洗滌的目的____ __。
(4)若反應后A中藍綠色固體變黑,C中無明顯現象,證明假設______(填寫序號)成立。
(5)乙同學認為只要將上圖中B裝置的試劑改用 試劑后,便可驗證上述所有假設。
(6)乙同學更換B試劑后驗證假設3成立的實驗現象是 。
(7)在假設3成立的前提下,某同學考慮用Ba(OH)2代替Ca(OH)2,測定藍綠色固體的化學式,若所取藍綠色固體質量為27.1g,實驗結束后裝置B的質量增加2.7g,C中的產生沉淀的質量為19.7g。則該藍綠色固體的化學式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,向2L密閉容器中加入2molN2和10molH2,發生反應N2(g)+3H2(g)![]() 2NH3(g)。2min時測得剩余N2為1mol,此時表示的化學反應速率正確的是( )
2NH3(g)。2min時測得剩余N2為1mol,此時表示的化學反應速率正確的是( )
A.v(N2)=0.25mol·Lˉ1·minˉ1 B.v(H2)=0.5mol·Lˉ1·minˉ1
C.v(NH3)=1mol·Lˉ1·minˉ1 D.v(NH3)=0.25mol·Lˉ1·minˉ1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在15g鐵和氧化鐵的混合物中加入150mL稀H2SO4放出氫氣1.68L(標準狀況)。當反應停止后,鐵和氧化鐵均無剩余,且溶液中無Fe3+存在。為了中和過量H2SO4,并使Fe2+完全轉化為Fe(OH)2沉淀,共耗用3 mol/L NaOH溶液200mL。求:
(1)混合物中鐵的質量為 g
(2)稀H2SO4的物質的量濃度為 mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗組為研究“不同條件”對化學平衡的影響情況,進行了如下實驗:一定條件下,向一個密閉容器中加入0.30molX、0.10molY和一定量的Z三種氣體,甲圖表示發生反應后各物質濃度(c)隨時間(t)的變化〔其中t0~t1階段c(Z)未畫出〕。乙圖表示化學反應速率(v)隨時間(t)的變化,四個階段都只改變一種條件(催化劑、溫度、濃度、壓強,每次改變條件均不同),已知t3~t4階段為使用催化劑。
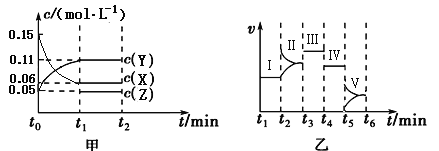
回答下列問題:
(1)若t1=5 min,則t0~t1階段以X濃度變化表示的反應速率為v(X)= 。
(2)在t2~t3階段Y的物質的量減小,則此階段開始時v正 v逆(填“>”、“=”或“<”)。
(3)t4~t5階段改變的條件為 ,此階段的平衡常數K = 。
(4)t5~t6階段容器內Z的物質的量共增加0.10 mol,在反應中熱量變化總量為a kJ,寫出該反應的熱化學方程式 。在乙圖Ⅰ~Ⅴ處平衡中,平衡常數最大的是 。
(5)若起始實驗條件不變,重新向該容器中加入0.60 mol X、0.20 mol Y和0.080 mol Z,反應至平衡狀態后X的轉化率= 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有部分短周期元素的性質或原子結構如下表:
元素編號 | 元素性質或原子結構 |
T | 最外層電子數比內層電子總數少4 |
X | 最外層電子數是次外層電子數的2倍 |
Y | 與氫形成的氣態化合物在標準狀況下的密度為0.76g·L-1 |
Z | 元素最高正價與負價的絕對值之差是6 |
(1)元素X的一種同位素可測定文物年代,這種同位素的符號是 ,在周期表中的位置是 。
(2)元素Y與氫元素形成一種離子YH4+,寫出該離子與Z離子形成化合物的電子式 。
(3)寫出元素X、T形成的化合物XT2的電子式 。
(4)元素Z與元素T相比,非金屬性較強的是 (用元素符號表示),下列表述中能證明這一事實的是 (填序號)。
a.常溫下Z的單質和T的單質狀態不同
b.Z的氫化物比T的氫化物穩定
c.一定條件下Z和T的單質都能與氫氧化鈉溶液反應
d.與鐵加熱,Z生成三價鐵,T生成二價鐵
e.T原子與Z原子電子層數相同,Z原子半徑小于T原子
(5)T的低價氧化物通入Z單質的水溶液中,發生反應的化學方程式為 。
(6)分別用電子式表示Z與鎂元素、Y與氮元素形成化合物的過程: 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2015年2月16日李克強總理到東北調研經濟情況,重點走訪了鋼鐵廠,鼓勵鋼鐵廠提高鋼鐵質量和產量,鐵及其化合物在日常生活中應用廣泛。
(1)利用Fe 2+、Fe3+的催化作用,常溫下可將SO2轉化為SO42-,從而實現對SO2的治理。已知含SO2的廢氣通入含Fe2+、Fe 3+的溶液時,其中一個反應的離子方程式為4Fe2++O2+4 H+ =4Fe3+ +2H2O,則另一反應的離子方程式為_________________;
(2)草酸亞鐵為黃色固體,作為一種化工原料, 可廣泛用于涂料、染料、陶瓷、玻璃器皿等的著色劑以及新型電池材料、感光材料的生產。合成草酸亞鐵的流程如下:
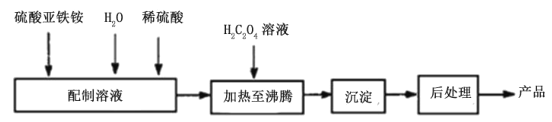
①配制(NH4) 2Fe(SO4)2溶液時,需加入少量稀硫酸,目的是___________________。
②得到的草酸亞鐵沉淀需充分洗滌,洗滌操作的具體方法為_________________________________,檢驗是否洗滌干凈的方法是___________________________。
(3)將制得的產品(FeC2O4·2H2O)在氬氣氣氛中進行加熱分解,結果如下圖(TG%表示殘留固體質量占原樣品總質量的百分數)。
① 則A→B發生反應的化學方程式為:__________________________________。
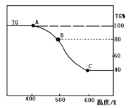
②已知 B→C過程中有等物質的量的兩種氣態氧化物生成,寫出B→C的化學方程式____________;
(4)某草酸亞鐵樣品中含有少量草酸銨。為了測定不純產品中草酸根的含量,某同學做了如下分析實驗:
Ⅰ.準確稱量m g 樣品,溶于少量2mol/L 硫酸中并用 100mL 容量瓶定容。
Ⅱ.取上述溶液20mL,用c mol/L高錳酸鉀標準溶液滴定,溶液變為淡紫色,消耗高錳酸鉀溶液的體積為V 1 mL。
Ⅲ.向上述溶液中加入足量 Zn 粉,使溶液中的 Fe3+恰好全部還原為 Fe2+。
Ⅳ.過濾,洗滌剩余的鋅粉和錐形瓶,洗滌液并入濾液
Ⅴ.用c mol/L KMnO4溶液滴定該濾液至溶液出現淡紫色,消耗KMnO4溶液的體積V 2 mL。
已知:2MnO4- +5H2C2O 4+6H+=2Mn2+ +10CO2+8H2O
MnO4- +8H++5Fe2+ =5Fe3+ + Mn2+ +4H2O
回答下列問題:
①若省略步驟Ⅳ,則測定的草酸根離子含量(填―偏大‖、―偏小‖或―不變‖)。
②mg樣品中草酸根離子的物質的量為(用 c,V1,V2的式子表示,不必化簡)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】己二酸是合成尼龍-66的主要原料之一。實驗室合成己二酸的原理、有關數據及裝置示意圖如下:3![]() +8HNO3—→3
+8HNO3—→3![]() +8NO↑+7H2O
+8NO↑+7H2O

實驗步驟如下:

Ⅰ.在三口燒瓶中加入16 mL 50%的硝酸(密度為1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL環己醇。
Ⅱ.水浴加熱三口燒瓶至50℃左右,移去水浴,緩慢滴加5~6滴環己醇,搖動三口燒瓶,觀察到有紅棕色氣體放出時再慢慢滴加剩下的環己醇,維持反應溫度在60℃~65℃之間。
Ⅲ.當環己醇全部加入后,將混合物用80℃~90℃水浴加熱約10 min(注意控制溫度),直至無紅棕色氣體生成為止。
Ⅳ.趁熱將反應液倒入燒杯中,放入冰水浴中冷卻,析出晶體后過濾、洗滌、干燥、稱重。
請回答下列問題:
(1)裝置b的名稱為 ,使用時要從 (填“上口”或“下口”)通入冷水;滴液漏斗的細支管a的作用是
(2)本實驗所用50%的硝酸的物質的量濃度為 ;實驗中,氮氧化物廢
氣(主要成分為N02和NO)可以用NaOH溶液來吸收,其主要反應為:
2N02+2NaOH=NaN02+NaN03+H20和NO+N02+2NaOH=2NaN02+H20
其中NaOH溶液可以用Na2C03溶液來替代,請模仿上述反應,寫出Na2C03溶液吸收的兩個方程式:
;
(3)向三口燒瓶中滴加環己醇時,反應溫度迅速上升,為使反應溫度不致過高,必要時可采取的措施是 。
(4)為了除去可能的雜質和減少產品損失,可分別用 和 洗滌晶體。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com