
| a/g | 起始讀數/mL | b/mL | c/mL |
| 0.1970 | 0.00 | 31.30 | 42.40 |


科目:高中化學 來源:不詳 題型:實驗題
 Fe2O3 + SO2↑+ SO3↑+ 14H2O。其中三氧化硫與水蒸氣同時冷凝便得到硫酸。用如圖所示裝置模擬用綠礬制硫酸的實驗,并檢驗生成的硫酸和二氧化硫(加熱裝置已略去)。其中b為干燥的試管。下列關于該反應說法正確的是( )
Fe2O3 + SO2↑+ SO3↑+ 14H2O。其中三氧化硫與水蒸氣同時冷凝便得到硫酸。用如圖所示裝置模擬用綠礬制硫酸的實驗,并檢驗生成的硫酸和二氧化硫(加熱裝置已略去)。其中b為干燥的試管。下列關于該反應說法正確的是( )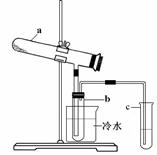
| A.若將反應后的三種氣體通入BaCl2溶液中,產生的沉淀為BaSO3、BaSO4 |
| B.b中產物用紫色石蕊試液即可檢驗出其中H+和SO42— |
| C.為檢驗反應的另一種生成物,試管c中應加入的試劑為NaOH溶液 |
| D.b中所得到的硫酸的質量分數為29.5% |
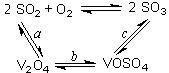
查看答案和解析>>
科目:高中化學 來源:不詳 題型:計算題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
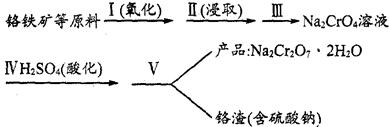
 8Na2CrO4(s)+2Fe2O3(s)+8CO2,該反應的化學平衡常數的表達式為)_____________,在常溫下該反應速率極慢,下列措施中不能使反應速率增大的是____________ 。
8Na2CrO4(s)+2Fe2O3(s)+8CO2,該反應的化學平衡常數的表達式為)_____________,在常溫下該反應速率極慢,下列措施中不能使反應速率增大的是____________ 。| A.升高溫度 | B.將原料粉碎 | C.增加純堿的用量 | D.通入過量的空氣 |
| 序號 | 實驗步驟 | 簡述實驗操作(不必敘述如何組裝實驗裝置) |
| ① | 溶解 | 將混合物放入燒杯中、加水、充分攪拌直到固體不能溶解 |
| ② | | |
| ③ | | |
| ④ | | |
| ⑤ | 過濾、干燥 | 得到K2Cr2O7晶體 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
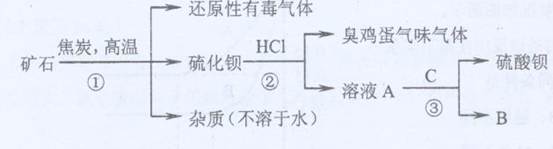 (1)寫出步驟①的化學反應方程式 ,該反應產生的氣體具有 、 等用途。
(1)寫出步驟①的化學反應方程式 ,該反應產生的氣體具有 、 等用途。查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
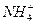 、
、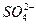 、Fe2+和結晶水,設計了下列操作步驟:①取少量該化合物加熱,發現試管口處有液體,該液體能使無水硫酸銅變藍;②另取少量該化合物溶于水中,滴加少量的氯水,再加入KSCN溶液,有血紅色出現;③取少量溶液于試管中,加入鹽酸,沒有現象,再加入BaCl2溶液,有白色沉淀生成;④取少量溶液于試管中,加入濃的NaOH溶液,微熱有使濕潤的紅色石蕊試紙變藍的氣體產生,同時也有白色沉淀產生,該沉淀很快變成灰綠色沉淀。
、Fe2+和結晶水,設計了下列操作步驟:①取少量該化合物加熱,發現試管口處有液體,該液體能使無水硫酸銅變藍;②另取少量該化合物溶于水中,滴加少量的氯水,再加入KSCN溶液,有血紅色出現;③取少量溶液于試管中,加入鹽酸,沒有現象,再加入BaCl2溶液,有白色沉淀生成;④取少量溶液于試管中,加入濃的NaOH溶液,微熱有使濕潤的紅色石蕊試紙變藍的氣體產生,同時也有白色沉淀產生,該沉淀很快變成灰綠色沉淀。| A.②中的現象說明一定有Fe2+ |
B.為了檢驗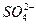 ,可以將③中的試劑換為HNO3酸化的Ba(NO3)2 ,可以將③中的試劑換為HNO3酸化的Ba(NO3)2 |
| C.通過上述實驗可確定該化合物的化學式為(NH4)2Fe(SO4)2·6H2O |
| D.④中的沉淀長時間放置會變成紅褐色沉淀 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
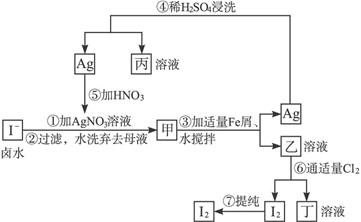
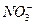 b.除去未反應的I-
b.除去未反應的I-查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com