
 某化學反應2A(g)B (g)+D(g)在不同條件下進行,B、D的起始濃度為0,把反應物A的濃度(mol/L)隨反應時間(min)的變化情況如下表所示.
某化學反應2A(g)B (g)+D(g)在不同條件下進行,B、D的起始濃度為0,把反應物A的濃度(mol/L)隨反應時間(min)的變化情況如下表所示.實驗序號 |
時間 濃度 溫度/℃ |
0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| 4 | 760 | 1.0 |
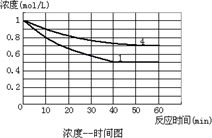 ,故答案為:
,故答案為: .
.

 學練快車道快樂假期寒假作業系列答案
學練快車道快樂假期寒假作業系列答案科目:高中化學 來源: 題型:
 B(g)+D(g)在密閉容器中分別在下列四種不同條件下進行,B、D起始濃度為0,反應物A的濃度(mol?L-1)隨反應時間(min)的變化情況如下表:
B(g)+D(g)在密閉容器中分別在下列四種不同條件下進行,B、D起始濃度為0,反應物A的濃度(mol?L-1)隨反應時間(min)的變化情況如下表:| 時間 實驗序號 |
1 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 (2010?太原模擬)在一恒容密閉容器中發生某化學反應2A(g)?B(g)+C(g),在三種不同條件下進行,其中實驗Ⅰ、Ⅱ都在800℃,實驗Ⅲ在850℃,B、C的起始濃度都為0,反應物A的濃度(mol?L-1)隨時間(min)的變化如圖所示:
(2010?太原模擬)在一恒容密閉容器中發生某化學反應2A(g)?B(g)+C(g),在三種不同條件下進行,其中實驗Ⅰ、Ⅱ都在800℃,實驗Ⅲ在850℃,B、C的起始濃度都為0,反應物A的濃度(mol?L-1)隨時間(min)的變化如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:
| 實驗 序號 |
時間 濃度 溫度 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 200℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化學 來源: 題型:
實驗 序號 |
濃度 時間 溫度 |
0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com