
【題目】下列冶煉金屬的反應原理,不正確的是
A. 鋁熱法煉鐵:Fe2O3 + 2Al 高溫Al2O3 + 2Fe
B. 火法煉銅:Cu2S + O2 高溫2Cu + SO2
C. 電解法制鈉:2NaCl(熔融) 電解2Na + Cl2↑
D. 電解法制鎂:2MgO(熔融) 電解2Mg + O2↑
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】銅的相關化合物在生產(chǎn)生活中具有重要的作用。回答下列問題:
(1)銅元素在周期表中的位置是______,基態(tài)銅原子中,核外電子占據(jù)最高能層的符號是______,占據(jù)該最高能層的電子數(shù)為__________。
(2)在一定條件下,金屬相互化合形成的化合物稱為金屬互化物,如Cu9Al4、Cu5Zn8等。某金屬互化物具有自范性,原子在三維空間里呈周期性有序排列,該金屬互化物屬于__________(填“晶體”或“非晶體”)。
(3)銅能與類鹵素[(SCN)2]反應生成Cu(SCN)2,1mol(SCN)2分子中含有σ鍵的數(shù)目為_____________。硫氰酸(H-S-C≡N)和異硫氰酸(H-N=C=S),這兩種酸中沸點較高的是異硫氰酸(H-N=C=S)。理論上前者沸點低于后者,其原因是____________________________。
(4)銅晶體中銅原子的堆積方式為面心立方堆積,每個銅原子周圍距離最近的銅原子個數(shù)為________。
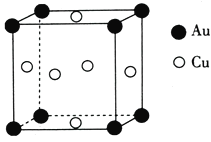
(5)銅與金形成的金屬互化物的晶胞結構如圖所示,其晶胞邊長為a nm,該金屬互化物的密度為____![]() 用含a、NA的代數(shù)式表示)gcm-3。
用含a、NA的代數(shù)式表示)gcm-3。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將氣體A、B置干容積為2L的密用容器中發(fā)生如下反應:4A(g)+B(g)![]() 2C (g),反皮進行到4s末,測得A、B、C的物質的量分別為0.5mol、0.4mol、0.2mol。則用反應物B表示該反應的速率為
2C (g),反皮進行到4s末,測得A、B、C的物質的量分別為0.5mol、0.4mol、0.2mol。則用反應物B表示該反應的速率為
A. 0.025mol·L-1·s-1c. B. 0.0125 mol·L-1·s-1
C. 0.05 mol·L-1·s-1 D. 0.1 mol·L-1·s-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國女藥學家屠呦呦因研制新型抗瘧青蒿素和雙氫青蒿素成果而獲得2015年諾貝爾生理學或醫(yī)學獎。青蒿素和雙氧青蒿素結構如圖所示。下列關于青蒿素和雙氫青蒿素的說法正確的是( )
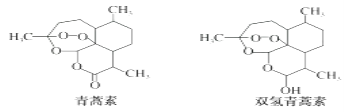
A. 青蒿素的分子式為C15H22O5B. 青蒿素和雙氫青蒿素是同分異構體
C. 青蒿素和雙氫青蒿素都能發(fā)生酯化反應 D. 雙氫青蒿素在水中的溶解性小于青蒿素
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家預言,燃料電池將是21世紀獲得電能的重要途徑。近幾年開發(fā)的甲醇燃料電池是采用鉑作電極催化劑,電池中的質子交換膜只允許質子(就是H+)和水分子通過。其工作原理的示意圖如下,請回答下列問題:
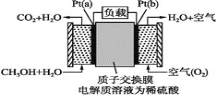
(1)該裝置的能量轉化形式為________。
(2)Pt(a)電極是電池________(填“正”或“負”)極;
(3)電解液中的H+向_____(填“a”或“b”)極移動;
(4)如果該電池工作時消耗1 mol CH3OH,則電路中通過___ mol電子。
(5)比起直接燃燒燃料產(chǎn)生電力,使用燃料電池有許多優(yōu)點,其中主要有兩點:首先是燃料電池的能量轉化率高,其次是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.根據(jù)下表所示化學反應與數(shù)據(jù)關系,回答下列問題:
化學反應 | 平衡常數(shù) | 溫度 | |
973 K | 1173 K | ||
①Fe(s)+CO2(g)FeO(s)+CO(g) | K1 | 1.50 | 2.15 |
②Fe(s)+H2O(g)FeO(s)+H2(g) | K2 | 2.40 | 1.67 |
③CO(g)+H2O(g)CO2(g)+H2(g) | K3 | ? | ? |
(1)反應①是________(填“吸熱”或“放熱”)反應。
(2)在973K時,K3=_________。
(3)要使反應③在一定條件下建立的平衡向逆反應方向移動,可采取的措施有______(填寫字母序號)。
A.縮小反應容器的容積 B.擴大反應容器的容積 C.升高溫度
D.使用合適的催化劑 E.設法減小平衡體系中的CO濃度
Ⅱ.無機和有機氰化物在工農(nóng)業(yè)生產(chǎn)中應用廣泛,尤其是冶金工業(yè)常用的氰化物,含氰廢水的處理顯得尤為重要。含氰廢水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工業(yè)上有多種廢水處理方法。
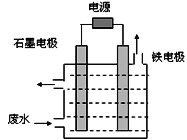
(1)電解處理法:
用如圖所示裝置處理含CN-廢水時,控制溶液pH為9~10并加入NaCl,一定條件下電解,陽極產(chǎn)生的ClO-將CN-氧化為無害物質而除去。鐵電極為__________(填“陰極” 或“陽極”),陽極產(chǎn)生ClO-的電極反應為__________________________,陽極產(chǎn)生的ClO-將CN-氧化為無害物質而除去的離子方程式為__________________________。
(2)UV(紫外光線的簡稱)—H2O2氧化法。
實驗過程:取一定量含氰廢水,調節(jié)pH,加入一定物質的量的H2O2,置于UV工藝裝置中,
光照一定時間后取樣分析。
【查閱資料】
①在強堿性溶液中4[Fe(CN)6]3-+4OH-===4[Fe(CN)6]4-+O2↑+2H2O,[Fe(CN)6]4-更穩(wěn)定;
②[Fe(CN)6]3-轉化為CN-容易被H2O2除去;
③HCN是有毒的弱酸,易揮發(fā)。
【問題設計】
①請寫出HCN的電子式________________。
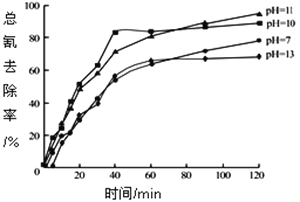
②含氰廢水在不同pH下的除氰效果如圖所示,pH選擇的最佳范圍應為________________(選填編號:![]() .7~10;
.7~10;![]() .10~11;
.10~11;![]() .11~13),解釋該pH不宜太大的原因___________________。
.11~13),解釋該pH不宜太大的原因___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)在密閉容器中,使2 mol N2和6 mol H2混合發(fā)生反應:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
①當反應達到平衡時, N2和H2的轉化率之比為________。
②保持體積不變,升高平衡體系的溫度,混合氣體的平均相對分子質量__________ (填“變大”、“變小”或“不變”) 。
③若容器恒容、絕熱,加熱使容器內(nèi)溫度迅速升至原來的2倍,達到新平衡后,容器內(nèi)溫度________(填“大于”、“小于”或“等于”)原來的2倍。
(2)在一定條件下,可逆反應A+B![]() mC變化如圖所示。已知縱坐標表示在不同溫度和壓強下生成物C在混合物中的質量分數(shù),p為反應在T2溫度時達到平衡后向容器加壓的變化情況。
mC變化如圖所示。已知縱坐標表示在不同溫度和壓強下生成物C在混合物中的質量分數(shù),p為反應在T2溫度時達到平衡后向容器加壓的變化情況。

①溫度T1________T2(填“大于”“等于”或“小于”)。
②正反應是________反應(填“吸熱”或“放熱”)。
③如果A、B、C均為氣體,則m________2(填“大于”“等于”或“小于”)。
④當溫度和容積不變時,如在平衡體系中加入一定量的某稀有氣體,則平衡________移動(填“向正反應方向”“向逆反應方向”或“不”)。
(3)工業(yè)上用凈化后的水煤氣在催化劑作用下制取氫氣:CO(g)+H2O(g)![]() H2(g)+CO2(g)。一定條件下,將4 mol CO與2 mol H2O(g)充入2 L密閉容器中,體系中各物質的濃度隨時間的變化如圖所
H2(g)+CO2(g)。一定條件下,將4 mol CO與2 mol H2O(g)充入2 L密閉容器中,體系中各物質的濃度隨時間的變化如圖所
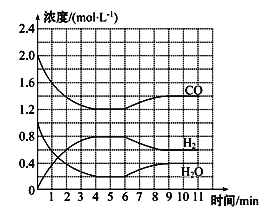
①在0~4 min時段,反應速率v(H2O)為_________。
②該反應到4 min時,CO的轉化率為________。
③若6 min時改變的外部條件為升溫,則該反應的ΔH__________0(填“>”“=”或“<”)。
④判斷該反應達到化學平衡狀態(tài)的依據(jù)是_______。
a.混合氣體的密度不變
b.混合氣體中c(CO)不變
c.v(H2O)正=v(H2)逆
d.斷裂2 mol H—O鍵的同時生成1 mol H—H鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】50 mL 0.5 molL -1 鹽酸與50 mL0.55 mol L -1 NaOH溶液在如下圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題:
(1)從實驗裝置上看,圖中尚缺少的一種玻璃用品是______________________。

(2)燒杯間填滿碎紙條的作用是______________________________________。
(3)若大燒杯上不蓋硬紙板,求得中和熱數(shù)值_______(填“偏大”“偏小”或“無影響”)。
(4)實驗中改用60 mL 0.50 molL -1 鹽酸跟50 mL 0.55 molL -1 NaOH溶液進行反應,與上述實驗相比,所放出的熱量 _______(填“相等”或“不相等”),所求中和熱 _____(填“相等”或“不相等”),簡述理由_______________________________。
(5)用相同濃度和體積的氨水代替NaOH溶液進行上述實驗,測得中和熱的數(shù)值會_________;用0.50 molL -1 NaOH溶液50 mL進行上述實驗,測得的中和熱的數(shù)值會__________(填“偏大”“偏小”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有一容積固定的密閉反應器,中間有一個可自由移動的導熱的隔板將容器分成甲、乙兩部分,分別發(fā)生下列兩個可逆反應:

甲:a(g)+b(g)![]() 2c(g) ΔH1<0、乙: x(g)+3y(g)
2c(g) ΔH1<0、乙: x(g)+3y(g)![]() 2z(g) ΔH2>0
2z(g) ΔH2>0
起初甲、乙均達到反應平衡后隔板位于正中間,然后進行相關操作后,下列敘述錯誤的是
A. 在反應器恒溫下,向乙中通入z氣體,c的物質的量濃度增大
B. 在反應器恒溫下,向甲中通入惰性氣體,乙中x、y的轉化率增大
C. 在反應器絕熱下,向乙中通入z氣體,反應器中溫度升高
D. 在反應器絕熱下,向甲中通入惰性氣體,c的物質的量不變
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com