
| A. | H2O2的電子式 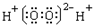 | |
| B. | 氨分子的結構式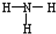 | |
| C. | S2-的結構示意圖  | |
| D. | 原子核內有20個中子的氯原子${\;}_{37}^{17}Cl$ |
 輕巧奪冠周測月考直通中考系列答案
輕巧奪冠周測月考直通中考系列答案科目:高中化學 來源: 題型:解答題
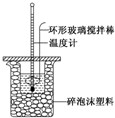 某實驗小組用0.50mol•L-1 NaOH溶液和0.50mol•L-1 硫酸溶液進行反應熱的測定,實驗裝置如圖所示.
某實驗小組用0.50mol•L-1 NaOH溶液和0.50mol•L-1 硫酸溶液進行反應熱的測定,實驗裝置如圖所示.| 溫度 次數 | 起始溫度t1/℃ | 終止溫 度t2/℃ | 溫度差 平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
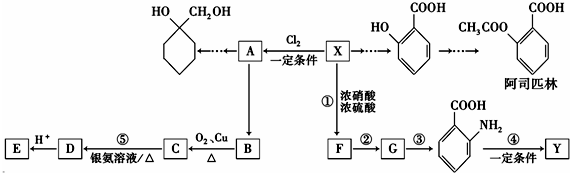
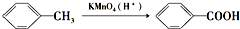
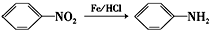 (苯胺,易被氧化)
(苯胺,易被氧化)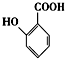 的名稱為鄰羥基苯甲酸,G中官能團名稱為硝基、羧基;
的名稱為鄰羥基苯甲酸,G中官能團名稱為硝基、羧基; ;
; $\stackrel{一定條件下}{→}$
$\stackrel{一定條件下}{→}$ +(n-1)H2O;
+(n-1)H2O;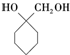 的合成路線(無機試劑任用).合成路線流程圖示例如下:
的合成路線(無機試劑任用).合成路線流程圖示例如下: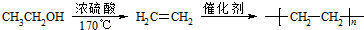
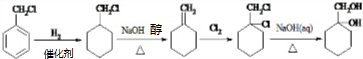 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Mg(OH)2[Al(OH)3] | B. | MgCl2(AlCl3) | C. | Mg(Al) | D. | MgO(Al2O3) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
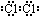 ,由②、④兩種元素的原子按1:1組成化合物的電子式為
,由②、④兩種元素的原子按1:1組成化合物的電子式為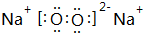 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
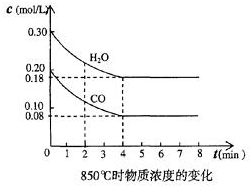 (1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示正反應程度越大反應進行越完全,反應的轉化率越大,K值大小與溫度的關系是:溫度升高,K值可能增大也可能減小(填一定增大、一定減小、或可能增大也可能減小).
(1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示正反應程度越大反應進行越完全,反應的轉化率越大,K值大小與溫度的關系是:溫度升高,K值可能增大也可能減小(填一定增大、一定減小、或可能增大也可能減小).| 時間(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.38 | 0.238 | 0.062 | 0.062 |
| 3 | c | c2 | c3 | c3 |
| 4 | c | c2 | c3 | c3 |
| 5 | 0.6 | 0.26 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 物質 | 開始沉淀時pH | 完全沉淀時pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 5.2 | 6.4 |
| 氧化劑 | 調節pH的物質 | ||
| A | 雙氧水 | E | 氨水 |
| B | 高錳酸鉀 | F | 堿式碳酸銅 |
| C | 氯水 | G | 氧化銅 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 34S原子核內的中子數為16 | B. | 16O與18O互稱同位素 | ||
| C. | 13C和15N原子核內的質子數相差2 | D. | 2H的核外電子數比1H多一個 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com