
分析 (1)根據鐵、氧化鐵都能與鹽酸反應以及反應后溶液中無Fe3+,所以鐵也與硫酸鐵反應,先根據H2求出和硫酸生成1.68LH2的鐵,然后根據混合物發生的反應:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O Fe2(SO4)3+Fe=3FeSO4,可知n(Fe2O3):n(Fe)=1:1,求出Fe2O3和Fe的質量,最終求出混合物中Fe和Fe2O3的質量;
(2)由題意我們應該可以理解反應后溶液中只有Fe 2+而無Fe3+,而且硫酸有剩余,也就說固體與酸反應后溶液中得到的是FeSO4和硫酸的混合液,接著在這混合溶液中滴加NaOH溶液,先中和了硫酸,又與 FeSO4反應生成了Fe(OH)2沉淀,最終溶液中剩余物質其實就是Na2SO4.這樣我們用守恒法考慮,SO4 2-來自原H2SO4,而Na+來自NaOH,這樣得到H2SO4~2NaOH,最后根據c=$\frac{n}{V}$求出原硫酸的物質的量濃度.
解答 解:(1)因鐵、氧化鐵都能與硫酸反應:Fe+H2SO4=FeSO4+H2↑ Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,又因反應后溶液中無Fe3+,所以有反應為:Fe+Fe2(SO4)3=3FeSO4,
1.68L氫氣的物質的量為:$\frac{1.68L}{22.4L/mol}$=0.075mol,根據反應Fe+H2SO4=FeSO4+H2↑可知與硫酸生成1.68LH2消耗的鐵為0.075mol,其質量為:56g/mol×0.075mol=4.2g,剩余混合物質量為:15-4.2=10.8g,剩余的混合物發生如下反應:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O、Fe2(SO4)3+Fe=3FeSO4可得關系式Fe2O3~Fe2(SO4)3~Fe,所以剩余混合物中Fe2O3和Fe的物質的量應該為1:1,設二者物質的量都為n,則160n+56n=10.8g,解得:n=0.05mol,則m(Fe2O3)=160g/mol×0.05mol=8g,m(Fe)=56g/mol×0.05mol=4.2,原混合物中鐵的質量為:4.2g+2.8=7g,
答:原混合物中含有7gFe,4.2gFe2O3;
(2)因為反應后溶液中無Fe3+存在,且固體沒有剩余,則全都是以Fe2+的形式存在,反應后溶質為硫酸亞鐵,根據質量守恒定律可知:n(H2SO4)=n(Na2SO4)=$\frac{1}{2}$n(NaOH)=3mol/L×0.2L×$\frac{1}{2}$=0.3mol,
所以原稀H2SO4的物質的量濃度為:$\frac{0.3mol}{0.15L}$=2mol/L,
答:原稀H2SO4的物質的量濃度為2mol/L.
點評 本題考查混合物反應的計算,題目難度中等,明確發生反應的實質為解答關鍵,注意掌握守恒思想在化學計算中的應用,試題培養了學生的分析能力及化學計算能力.


科目:高中化學 來源: 題型:推斷題
 根據如圖反應框圖填空.已知反應①是工業上生產化合物D的反應,反應⑤是實驗室鑒定化合物E的反應.
根據如圖反應框圖填空.已知反應①是工業上生產化合物D的反應,反應⑤是實驗室鑒定化合物E的反應.
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,2.24 L H2O中所含的原子總數為0.3NA | |
| B. | 0.1 molCl2與足量的NaOH稀溶液反應,轉移的電子總數為0.2NA | |
| C. | 1mol•L一1的NaCl溶液中所含Na+數目為NA | |
| D. | 常溫常壓下,14g由N2和CO組成的混合氣體中含有的原子總數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
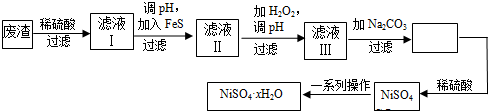
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 |  | 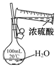 | 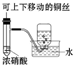 |
| A.制備少量氨氣 | B.吸收HCl | C.配制一定濃度硫酸溶液 | D.制備并收集少量NO2氣體 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 三氯化鐵溶液中加入鐵粉 Fe3++Fe═2 Fe2+ | |
| B. | 鋁粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| C. | FeCl2溶液跟Cl2反應:2Fe2++Cl2=2Fe3++2Cl- | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 物質 | 試劑 | 分離方法 | |
| ① | 氯化鈉(硝酸鉀) | 蒸餾水 | 降溫結晶 |
| ② | 二氧化碳(氯化氫) | 飽和碳酸鈉溶液 | 洗氣 |
| ③ | 乙醇(水) | 生石灰 | 蒸餾 |
| ④ | 苯(苯酚) | 濃溴水 | 分液 |
| A. | ②③ | B. | ①③ | C. | 只有③ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| ① | ② | ③ | 實驗結論 | 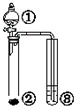 | |
| A. | 硫酸 | Na2SO3 | KMnO4 | SO2有漂白性 | |
| B. | Br2的苯溶液 | 鐵屑 | AgNO3 | 苯和溴單質在鐵催化劑作用下發生取代反應 | |
| C. | H2O | 工業電石 | KMnO4 | 乙炔具有還原性 | |
| D. | 硫酸 | Na2CO3 | Na2SiO3 | 非金屬性:S>C>Si |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲=乙=丙=丁 | B. | 乙=丙>甲=丁 | C. | 乙>丙>甲>丁 | D. | 乙=丙>甲>丁 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com