
| A. | 溶液pH≤2時,生鐵發生析氫腐蝕 | |
| B. | 生鐵的腐蝕中化學腐蝕比電化學腐蝕更普遍 | |
| C. | 在酸性溶液中生鐵可能發生吸氧腐蝕 | |
| D. | 兩溶液中負極反應均為:Fe-2e-═Fe2+ |
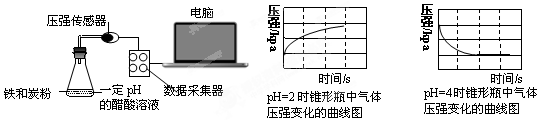
分析 根據壓強與時間關系圖知,pH=2的醋酸溶液中壓強隨著反應的進行而逐漸增大,說明該反應發生析氫腐蝕,pH=4的醋酸溶液中壓強隨著反應的進行而逐漸減小,說明發生吸氧腐蝕,根據原電池原理來分析解答.
解答 解:A.根據PH=2的溶液中壓強與時間的關系知,壓強隨著反應的進行而逐漸增大,說明該裝置發生析氫腐蝕,則溶液pHpH≤2時,生鐵發生析氫腐蝕,故A正確;
B.金屬的腐蝕以電化學腐蝕為主,所以生鐵的腐蝕中電化學腐蝕更普遍,故B錯誤;
C.pH=4的醋酸溶液中壓強隨著反應的進行而逐漸減小,說明發生吸氧腐蝕,pH=4的醋酸溶液呈酸性,所以在酸性溶液中生鐵可能發生吸氧腐蝕,故C正確;
D.兩個溶液中都發生電化學腐蝕,鐵均作負極,電極反應式為Fe-2e-=Fe2+,故D正確;
故選B.
點評 本題考查了析氫腐蝕和吸氧腐蝕,根據壓強與時間的關系分析吸氧腐蝕和析氫腐蝕、反應速率大小、電極反應等知識點,難度中等.


 智能訓練練測考系列答案
智能訓練練測考系列答案科目:高中化學 來源: 題型:選擇題
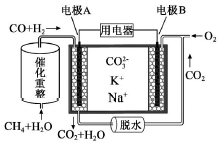
| A. | 電極B上發生的電極反應為:O2+2CO2+4e-=2CO32- | |
| B. | 電極A上H2參與的電極反應為:H2+2OH--2e-=2H2O | |
| C. | 電池工作時,CO32-向電極B移動 | |
| D. | 反應CH4+H2O $\frac{\underline{催化劑}}{△}$ 3H2+CO,每消耗1molCH4轉移12mol 電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 操作 | 可能的實驗現象 | 解釋 | |
| A | 某溶液中加入鹽酸酸化的氯化鋇溶液 | 有白色沉淀生成 | 溶液中一定含有SO42- |
| B | 將SO2中通入硝酸鋇溶液中 | 有白色沉淀生成 | BaSO3不溶于硝酸 |
| C | 同溫同壓下,用pH試紙測定相同濃度的碳酸鈉和硫酸鈉溶液的酸堿性 | 碳酸鈉溶液顯堿性,硫酸鈉溶液顯中性 | 碳酸鈉發生了水解 |
| D | 向淀粉KI溶液中通入Cl2 | 溶液先變藍后褪色 | Cl2先表現氧化性、后表現強氧化性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入氫氧化鈉溶液并加熱,產生的氣體能使濕潤紅色石蕊試紙變藍,推斷溶液中含有NH4+ | |
| B. | 無色試液在焰色反應中呈黃色,推斷試液是鈉鹽溶液,不含鉀鹽 | |
| C. | 加入稀鹽酸產生無色氣體,將氣體通入澄清石灰水中,溶液變渾濁,推斷溶液中含有CO32- | |
| D. | 加入氯化鋇溶液有白色沉淀產生,再加鹽酸,沉淀不消失,推斷溶液中含有SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
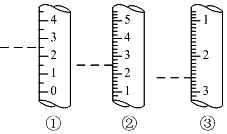 托盤天平、容量瓶、量筒是常見的中學化學計量儀器,熟知這些儀器的使用是定量研究化學的基礎.
托盤天平、容量瓶、量筒是常見的中學化學計量儀器,熟知這些儀器的使用是定量研究化學的基礎.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入銀氨溶液,并水浴加熱 | |
| B. | 加入2~3滴石蕊試液 | |
| C. | 先加入濃NaOH溶液,加熱蒸餾,把蒸餾出的物質加銀氨溶液并水浴加熱 | |
| D. | 直接蒸餾,把蒸餾出的物質加NaOH溶液調至堿性,再加銀氨溶液,并水浴加熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A(g)+2B(g)?2C(g);△H1>0 | B. | A(g)+B(g)?C(g)+D(g);△H2>0 | ||
| C. | A(s)+2B(g)?C(g);△H3>0 | D. | A(s)?B(g)+C(g);△H4<0 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com