
���}Ŀ���O(sh��)NA��ʾ����٤���_����(sh��)�������f�����_���ǣ� ��
A.��(bi��o)�r�£�11.2L�״��к��е���Ӕ�(sh��)9NA
B.6.0g��ȩ��HCHO���ʹ���Ļ�����к��е�ԭ�ӿ���(sh��)��0.8NA
C.100mL0.1mol/L��KAl(SO4)2��Һ�к��е���x�ӿ���(sh��)С��0.02NA
D.�քe��H2O2��KMnO4�Ƃ�����������D(zhu��n)�Ƶ���Ӕ�(sh��)Ŀ���
���𰸡�B
��������
A����(bi��o)��(zh��n)��r�£��״����ǚ��w���������Ú��wĦ���w�eӋ��11.2L�״������|(zh��)������Ҳ����Ӌ���11.2L�״��к��е���Ӕ�(sh��)��A�e�`��
B����ȩ(HCHO)�ʹ�����ʽ����CH2O���t6.0g��ȩ(HCHO)�ʹ���Ļ�����к�CH2O�����|(zh��)������![]() = 0.2 mol�����е�ԭ�ӂ���(sh��)��0.2mol��4��NA= 0.8NA��B����_��
= 0.2 mol�����е�ԭ�ӂ���(sh��)��0.2mol��4��NA= 0.8NA��B����_��
C�����Al3+����Һ��ˮ�⣬Al3++3H2O![]() Al(OH)3+3H+����ʹ��x�Ӕ�(sh��)Ŀ���ӣ�����100mL 0.1mol/L��KAl(SO4)2��Һ�к��е���x�ӿ���(sh��)����0.02NA��C�e�`��
Al(OH)3+3H+����ʹ��x�Ӕ�(sh��)Ŀ���ӣ�����100mL 0.1mol/L��KAl(SO4)2��Һ�к��е���x�ӿ���(sh��)����0.02NA��C�e�`��
D��2H2O2![]() O2��+2H2O���p��ˮ�е���Ԫ�؏�-1�r���ߵ�0�r��ÿ����1mol O2�D(zhu��n)��2mole-��2 KMnO4
O2��+2H2O���p��ˮ�е���Ԫ�؏�-1�r���ߵ�0�r��ÿ����1mol O2�D(zhu��n)��2mole-��2 KMnO4 ![]() K2MnO4+ MnO2+ O2����KMnO4����Ԫ�؏�-2�r��0�r��ÿ����1mol O2�D(zhu��n)��4mole-��D�e�`��
K2MnO4+ MnO2+ O2����KMnO4����Ԫ�؏�-2�r��0�r��ÿ����1mol O2�D(zhu��n)��4mole-��D�e�`��
���xB��



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�����S���ַQ��S����B2���ɴ��M(j��n)�l(f��)���ͼ�(x��)�����������������M(j��n)ҕ�����p�p�۾�ƣ�ڡ����S�ط��ӵĽY(ji��)��(g��u)�飺

��֪��
���P(gu��n)���S�ص������f���У������_���ǣ�
A.ԓ������ķ���ʽ��C17H22N4O6
B.���ԗl���¼ӟ�ˮ�⣬��CO2����
C.���ԗl���¼ӟ�ˮ�⣬������Һ�ӉA����NH3����
D.�ܰl(f��)����������(y��ng)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ���҇��������������Ƶú�ʹ�ý����\�ć��ң�һ�N���W�\�V��ZnS������SiO2������FeS��CdS��PbS�s�|(zh��)����ԭ���Ƃ�����\��������D��ʾ��
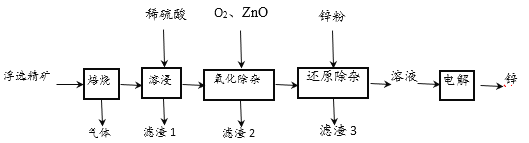
���P(gu��n)�����x��[c (Mn+)=0.1mol��L��1]�γɚ������������pH�������£�
�����x�� | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
�_ʼ������pH | 1.5 | 6.3 | 6.2 | 7.4 |
������ȫ��pH | x | 8.3 | 8.2 | 9.4 |
�����£�Ksp[Fe(OH)3]��1��10��38����Һ�Ю�(d��ng)�x�ӝ��С��1��10��5mol/L�r���J(r��n)�������ȫ���ش����І��}��
��1����ϡ�����ܽ��r���a(ch��n)��PbSO4��SiO2��������(j��ng)�^�V����VҺ�м���O2��ZnO��Ŀ���dz�ȥ�s�|(zh��)Fe2+��Fe3+���t�������s������ZnO���������{(di��o)��(ji��)��Һ��pH����(y��ng)�{(di��o)��(ji��)��Һ��pH�ķ�����_______���(sh��)ֵ����
��2�����K늘O늽������\��Һ�Ƃ���|(zh��)�\�r��늽�Ŀ�����(y��ng)��________��늽�ʹ�\���e��늽�Һ�ɷ���_______����ѭ�h(hu��n)ʹ�á�
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��ijʮ�C���@[(NH4)xH6��xV10O28��yH2O(�����C�飫5�r)]���Á�����߶��C�X�Ͻ�
��. (NH4)xH6��xV10O28��yH2O���Ƃ�
��NH4VO3����pH��4�������Խ��|(zh��)�����Ҵ����^�V�õ�(NH4)xH6��xV10O28��yH2O���w���Ҵ���������____________________________________��
��. (NH4)xH6��xV10O28��yH2O�ĽM�ɜy��
(1) NH4+�����y��
��(zh��n)�_�Qȡ0.363 6 gԓʮ�C���@���w���������sˮ��NaOH��Һ���ӟ���У����ɵİ�����20.00 mL 0.100 0 mol��L��1�}���(bi��o)��(zh��n)��Һ���ա��õȝ�ȵ�NaOH��(bi��o)��(zh��n)��Һ�ζ��^���}�ᣬ����NaOH��(bi��o)��(zh��n)��Һ8.00 mL��
(2) V10O![]() (M��958 g��mol��1)�����y��
(M��958 g��mol��1)�����y��
���E1����(zh��n)�_�Qȡ0.3636 gԓʮ�C���@���w�������m��ϡ���ᣬ��ʹ֮�ܽ⡣
���E2���������sˮ��NaHSO3�����?j��n)��裬�?/span>V10O![]() ��ȫ�D(zhu��n)����VO2����
��ȫ�D(zhu��n)����VO2����
���E3�����m��ϡ�����ữ���ӟ���У���ȥ��Һ�У�4�r��
���E4����0.020 00 mol��L��1 KMnO4��(bi��o)��(zh��n)��Һ�ζ����K�c�r����30.00 mL KMnO4��(bi��o)��(zh��n)��Һ(ԓ�^�����C����������5�r���i��߀ԭ����2�r)��
�ٌ������E2����(y��ng)���x�ӷ���ʽ��____________________________________��
����δ�M(j��n)�в��E3�������t��(sh��)ֵy��________(����ƫ������ƫС�������oӰ���)��
��ͨ�^Ӌ��_��ԓʮ�C���@���w�Ļ��W(xu��)ʽ(����Ӌ���^��)��________
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ���״�����Ҫ�Ļ���ԭ�ϣ��ֿ�����ȼ�ϡ����úϳɚ⣨��Ҫ�ɷ֞�CO��CO2��H2���ڴ����������ºϳɼ״����l(f��)������Ҫ����(y��ng)���£�
��CO(g)+2H2(g)![]() CH3OH(g) ��H1
CH3OH(g) ��H1
��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H2
CH3OH(g)+H2O(g) ��H2
��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H3
CO(g)+H2O(g) ��H3
��1����֪���P(gu��n)�Ļ��W(xu��)�I�I�ܔ�(sh��)��(j��)���£�
���W(xu��)�I | H��H | C��O | | H��O | C��H |
E/��kJ��mol��1�� | 436 | 343 | 1076 | 465 | 413 |
�ɴ�Ӌ���H1=______kJ��mol��1���Ô�(sh��)ֵ��ʾ�����t��H3=______kJ��mol��1���á�H1�͡�H2��ʾ����
��2�����ء��������]�����г���һ������CO(g)��H2(g)�M(j��n)�Тٷ���(y��ng)���������f������(y��ng)�_(d��)��ƽ���B(t��i)����_____���̖����ͬ����
a���wϵ�������ֲ�׃
b��v��(CO) = v��(H2)
c��CO�cCH3OH�����|(zh��)����֮�ȱ��ֲ�׃
d��ÿ����1molCO��ͬ�r����1molCH3OH
e����Ϛ��w���ܶȱ��ֲ�׃
��3����ͬ�ء�ͬ�w�e�ļס��ҡ����������]�����зքe������w�M(j��n)�Тٷ���(y��ng)����������2mol H2��1molCO����������1mol H2��0.5mol CO����������1mol CH3OH����ء������·���(y��ng)�_(d��)ƽ��r�������P(gu��n)ϵ���_����________��
a���D(zhu��n)���ʣ���>�� b������(y��ng)�ų��ğ�����(sh��)ֵQ��Q�� = 2Q��
c��CO���|(zh��)��m��m��= m��> 2m�� d��������(n��i)����P��P��=P��<2P��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ����ij�W(xu��)������֪���|(zh��)������ȵ������y��δ֪���|(zh��)������ȵ�NaOH��Һ�r���x���̪��ָʾ�����ش����І��}��
��1���Ø�(bi��o)��(zh��n)������ζ����y��NaOH��Һ�r���K�c�F(xi��n)����_______��
��2�����ζ��_ʼ�ͽY(ji��)���r����ʽ�ζ����е�Һ����D��ʾ���t�ζ��Y(ji��)���r���x��(sh��)��___________ mL������������Һ���w�e��_______mL��
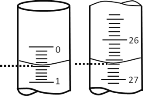
�ζ��Δ�(sh��) | ���yNaOH��Һ���w�e/mL | 0.1000mol��L��1������w�e/mL | ||
�ζ�ǰ�̶� | �ζ���̶� | ��Һ�w�e/mL | ||
��һ�� | 25.00 | 0.00 | 26.11 | 26.11 |
�ڶ��� | 25.00 | 1.56 | 30.30 | 28.74 |
������ | 25.00 | 0.22 | 26.31 | 26.09 |
��3��ij�W(xu��)������(j��)3�Ό��քeӛ����P(gu��n)��(sh��)��(j��)���±���
����(j��)�ϱ픵(sh��)��(j��)Ӌ��ɵ�ԓNaOH��Һ�����|(zh��)������Ȟ�___mol��L��1��������λ��Ч��(sh��)�֣���
��4�����в����п���ʹ���yNaOH��Һ�ĝ�Ȕ�(sh��)ֵƫ�͵���_____������ĸ����
A����ʽ�ζ���δ�Ø�(bi��o)��(zh��n)���ϴ��ֱ��ע���(bi��o)��(zh��n)����
B���xȡ�����w�e�r���_ʼ��ҕ�x��(sh��)���ζ��Y(ji��)���r��ҕ�x��(sh��)
C����ʽ�ζ����ڵζ�ǰ�К��ݣ��ζ��������ʧ
D���F��ƿ��ˮϴ����ô��yҺ��ϴ
��5����A�к͵ζ�ԭ��Ҳ������������͵ĵζ����磺һ�N�y��ˮ����Br���ĝ�ȵČ��E���£�
�����F��ƿ�м���̎�����ˮ��25.00mL�������NH4Fe(SO4)2��Һ��
�ڼ���V1mL c1 mol/L AgNO3��Һ���^��������֓u��
����c2mol/L KSCN��(bi��o)��(zh��n)��Һ�M(j��n)�еζ������K�c�r���Ę�(bi��o)��(zh��n)��ҺV2mL��
Ӌ��ԓˮ����Br�������|(zh��)������Ȟ�_______mol��L��1����֪��Ksp(AgBr��= 7.7��10��13��Ag++ SCN��=AgSCN(��ɫ)�� ��Ksp(AgSCN)= 1��10��12����
��ij���С�M��0.50 mol/L NaOH��Һ��0.50 mol/L������Һ�M(j��n)���к͟�Ĝy��������b����D��ʾ��
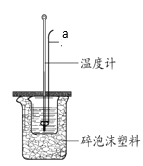
��6���x��a�����Q��_______��
��7��ȡ50 mL NaOH��Һ��30 mL������Һ�M(j��n)�Ќ��y����ֹ�ضȲ��ƽ��ֵ��4.0�档�����J(r��n)��0.50 mol/L NaOH��Һ��0.50 mol/L������Һ���ܶȶ���1 g/cm3���ͺ�������Һ�ıȟ���c��4.18 J/(g����)���tӋ����к͟���H��______(ȡС��(sh��)�c��һλ)��
��8���������Y(ji��)���c��57.3 kJ/mol��ƫ��a(ch��n)��ƫ���ԭ�������_____ (����ĸ)��
a������b�ñ��ء�����Ч����
b������Ͳ��ȡNaOH��Һ���w�e�r��ҕ�̶Ⱦ��x��(sh��)
c���ֶ�ΰ�NaOH��Һ����ʢ�������С������
d���Üض�Ӌ�y��NaOH��Һ��ʼ�ضȺ�ֱ�Ӝy��H2SO4��Һ�Ĝض�
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ����֪��AG��lgc(H+)/c(OH-)���Ҝ�����0.01mol��L1 NH3��H2O��Һ�ζ�20.00mL 0.01mol��L1ijһԪ��HA���ɵ��D��ʾ�ĽY(ji��)���������f�����e�`����
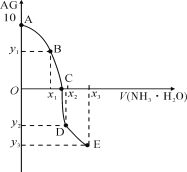
A. ԓ�ζ��������x�ü�����ָʾ��
B. �����^���У�C�c�rˮ����x�̶����
C. ��x3��30���t��3c(OH)��c(NH4+)+3c(H+)��2c(NH3��H2O)
D. A��C���^���У��ɴ��ڣ�c(A)��c(H+)��c(NH)��c(OH)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ���±��Dz�ͬ�ض���ˮ���x�ӷe����(sh��)��
�ض�/�� | 25 |
|
|
ˮ���x�ӷe����(sh��) |
| a |
|
ԇ�ش������}��
��1����![]() ���t��________���������������������
���t��________���������������������![]() �����������������________________��
�����������������________________��
��2��![]() �£�ij
�£�ij![]() ��Һ��
��Һ��![]() ��ȡԓ��Һ
��ȡԓ��Һ![]() ����ˮϡ���
����ˮϡ���![]() ���tϡጺ���Һ��
���tϡጺ���Һ��![]() ________��
________��
��3��![]() �£���
�£���![]() �Ŀ����c��Һ
�Ŀ����c��Һ![]() �c
�c![]() ��ϡ����
��ϡ����![]() ��ϣ��O(sh��)��Ϻ���Һ���w�e��ԭ����Һ�w�e֮�ͣ������û����Һ��
��ϣ��O(sh��)��Ϻ���Һ���w�e��ԭ����Һ�w�e֮�ͣ������û����Һ��![]() ���t
���t![]() ________������Һ�и��N�x�ӵĝ���ɴ�С�����������___________��
________������Һ�и��N�x�ӵĝ���ɴ�С�����������___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
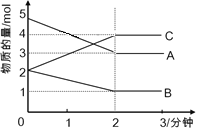
���}Ŀ����2L�������]�����У�ij���淴��(y��ng)(ABC������w)�M(j��n)���^���У� �ڲ�ͬ����(y��ng)�r�g�����|(zh��)���|(zh��)������׃����r��D��ʾ���tԓ����(y��ng)�Ļ��W(xu��)����ʽ��_________________���_ʼ��2��犕r����C��ʾ�䷴��(y��ng)���ʞ�__________��
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com