
【題目】(1)25℃時,相同物質的量濃度的下列溶液:①NaCl②NaOH③H2SO4④(NH4)2SO4,其中水的電離程度按由大到小順序排列為___________(填序數)。
(2)在25℃下,將amol·L-1的氨水與0.01 mol·L-1的鹽酸等體積混合,反應平衡時溶液中c(NH4+)=c(Cl-),則溶液顯___________(填“酸”堿”或“中)性;用含a的代數式表示NH3·H2O的電離常數Kb=___________。
(3)一定溫度下,向氨水中通入CO2,得到(NH4)2CO3、NH4HCO3等物質,溶液中各種微粒的物質的量分數與pH的關系如圖所示。隨著CO2的通入,溶液中c(OH-)/c(NH3·H2O)將___________(填“增大”“減小”或“不變”)。pH=9時,溶液中c(NH4+)+c(H+)=___________。
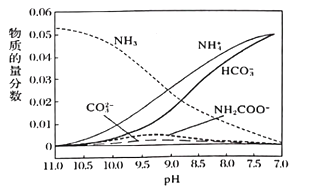
(4)焦亞硫酸鈉(Na2S2O5)可用作食品的抗氧化劑,常用于葡萄酒、果脯等食品中。在測定某葡萄酒中Na2S2O5殘留量時,取25.00mL葡萄酒樣品,用0.01000mol·L-1的碘標準液滴定至終點,消耗5.00mL。該滴定反應的離子方程式為___________;葡萄酒中的Na2S2O5的使用量是以SO2來計算的,則該樣品中Na2S2O5的殘留量為___________g·L-1。
【答案】④>①>②>③ 中 ![]() 減小 2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-) S2O52-+2I2+3H2O===2SO42-+4I-+6H+ 0.128
減小 2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-) S2O52-+2I2+3H2O===2SO42-+4I-+6H+ 0.128
【解析】
(1)根據根據影響水電離的因素進行判斷;(2)根據電荷守恒進行判斷;(3)根據電子守恒進行解答。
(1)根據影響水電離的因素可知:②NaOH、③H2SO4 抑制水的電離,且相同物質的量濃度的③H2SO4 抑制程度更大;④(NH4)2SO4能發生水解,促進水的電離;①NaCl對水的電離無影響,所以25℃時,相同物質的量濃度的溶液水的電離程度按由大到小順序排列為④>①>②>③;答案:④>①>②>③;
(2)在25℃下,將amol·L-1的氨水與0.01 mol·L-1的鹽酸等體積混合,反應平衡時溶液中c(NH4+)=c(Cl-),根據電荷守恒,c(H+)+c(NH4+)=c(Cl-)+ c(OH-)所以c(H+)=c(OH),則溶液顯中性; 因為平衡時溶液中c(NH4+)=c(Cl-)=0.005mol/L,根據物料守恒得c(NH3.H2O)=(0.5a-0.005)mol/L,因為溶液呈中性,所以c(H+)=c(OH)=10-7mol/L,NH3H2O的電離常數Kb= c(OH-).c(NH4+)/c((NH3.H2O)=107×5×103/(0.5a5×103)=109/(a0.01);答案:![]()
(3)c(OH-)/c((NH3.H2O)= c(OH-)×c(NH4+)/[c((NH3.H2O)×c(NH4+)]=Kb/c(NH4+),Kb不變,c(NH4+)不斷增大,比值不斷減小;根據電荷守恒,pH=9時,溶液中存在電荷守恒c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-);答案:減小; 2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-);
(4) I2作氧化劑,1molI2參與反應得到2mol電子,S2052-為還原劑,1molS2052-參與反應,硫元素失去4mol電子,根據原子守恒配平方程式: S2052-+212+3H20=2SO42-+4I-+6H+,計算祥品中S2052-的殘留量時以SO2計算,n(I2)=n(SO2)=0.01000mol.L1x0.01L=0.0001mol,m(S02)=0.0064g,則該樣品中Na2S2O5的殘留量為0.0064g/0.05L =0.128g.L-1。答案:0.128。


 名題金卷系列答案
名題金卷系列答案科目:高中化學 來源: 題型:
【題目】已知:A的蒸汽對氫氣的相對密度是15,且能發生銀鏡反應,F的分子式為C3H6O2。有關物質的轉化關系如下:
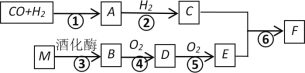
請回答:
(1)B中含有的官能團名稱是__________,反應⑥的反應類型為__________。
(2)寫出反應④的化學方程式__________。
(3)寫出有機物F與NaOH溶液反應的化學方程式__________。
(4)下列說法正確的是__________。
A.有機物D的水溶液常用于標本的防腐
B.有機物B、C、E都能與金屬鈉發生反應
C.有機物F中混有E,可用飽和碳酸鈉溶液進行分離
D.有機物M為高分子化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】不用任何試劑,只用試管和膠頭滴管就可以鑒別開來的一組是:( )
(1)![]() 溶液和
溶液和![]() 溶液 (2)NaOH溶液和
溶液 (2)NaOH溶液和![]() 溶液
溶液
(3)HCl溶液和![]() 溶液 (4)AlCl3溶液和氨水溶液
溶液 (4)AlCl3溶液和氨水溶液
A.(1)(2)(3)B.(2)(3)(4)C.(1)(2)D.(2)(3)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A、B、C、D之間的轉化關系如圖所示。下列說法正確的是( )

A.若A為Fe,C為氫氣,則B一定是酸
B.若A為H2O,B、D為化合物,則C一定是氣體單質
C.若C為單質,D為化合物,則A、B中一定有一種物質是單質
D.若D為單質,A、B為化合物,該反應一定屬于氧化還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,二元弱酸 H2Y 溶液中滴加 KOH 溶液,所得混合溶液的 pH 與離子濃度變化的關系如下圖所示,下列有關說法錯誤的是
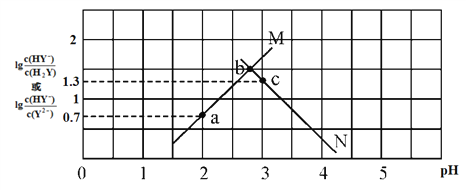
A. 曲線 M 表示 pH與 lg![]() 的變化關系
的變化關系
B. a點溶液中:c(H+) ― c(OH-)=2c(Y2-)+c(HY-) ― c(K+)
C. H2Y 的第二級電離常數Ka2(H2Y)=10-4.3
D. 交點b的溶液中:c(H2Y)=c(Y2-)>c(HY-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,在2 L密閉容器中,A、B、C三種氣體的物質的量隨時間變化的曲線如圖所示。下列說法正確的是
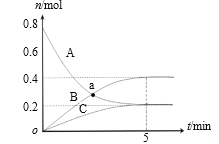
A.a點時,υ(A) =υ(B)
B.反應開始到5min,B的物質的量增加了0.2 mol
C.反應的化學方程式為:3A![]() 2B+C
2B+C
D.反應開始到5min,υ(C) =0.04 mol/(L·min)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】自來水是自然界中的淡水經過絮凝、沉淀、過濾、消毒等工藝處理后得到的。常用的自來水消毒劑有二氧化氯(ClO2)和高鐵酸鉀(K2FeO4)等。
(1)某研究小組用下圖裝置制備少量ClO2(夾持裝置已略去)。
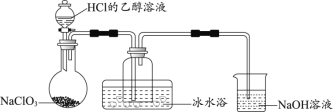
資料:ClO2常溫下為易溶于水而不與水反應的氣體,水溶液呈深黃綠色,11℃時液化成紅棕色液體。以NaClO3和HCl的乙醇溶液為原料制備ClO2的反應為2NaClO3 + 4HCl= 2ClO2↑+ Cl2↑+ 2NaCl + 2H2O。
①冰水浴的作用是____________。
② NaOH溶液中發生的主要反應的離子方程式為________________。
(2)將ClO2水溶液滴加到KI溶液中,溶液變棕黃;再向其中加入適量CCl4,振蕩、靜置,觀察到____,證明ClO2具有氧化性。
(3)ClO2在殺菌消毒過程中會產生副產物亞氯酸鹽(ClO2-),需將其轉化為Cl-除去。下列試劑中,可將ClO2-轉化為Cl-的是_____________________(填字母序號)。
a. FeSO4 b. O3 c. KMnO4 d. SO2
(4)K2FeO4是一種新型、綠色的多功能凈水劑,集氧化、吸附、絮凝、沉淀、滅菌、消毒、脫色、除臭等性能為一體。實驗室制備K2FeO4的方法如下:在冰水浴中,向KClO和KOH的混合溶液中少量多次加入硝酸鐵,并不斷攪拌。
①上述制備K2FeO4反應的離子方程式為______________________。
②凈水過程中,K2FeO4起到吸附、絮凝作用的原理是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高純度單晶硅是典型的無機非金屬材料,又稱“半導體”材料,它的發現和使用曾引起計算機的一場“革命”。這種材料可以按下列方法制備,下列說法正確的是
SiO2 ![]() Si(粗)
Si(粗) 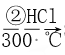 SiHCl3
SiHCl3 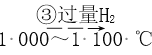 Si(純)
Si(純)
A. 步驟①的化學方程式為SiO2+C![]() Si+CO2↑
Si+CO2↑
B. 步驟①、②、③中每生成或反應1 mol Si,轉移2 mol電子
C. 二氧化硅能與氫氟酸反應,而硅不能與氫氟酸反應
D. SiHCl3(沸點33.0 ℃)中含有少量的SiCl4(沸點67.6 ℃),通過蒸餾可提純SiHCl3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家開發出一種“潔凈煤技術”,通過向地下煤層“氣化爐”中交替鼓入空氣和水蒸氣的方法,連續產出高熱值的煤炭氣,其主要成分是CO和H2。“氣化爐”中主要反應有:
C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJmol﹣1
CO(g)+H2O(g)=CO2(g)+H2(g)△H=﹣41.2kJmol﹣1
(1)氣化爐中CO2與C反應轉化為CO,該反應的熱化學方程式是___。
(2)用煤炭氣合成甲醇的反應為CO(g)+2H2(g)CH3OH(g)。在密閉容器中,將CO和H2按物質的量1:2混合反應,CO的平衡轉化率與溫度、壓強的關系如圖所示。
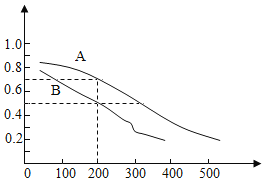
①生成甲醇的反應為___反應(填“放熱”或“吸熱”)。
②圖中兩條曲線分別表示壓強為0.1MPa和5.0MPa下CO轉化率隨溫度的變化,其中代表壓強是5.0MPa的曲線是___(填“A”或“B”)。
③在不改變反應物用量的前提下,為提高CO轉化率可采取的措施有___(答出一種即可)。
④壓強為0.1MPa、溫度為200℃時,平衡混合氣中甲醇的物質的量分數是___。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com