
【題目】下列物質屬于電解質的是( )
A. 稀硫酸 B. H2 C. NaCl D. 青銅
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】下列化學用語能正確表示相應意義的是( )
A.乙烯的結構簡式C2H4
B.丁烷的結構簡式CH3(CH2)2CH3
C.四氯化碳的結構式 ![]()
D.苯的分子式 ![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硝基苯是重要的精細化工原料,是醫藥和染料的中間體,還可做有機溶劑.制備硝基苯的過程如下: ①配制混酸:組裝如圖反應裝置.取100 mL燒杯,用20 mL濃硫酸與濃硝酸18 mL配制混和酸,加入漏斗中.把18 mL苯加入三頸燒瓶中.
②向室溫下的苯中逐滴加入混酸,邊滴邊攪拌,混和均勻.
③在50﹣60℃下發生反應,直至反應結束.
④除去混和酸后,粗產品依次用蒸餾水和10%Na2CO3溶液洗滌,最后再用蒸餾水洗滌得到粗產品.已知
(i) ![]() +HNO3(濃)
+HNO3(濃) ![]()
![]() +H2O
+H2O 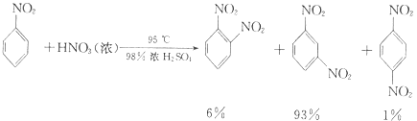
(ii)可能用到的有關數據列表如下
物質 | 熔點/℃ | 沸點/℃ | 密度(20℃)/gcm﹣3 | 溶解性 |
苯 | 5.5 | 80 | 0.88 | 微溶于水 |
硝基苯 | 5.7 | 210.9 | 1.205 | 難溶于水 |
1,3﹣二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
濃硝酸 | 83 | 1.4 | 易溶于水 | |
濃硫酸 | 338 | 1.84 | 易溶于水 |
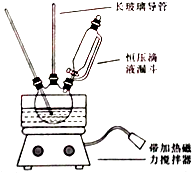
請回答下列問題:
(1)配置混酸應先在燒杯中先加入 .
(2)恒壓滴液漏斗的優點是 .
(3)實驗裝置中長玻璃管可用代替(填儀器名稱).
(4)反應結束后產品在液體的層(填“上”或者“下”),分離混酸和產品的操作方法為
(5)用10%Na2CO3溶液洗滌之后再用蒸餾水洗滌時,怎樣驗證液體已洗凈? .
(6)為了得到更純凈的硝基苯,還須先向液體中加入除去水,然后蒸餾,最終得到17.5g硝基苯,則硝基苯的產率為(保留兩位有效數字).若加熱后,發現未加沸石,應采取的操作是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)在反應A(g)+3B(g)=2C(g)中,若以物質A表示的該反應的化學反應速率為0.2 mol·L1·min1,則以物質B表示此反應的化學反應速率為________mol·L1·min1。
(2)在2 L的密閉容器中,充入2 mol N2和3 mol H2,在一定條件下發生反應,3 s后測得N2為1.9 mol,則以H2的濃度變化表示的反應速率為____________________________。
(3)將10 mol A和5 mol B放入容積為10 L的密閉容器中,某溫度下發生反應:3A(g)+B(g) ![]() 2C(g),在最初2 s內,消耗A的平均速率為0.06 mol·L1·s1,則在2 s時,容器中有______ mol A,此時C的物質的量濃度為________。
2C(g),在最初2 s內,消耗A的平均速率為0.06 mol·L1·s1,則在2 s時,容器中有______ mol A,此時C的物質的量濃度為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是(NA表示阿伏加德羅常數的量)( )
A. 在常溫常壓下, ![]() 氧氣和臭氧組成的混合氣體中所含氧原子數目為NA
氧氣和臭氧組成的混合氣體中所含氧原子數目為NA
B. 1mol![]() (碳正離子)中含電子數目為10NA
(碳正離子)中含電子數目為10NA
C. 標準狀況下,22.4LSO3中含有的氧原子數為3NA
D. 200mL 0.5mol/L硝酸銨溶液中含有![]() 0.1NA
0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫疊氮酸(HN3)及其鹽(如NaN3、NH4N3、CuN3等)都具有爆炸性,最近南京理工大學胡丙成教授團隊成功合成出PHAC,其化學式為(N3)6(H3O)3(NH4)4Cl。回答下列問題:
(1)PHAC中“N3”的化合價為______。N2F2的電子式為_______。
(2)汽車安全氣囊中的NaN3可發生下列反應:
NaN3(s)=Na(s)+3/2N2(g) △H1;
2NaN3(s)+CuO(s)=Na2O(s)+3N2(g)+Cu(s) △H1;
則反應CuO(s)+2Na(s)=Na2O(s)+Cu(s) △H=_______(用△H1和△H2表示)
(3)25℃時,將lmolNH4N3投入一2L的恒容密閉容器中,0.5min后反應達到平衡,測得生成的兩種單質的物質的量之和為1.6mol, 則NH4N3的平衡轉化率為_______,25℃時該反應的平衡常數K=________。
(4)氫疊氮酸(HN3)易溶于水,且酸性與醋酸相近。
①HN3在水溶液中的電離方程式為_______________.
② 0.1mol/L的HN3溶液與0.1mol/L的NaN3等體積混合,混合溶液中各離子濃度由大到小的順序為__________________。
③ 已知T℃時,Ksp(CuN3)=5.0×10-9,Ksp(Cu2S)=2.5×10-48,則相同溫度下反應:
Cu2S(s)+2N3-(aq)![]() 2CuN3(s)+S2-(aq)的平衡常數K=_________.
2CuN3(s)+S2-(aq)的平衡常數K=_________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“千年大計、國家大事”,雄安新區無疑是今年最受矚目的地區。不過,近日媒體報道河北廊坊、天津等地存在超大規模的工業污水滲坑,給雄安新區的水環境帶來隱患,目前正采用多種方法對污水進行處理,改善水資源狀況。
(1)在微生物作用的條件下,廢水中的NH4+經過兩步反應氧化成NO3-,兩步反應的能量變化示意圖如下:
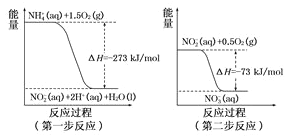
①第一步反應是______反應(選填“放熱”或“吸熱”),判新依據是_________。1mol NH4+ (aq)全部氧化成NO3- (aq)的熱化學方程式為_____________。
②一定條件下,向廢水中加入CH3OH,將HNO3還原成N2。若該過程中CH3OH反應生成CO2,則參加反應的還原劑和氧化劑的物質的量之比為______.
(2)二氧化氯(ClO2)是一種黃綠色到橙黃色的氣體,是國際上公認為安全、無毒的綠色消毒劑,可以投入廢水中清除污染物。
①二氧化氯可以將廢水中的氰化物(CN-)氧化成兩種無污染氣體.寫出離子方程式________。
②廢水中的重金屬離子的危害性很大,二氧化氯能夠在弱酸性溶液中把二價錳離子氧化成不溶于水的二氧化錳(MnO2),寫出反應的離子方程式_______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com