

|

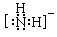
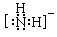 。(4)NH4H與D2O反應時,NH4H電離出來的NH4+離子與D2O電離出來的OD-結合生成NH3和HDO,NH4H電離出來的H-與D2O電離出來的D+反應生成HD,因此產物為HDO、HD、和NH3。Na3N與水反應的化學方程式為Na3N+3H2O=3NaOH+NH3↑。(5)X+中所有電子正好充滿K、L、M三個電子層,則X的電子排布式為1s22s22p63s23p63d104s1。根據晶胞結構可以看出與同一個N3-相連的X+有6個。(6)NaCl晶胞中一個Na+周圍有6個Cl-,一個Cl-周圍有6個Na+,ZN晶體具有與NaCl相似的晶體結構,所以符合的結構為AD。
。(4)NH4H與D2O反應時,NH4H電離出來的NH4+離子與D2O電離出來的OD-結合生成NH3和HDO,NH4H電離出來的H-與D2O電離出來的D+反應生成HD,因此產物為HDO、HD、和NH3。Na3N與水反應的化學方程式為Na3N+3H2O=3NaOH+NH3↑。(5)X+中所有電子正好充滿K、L、M三個電子層,則X的電子排布式為1s22s22p63s23p63d104s1。根據晶胞結構可以看出與同一個N3-相連的X+有6個。(6)NaCl晶胞中一個Na+周圍有6個Cl-,一個Cl-周圍有6個Na+,ZN晶體具有與NaCl相似的晶體結構,所以符合的結構為AD。

 口算小狀元口算速算天天練系列答案
口算小狀元口算速算天天練系列答案科目:高中化學 來源:不詳 題型:填空題
| 元素 | 相關結構和性質 |
| A | 其單質的一種晶體不是金屬晶體,但是電的良導體,且難熔、質軟并有潤滑性,可用作原子核反應堆的慢化劑、火箭發動機噴灌和電極材料等。 |
| B | 其單質既能與強酸溶液反應,又能與強堿溶液反應,其簡單離子在第三周期單核離子中半徑最小。 |
| C | 是蛋白質的組成元素之一,原子核外有三種不同能量的電子,且未成對電子數最多。 |
| D | 原子核外最外層電子排布式為nsnnp2n+1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| A原子核外電子分占3個不同能級,且每個能級上排布的電子數相同 |
| B元素原子的核外p電子總數比s電子總數少1 |
| C原子p軌道上成對電子數等于未成對電子數,且與A同周期 |
| D元素的族序數與周期數的差為4,且不與A元素在同一周期 |
| E位于周期表中第七列 |
| F元素基態原子的M層全充滿,N層沒有成對電子,只有一個未成對電子 |

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| 元素符號 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| x 值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.M<N<Y<X<Z | B.N<M<X<Y<Z |
| C.N<M<Y<X<Z | D.X<Z<N<M<Y |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題


查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| 電離能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 899 | 1 757 | 14 840 | 21 000 |
| B | 738 | 1 451 | 7 733 | 10 540 |

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| 元素 | A | B | D |
| 性質或結構信息 | 工業上通過分離液態空氣獲得其單質,單質能助燃 | 氣態氫化物的水溶液顯堿性 | 原子有三個電子層,簡單離子在本周期中半徑最小 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com