
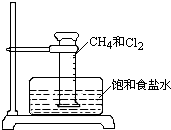
 某課外活動小組利用如圖所示裝置探究甲烷于氯氣的反應.根據題意,回答下列問題:
某課外活動小組利用如圖所示裝置探究甲烷于氯氣的反應.根據題意,回答下列問題:分析 ①甲烷為飽和烷烴,在光照條件下能夠與氯氣發生取代反應,若用日光直射,可能會引起爆炸;甲烷與氯氣發生一氯取代反應生成一氯甲烷和氯化氫;
②甲烷發生取代反應生成氯化氫,氯氣消耗所以量筒內顏色變淺,氣體減少所以壓強減小,量筒內的壓強減小,量筒內液面上升.因生成的HCl易溶于水,溶液中Cl-濃度增大,使氯化鈉的溶解平衡逆向移動,反應生成CH2Cl2、CHCl3、CCl4常溫下是無色油液體;
③氯氣在飽和食鹽水中的溶解度降低;
④取代反應是指有機化合物分子中任何一個原子或基團被試劑中同類型的其它原子或基團所取代的反應;依據反應2CHCl3+O2→2COCl2+2HCl,生成的產物氯化氫的性質解答.
解答 解:①CH4和Cl2在光照(或光亮處)條件下發生反應,若用日光直射,反應非常劇烈,可能會引起爆炸,甲烷與氯氣反應生成一氯甲烷的方程式為:CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl,
故答案為:光照(或光亮處);爆炸;CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl;
②甲烷發生取代反應生成氯化氫,氯氣消耗所以量筒內顏色變淺,氣體減少所以壓強減小,量筒內的壓強減小,量筒內液面上升.因生成的HCl易溶于水,溶液中Cl-濃度增大,使氯化鈉的溶解平衡逆向移動,反應生成CH2Cl2、CHCl3、CCl4常溫下是無色油液體,所以看到的現象有:量筒內壁出現油狀液滴,飽和食鹽水中有少量固體析出,量筒內黃綠色氣體顏色變淺;量筒內液面上升;
故答案為:量筒內黃綠色氣體顏色變淺 量筒內液面上升;
③氯氣和水反應生成鹽酸和次氯酸,飽和食鹽水電離出氯離子,氯氣在飽和食鹽水中的溶解度降低,所以用飽和食鹽水而不用水的原因是降低Cl2在水中溶解度,抑制Cl2和水的反應,
故答案為:降低Cl2在水中溶解度,抑制Cl2和水的反應;
④反應前碳與氫原子和三個氯原子都是以單的鍵相連,反應之后碳氧之間是雙鍵,不符合取代反應的特點,不所以取代反應;
氯仿如果變質則發生反應2CHCl3+O2→2COCl2+2HCl,生成的氯化氫溶于水,電離產生氫離子和氯離子,所以能夠使濕潤的藍色石蕊試紙變紅色,加入硝酸銀溶液會發生反應生成白色的氯化銀沉淀,
故選:B;BE.
點評 本題考查了探究甲烷于氯氣的反應的實驗,熟悉甲烷的結構、性質是解題關鍵,注意④為易錯選項,抓住物質的性質是解題關鍵,題目難度中等.


 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | HClO4、KClO3 | B. | KClO、KCl | C. | NaClO、KCl | D. | NaCl、KCl |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 金屬性逐漸增強 | B. | 原子半徑逐漸增大 | ||
| C. | 最高正價數值逐漸增大 | D. | 從硅到氯負價從-4-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用滲析法分離Fe(OH)3膠體和FeCl3溶液的混合物 | |
| B. | 用重結晶法提純NaCl和KNO3的混合物中的KNO3 | |
| C. | 用蒸餾法分離乙醇和甲醇的混合物 | |
| D. | 用分液的方法分離甘油和水的混合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 表示的分子式C6H14;名稱是2-甲基戊烷.
表示的分子式C6H14;名稱是2-甲基戊烷. 中含有的官能團的名稱為羥基、酯基.
中含有的官能團的名稱為羥基、酯基.
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 編號 | 化學反應 | 離子方程式 | 評價 |
| A | 過氧化鈉與水反應 | 2O22-+2H2O═4OH-+O2↑ | 正確 |
| B | 漂白粉溶液中通入過量SO2 | ClO-+H2O+SO2═ HSO3-+HClO | 正確 |
| C | Fe3O4溶于鹽酸 | Fe3O4+8H+═2Fe3++Fe2++4H2O | 錯誤,應只生成Fe3+ |
| D | 碳酸氫鈣溶液中加入過量的氫氧化鈉溶液 | Ca2++HCO3-+OH- ═CaCO3↓+H2O | 錯誤,產物及配平不對 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com